FDA cảnh báo vaccine ngừa RSV của GSK và Pfizer có nguy cơ gây liệt hiếm gặp
Cục Quản lý Thực phẩm và Dược phẩm Mỹ ( FDA) vừa đưa ra cảnh báo về nguy cơ hiếm gặp liên quan đến 2 loại vaccine phòng ngừa virus hợp bào hô hấp ( RSV) của GSK Plc và Pfizer Inc.
Các loại vaccine này phải được dán nhãn cảnh báo rằng chúng có thể làm tăng nguy cơ mắc hội chứng Guillain-Barre, một rối loạn thần kinh nghiêm trọng có thể dẫn đến yếu cơ và liệt toàn thân.
Vaccine Pfizer-BioNTech Covid-19 dành cho trẻ em tại một phòng tiêm chủng của Salvation Army ở Philadelphia, Pennsylvania, Mỹ, ngày 12/11/2021. (Nguồn: Bloomberg)
Cảnh báo này được đưa ra sau khi FDA phân tích dữ liệu từ các nghiên cứu theo dõi những người đã tiêm 2 loại vaccine ngừa RSV là Arexvy của GSK và Abrysvo của Pfizer.
Kết quả cho thấy, nguy cơ mắc hội chứng Guillain-Barre tăng cao trong vòng 42 ngày sau khi tiêm chủng. Theo dữ liệu của FDA, cứ mỗi triệu liều vaccine Abrysvo được tiêm, có khoảng 9 trường hợp mắc hội chứng Guillain-Barre vượt mức. Đối với Arexvy, con số này là 7 trường hợp trên mỗi triệu liều, đặc biệt ở nhóm người từ 65 tuổi trở lên.
Video đang HOT
Hội chứng Guillain-Barre là một rối loạn tự miễn, trong đó hệ miễn dịch của cơ thể tấn công nhầm vào các dây thần kinh, gây ra tình trạng tê yếu và mất kiểm soát cơ bắp. Trong một số trường hợp nghiêm trọng, hội chứng này có thể dẫn đến liệt hoàn toàn.
Hiện tại, y học chưa tìm ra cách chữa trị dứt điểm cho căn bệnh này. Tuy nhiên, FDA nhấn mạnh rằng dữ liệu hiện có chưa đủ để khẳng định chắc chắn rằng vaccine là nguyên nhân trực tiếp gây ra hội chứng Guillain-Barre.
Thay vào đó, cơ quan này khuyến nghị các công ty dược phẩm cần bổ sung thông tin cảnh báo vào tờ hướng dẫn sử dụng vaccine để người dùng được thông báo rõ về rủi ro tiềm ẩn này.
Mối nguy cơ liên quan đến hội chứng Guillain-Barré từ vaccine không phải là điều mới. Trước đây, FDA từng đưa ra cảnh báo tương tự đối với vaccine Covid-19 của Johnson & Johnson vào năm 2021, khi phát hiện nguy cơ nhỏ về hội chứng Guillain-Barre sau khi tiêm loại vaccine này.
Trước đại dịch Covid-19, hội chứng này cũng đã từng được ghi nhận liên quan đến vaccine phòng cúm mùa. Dù vậy, tỷ lệ mắc hội chứng Guillain-Barre sau khi tiêm vaccine luôn ở mức rất thấp, chỉ xảy ra trong một số trường hợp hiếm gặp.
Nguy cơ này cũng đã được Trung tâm Kiểm soát và Phòng ngừa Dịch bệnh Mỹ (CDC) thảo luận vào năm 2024, khi hội đồng cố vấn vaccine của cơ quan này xem xét dữ liệu liên quan đến vaccine ngừa RSV. Song, dữ liệu tại thời điểm đó chưa đủ rõ ràng để đưa ra cảnh báo cụ thể.
Các nhà khoa học cho biết, nghiên cứu sau khi vaccine được đưa vào sử dụng trên thị trường vẫn đang tiếp tục để làm rõ hơn về mối liên hệ giữa vaccine ngừa RSV và hội chứng Guillain-Barre.
Các công ty GSK và Pfizer hiện chưa đưa ra phản hồi về cảnh báo mới này. FDA cho biết, cơ quan này sẽ tiếp tục giám sát và thu thập dữ liệu để đảm bảo an toàn cho các loại vaccine đang lưu hành trên thị trường.
Hội chứng Guillain-Barre không chỉ liên quan đến vaccine ngừa RSV mà còn từng gây tranh cãi đối với nhiều loại vaccine khác, bao gồm vaccine phòng ngừa virus papilloma ở người (HPV) và bệnh não mô cầu. Thế nhưng, bằng chứng về mối liên hệ giữa các loại vaccine này và hội chứng Guillain-Barre vẫn còn hạn chế và chưa đủ rõ ràng để đưa ra kết luận chắc chắn.
FDA Mỹ phê duyệt vaccine của Merck phòng ngừa phế cầu khuẩn ở người trưởng thành
Ngày 18/6, hãng dược phẩm Merck (Đức) cho biết Cơ quan Quản lý Thực phẩm và Dược phẩm của Mỹ (FDA) đã cấp phép loại vaccine mới do hãng bào chế để phòng ngừa nhiễm phế cầu khuẩn gây viêm phổi và nhiều bệnh nghiêm trọng khác ở người trưởng thành.
Vaccine phòng ngừa phế cầu khuẩn ở người trưởng thành do Merck bào chế. Ảnh: Merck
Vaccine đơn liều Capvaxive phòng ngừa 21 chủng của phế cầu khuẩn, ngăn chặn một dạng nghiêm trọng của bệnh phế cầu khuẩn có thể xâm lấn các bộ phận khác của cơ thể và dẫn đến viêm phổi. Theo Merck, đây là loại vaccine phế cầu liên hợp đầu tiên được bào chế dành riêng cho người trưởng thành và đem lại khả năng bảo vệ rộng hơn so với các loại vaccine hiện có trên thị trường. Vaccine này cũng giúp chống lại 8 chủng phế cầu khuẩn mà những loại vaccine được phê duyệt hiện nay chưa ngăn chặn được.
Theo số liệu giai đoạn 2018 - 2021do Merck trích dẫn từ Trung tâm kiểm soát và phòng ngừa dịch bệnh Mỹ (CDC), 8 chủng này chiếm 30% số trường hợp mắc bệnh phế cầu khuẩn xâm lấn ở những người từ 65 tuổi trở lên.
Sau khi vaccine được FDA cấp phép, ban cố vấn của CDC sẽ nhóm họp vào ngày 27/6 tới để xem xét những người đủ điều kiện tiêm phòng vaccine này.
Người trưởng thành khỏe mạnh vẫn có nguy cơ mắc bệnh phế cầu khuẩn. Tuy nhiên, những bệnh nhân cao tuổi và những người mắc bệnh mãn tính hoặc suy giảm hệ miễn dịch có nguy cơ mắc bệnh cao hơn, đặc biệt là những loại bệnh phế cầu khuẩn nghiêm trọng hơn hay còn gọi là dạng "xâm lấn".
Thống kê cho thấy khoảng 150.000 người Mỹ trưởng thành phải nhập viện vì viêm phổi do phế cầu khuẩn gây ra mỗi năm. Trong một thông báo vào tháng 12/2023, Merck cho biết tỷ lệ tử vong do bệnh phế cầu khuẩn xâm lấn cao nhất ở bệnh nhân từ 50 tuổi trở lên.
Hiện có 2 loại vaccine phòng phế cầu khuẩn của Merck lưu hành trên thị trường, nhưng không có loại vaccine nào dành cho người trưởng thành. Trong đó, vaccine Vaxneuvance đã được cấp phép tại Mỹ để tiêm cho những trẻ từ 6 tuần tuổi trở lên.
Trong khi đó, vaccine đơn liều Prevnar 20 của hãng Pfizer (Mỹ) hiện là loại vaccine hàng đầu dành cho người trưởng thành.
Mỹ cân nhắc sử dụng vaccine ngừa virus hợp bào hô hấp cho người lớn tuổi  Theo phóng viên TTXVN tại Washington, ngày 21/6, Ủy ban Cố vấn tiêm chủng của Trung tâm Kiểm soát và Phòng ngừa dịch bệnh Mỹ (CDC) dự kiến sẽ bỏ phiếu về khuyến nghị sử dụng vaccine mới được phê duyệt gần đây của các hãng dược Pfizer và GSK để ngăn ngừa nhiễm virus hợp bào hô hấp (RSV) nghiêm trọng ở...
Theo phóng viên TTXVN tại Washington, ngày 21/6, Ủy ban Cố vấn tiêm chủng của Trung tâm Kiểm soát và Phòng ngừa dịch bệnh Mỹ (CDC) dự kiến sẽ bỏ phiếu về khuyến nghị sử dụng vaccine mới được phê duyệt gần đây của các hãng dược Pfizer và GSK để ngăn ngừa nhiễm virus hợp bào hô hấp (RSV) nghiêm trọng ở...
 Trung Quốc tung chatbot đấu ChatGPT, cổ phiếu Phố Wall chao đảo bốc hơi 1.000 tỉ14:53
Trung Quốc tung chatbot đấu ChatGPT, cổ phiếu Phố Wall chao đảo bốc hơi 1.000 tỉ14:53 Ý tưởng gây sốc của Tổng thống Trump về Dải Gaza08:59
Ý tưởng gây sốc của Tổng thống Trump về Dải Gaza08:59 Hé lộ kế hoạch mới của ông Trump về xung đột Nga-Ukraine08:31
Hé lộ kế hoạch mới của ông Trump về xung đột Nga-Ukraine08:31 Iran công bố tên lửa đạn đạo mới nhất08:23
Iran công bố tên lửa đạn đạo mới nhất08:23 Tổng thống Trump lên tiếng về 'thảm kịch' hàng không ở thủ đô Washington DC10:41
Tổng thống Trump lên tiếng về 'thảm kịch' hàng không ở thủ đô Washington DC10:41 Ông Trump cấm người chuyển giới tham gia các môn thể thao dành cho nữ08:45
Ông Trump cấm người chuyển giới tham gia các môn thể thao dành cho nữ08:45 Nga sắp cho chạy thử 'chiến hạm mạnh nhất thế giới' sau cuộc đại tu?10:04
Nga sắp cho chạy thử 'chiến hạm mạnh nhất thế giới' sau cuộc đại tu?10:04 Hamas vừa thả 4 nữ binh sĩ Israel, sẽ nhận lại được gì?02:38
Hamas vừa thả 4 nữ binh sĩ Israel, sẽ nhận lại được gì?02:38 CIA có đánh giá mới về nguồn gốc Covid-1908:54
CIA có đánh giá mới về nguồn gốc Covid-1908:54 Lãnh đạo nước ngoài đầu tiên được ông Trump mời đến Nhà Trắng08:45
Lãnh đạo nước ngoài đầu tiên được ông Trump mời đến Nhà Trắng08:45 Máy bay rơi gần trung tâm thương mại ở Mỹ, nhiều người thương vong03:42
Máy bay rơi gần trung tâm thương mại ở Mỹ, nhiều người thương vong03:42Tiêu điểm
Tin đang nóng
Tin mới nhất

Tổng thống Donald Trump tiết lộ mức thuế quan mới 'linh hoạt' với từng nước

Tổng thống Mỹ ký sắc lệnh đóng băng nguồn tài trợ cho Nam Phi

Tỷ phú Musk thúc giục Mỹ đầu tư vào UAV và AI để giành lợi thế trong chiến tranh

Gặp gỡ mừng Xuân Ất Tỵ và kỷ niệm 95 năm thành lập Đảng tại Brazil

Tín hiệu mới của Tổng thống Trump về cuộc gặp thượng đỉnh Mỹ - Triều
UNAIDS lo ngại việc Mỹ ngừng viện trợ nước ngoài

Hội đồng Nhân quyền Liên hợp quốc yêu cầu Rwanda rút quân khỏi CHDC Congo

Tổng thống Mỹ tuyên bố ý định sa thải Hội đồng quản trị Trung tâm Kennedy

Tìm thấy xác máy bay rơi ở Alaska, 10 người được cho đã thiệt mạng

Tổng thống Putin chỉ đạo thay đổi cơ cấu tăng trưởng kinh tế của Nga

Hai đại tá Nga bị rơi khỏi cửa sổ trong cùng một ngày

Hé lộ 5 điểm chính trong kế hoạch chấm dứt xung đột Ukraine của ông Trump
Có thể bạn quan tâm

'Đèn âm hồn' gây sốt phòng vé nhưng vướng tranh cãi, đạo diễn nói gì?
Hậu trường phim
18:04:31 08/02/2025
HOT: Hoa hậu Lê Hoàng Phương phản ứng gắt ra mặt khi bị hỏi chuyện yêu bạn trai vừa chia tay của Thiều Bảo Trâm
Sao việt
17:54:49 08/02/2025
Hôm nay nấu gì: Bữa cơm ít thịt nhiều rau vẫn siêu ngon
Ẩm thực
17:50:45 08/02/2025
Đấu vật với hot girl xinh đẹp, đối thủ nam hé lộ trải nghiệm khó quên
Netizen
17:15:26 08/02/2025
Thầy phong thủy dặn: Đi chợ mua cỗ Tết đừng ham hố 5 món này, cả người lẫn của đều lao đao
Trắc nghiệm
17:09:59 08/02/2025
Hình ảnh một người bị khiêng khỏi sự kiện của nhóm nam triệu bản dấy lên lo ngại
Nhạc quốc tế
15:55:51 08/02/2025
Nóng: 700 ngàn người dậy sóng trước clip Taylor Swift - Miley Cyrus công khai cạch mặt nhau tại Grammy
Sao âu mỹ
15:52:11 08/02/2025
Hành khách trong vụ tai nạn ở Phú Yên: Đi Đà Lạt chụp ảnh cưới thì bị nạn
Tin nổi bật
15:27:26 08/02/2025
 Động đất tại Tây Tạng: Nâng cấp độ ứng phó khẩn cấp lên mức 2
Động đất tại Tây Tạng: Nâng cấp độ ứng phó khẩn cấp lên mức 2 Hungary cáo buộc Ukraine đẩy châu Âu vào thế khó
Hungary cáo buộc Ukraine đẩy châu Âu vào thế khó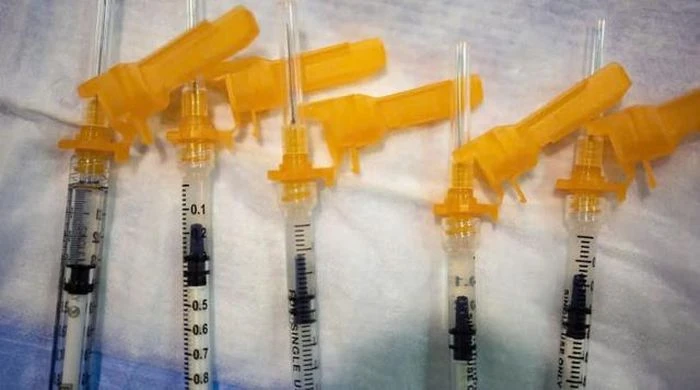
 Năm mới, 250 loại thuốc tăng giá ở Mỹ
Năm mới, 250 loại thuốc tăng giá ở Mỹ Việt Nam ghi nhận hàng chục nghìn ca, bệnh tay chân miệng vẫn là thách thức lớn
Việt Nam ghi nhận hàng chục nghìn ca, bệnh tay chân miệng vẫn là thách thức lớn Suy giảm ca mắc và tử vong chưa đủ để xóa sổ AIDS trên toàn cầu
Suy giảm ca mắc và tử vong chưa đủ để xóa sổ AIDS trên toàn cầu Australia phê duyệt vaccine tăng cường mới ngăn ngừa COVID-19
Australia phê duyệt vaccine tăng cường mới ngăn ngừa COVID-19 Các nước bỏ lỡ thời hạn đạt được thỏa thuận toàn cầu về đại dịch
Các nước bỏ lỡ thời hạn đạt được thỏa thuận toàn cầu về đại dịch WHO kêu gọi phát triển vaccine phòng các căn bệnh gây tử vong trên diện rộng
WHO kêu gọi phát triển vaccine phòng các căn bệnh gây tử vong trên diện rộng

 Tổng thống Mỹ ký sắc lệnh trừng phạt Tòa án Hình sự quốc tế
Tổng thống Mỹ ký sắc lệnh trừng phạt Tòa án Hình sự quốc tế

 Điểm tên những quốc gia đã cấm ứng dụng AI DeepSeek của Trung Quốc
Điểm tên những quốc gia đã cấm ứng dụng AI DeepSeek của Trung Quốc Nữ sinh mất tích bí ẩn ở TPHCM được tìm thấy tại Trung Quốc
Nữ sinh mất tích bí ẩn ở TPHCM được tìm thấy tại Trung Quốc
 Danh tính nạn nhân tử vong trong xe khách 54 chỗ bị lật ở Phú Yên
Danh tính nạn nhân tử vong trong xe khách 54 chỗ bị lật ở Phú Yên Kinh hoàng vụ lật xe khách tại Phú Yên và lời kể của nạn nhân
Kinh hoàng vụ lật xe khách tại Phú Yên và lời kể của nạn nhân Hoa hậu Kỳ Duyên đã căng: Phản pháo gắt khi bị đùa quá lố chuyện giới tính
Hoa hậu Kỳ Duyên đã căng: Phản pháo gắt khi bị đùa quá lố chuyện giới tính Nữ sinh Sơn La 17 tuổi mất tích: Gia đình nhận tin con gái ở Cần Thơ
Nữ sinh Sơn La 17 tuổi mất tích: Gia đình nhận tin con gái ở Cần Thơ Đòn trừng phạt chồng cũ Từ Hy Viên và mẹ chồng cũ sau trò lố lợi dụng cái chết của minh tinh
Đòn trừng phạt chồng cũ Từ Hy Viên và mẹ chồng cũ sau trò lố lợi dụng cái chết của minh tinh Cha nghèo bán hết tài sản, vay mượn để con học ĐH, con ra trường lương tháng 2 triệu đồng: Sai lầm khiến nhiều phụ huynh giật mình
Cha nghèo bán hết tài sản, vay mượn để con học ĐH, con ra trường lương tháng 2 triệu đồng: Sai lầm khiến nhiều phụ huynh giật mình Thi thể thiếu niên 16 tuổi bị cột vào đầu bơm nước, nổi trên kênh ở Đồng Tháp
Thi thể thiếu niên 16 tuổi bị cột vào đầu bơm nước, nổi trên kênh ở Đồng Tháp NS Lê Quốc Nam tiếp tục lên tiếng sau khi tố Minh Dự: "Tôi nhận lời xin lỗi, họ xin làm sự việc nhẹ lại"
NS Lê Quốc Nam tiếp tục lên tiếng sau khi tố Minh Dự: "Tôi nhận lời xin lỗi, họ xin làm sự việc nhẹ lại" Danh tính các nạn nhân tử vong trong xe khách bị lật ở Phú Yên
Danh tính các nạn nhân tử vong trong xe khách bị lật ở Phú Yên Thông tin mới vụ xe tải cán qua người đi xe máy 2 lần trên Quốc lộ 51 ở Đồng Nai
Thông tin mới vụ xe tải cán qua người đi xe máy 2 lần trên Quốc lộ 51 ở Đồng Nai Bức ảnh làm lộ chuyện 2 con Từ Hy Viên bị bỏ bê nghiêm trọng sau khi đột ngột mất mẹ
Bức ảnh làm lộ chuyện 2 con Từ Hy Viên bị bỏ bê nghiêm trọng sau khi đột ngột mất mẹ Châu Du Dân 2 lần đưa tang tình cũ: Trầm cảm vì mất Hứa Vỹ Luân, 18 năm sau bi kịch lặp lại với Từ Hy Viên
Châu Du Dân 2 lần đưa tang tình cũ: Trầm cảm vì mất Hứa Vỹ Luân, 18 năm sau bi kịch lặp lại với Từ Hy Viên Ca sĩ Lynda Trang Đài sau khi bị bắt vì ăn trộm: Có động thái lạ trên MXH, dàn sao hé lộ tình trạng bất ổn
Ca sĩ Lynda Trang Đài sau khi bị bắt vì ăn trộm: Có động thái lạ trên MXH, dàn sao hé lộ tình trạng bất ổn Bạn thân tiết lộ tình trạng của Uông Tiểu Phi: Tái phát bệnh tâm thần, liên tục gào thét "Tôi muốn chết"
Bạn thân tiết lộ tình trạng của Uông Tiểu Phi: Tái phát bệnh tâm thần, liên tục gào thét "Tôi muốn chết"
 Chấn động: Bằng chứng "nút thắt" trong vụ án của Tangmo Nida lộ diện sau 3 năm, cuộc điều tra liệu có bước ngoặt?
Chấn động: Bằng chứng "nút thắt" trong vụ án của Tangmo Nida lộ diện sau 3 năm, cuộc điều tra liệu có bước ngoặt?