Mỹ ‘khát’ thuốc kháng virus chữa Covid-19
Sản xuất remdesivir cung cấp cho nhiều nước điều trị Covid-19, y tế Mỹ lại khan hiếm loại thuốc kháng virus này, buộc phải lựa chọn bệnh nhân được dùng.
“Chính phủ Mỹ tài trợ cho quá trình sản xuất remdesivir, nhưng rất nhiều bệnh nhân Covid-19 nằm viện không được nhận thuốc”, Patterson, trưởng bộ phận các bệnh truyền nhiễm tại Trung tâm Khoa học Y tế Đại học Texas, San Antonio, tuyên bố.
Bác sĩ Thomas Patterson cho biết không đủ thuốc kháng virus remdesivir cho hơn 30% bệnh nhân trong đợt bùng phát Covid-19 tại Texas gần đây. Ông buộc lựa chọn bệnh nhân nào được kê thuốc, bệnh nhân nào không. Cho tới nay, remdesivir là loại thuốc duy nhất được phê duyệt điều trị Covid-19 tại Mỹ.
Vì thiếu nguồn cung, các bệnh viện Mỹ không thể mua remdesivir theo cách họ mua các thuốc khác. Bộ Y tế và Dịch vụ Nhân sinh (HHS) sắp xếp để sản phẩm được giao đến các bệnh viện thường xuyên.
Trong khi hãng dược Gilead khẳng định sản xuất đủ số thuốc đáp ứng nhu cầu, nguồn cung thường xuyên khan hiếm đối với phần lớn bệnh nhân Mỹ.
Theo khảo sát hồi tháng 7 của Hội Dược sĩ Hệ thống Y tế Mỹ, gần 33% trong hơn 131 bệnh viện không được nhận đủ lô remdesivir đáp ứng nhu cầu điều trị.
Bác sĩ Peter Chin-Hong, chuyên gia bệnh truyền nhiễm tại UCSF Health, cho hay ông nhiều lần có ý định mượn trước một lượng thuốc từ các cơ sở y tế lân cận, hứa sẽ trả lại khi bệnh viện của ông được nhận đợt hàng mới.
Trong khi đó, nhờ việc dùng thuốc gốc của remdesivir, tại nhiều nước đang phát triển, gồm Bangladesh, Pakistan, Philippines nguồn cung cho các bệnh viện luôn dồi dào.
Lô thuốc gốc remdesivir tại Hàn Quốc, ngày 30/7. Ảnh: Reuters
Bác sĩ Ahmedul Kabir, giáo sư y khoa tại Đại học Y Dhaka, Bangladesh cho hay các bệnh viện nơi ông công tác đặt mua thuốc gốc, do đó luôn đủ remdesivir điều trị cho bệnh nhân.
Video đang HOT
“Bangladesh là một quốc gia thuộc thế giới thứ ba, chúng tôi có đủ lượng remdesivir đáp ứng nhu cầu. Thật ngạc nhiên Mỹ lại không đủ. Đất nước họ đáng lẽ phải cung cấp nhiều dồi dào”, Kabir nói.
“Chúng tôi có thể sản xuất nhiều hơn. Hiện, sản lượng thuốc đạt 80.000 lọ mỗi tháng. Chúng tôi có thể tăng năng suất lên đến 150.000 lọ”, Rabbur Reza, giám đốc điều hành Beximco tuyên bố. Beximco là một trong những hãng dược tại Bangladesh.
Trong khi đó tại Mỹ, Gilead là đơn vị độc quyền bán remdesivir, không có đối thủ cạnh tranh.
Tại cuộc họp báo hôm 8/9, các bác sĩ, luật sư và một thành viên Quốc hội đã lên án chính quyền Tổng thống Donald Trump vì không đảm bảo nguồn cung.
“Những người mắc Covid-19 đáng ra có thể được chữa trị, giảm các cơn đau và thời gian nhập viện. Thực tế, họ không nhận được sự hỗ trợ nào vì chính quyền Trump từ chối hành động”, Lloyd Doggett, một đảng viên Đảng Dân chủ Texas, cho biết. “Chúng ta có thể nhanh chóng mở rộng nguồn cung nếu ông Trump thực hiện một số vai trò lãnh đạo, dù đã muộn màng”.
Christopher Morten, chuyên gia luật tại Đại học Luật thành phố New York, cho biết chính quyền Tổng thống Trump có thể điều chỉnh quy định, cho phép “mở cửa” bằng sáng chế, để Gilead thu lợi từ việc bán thuốc remdesivir, mà các công ty khác vẫn được phép sản xuất các phiên bản thuốc gốc.
Theo dữ liệu Gilead Sciences trình bày trước Cơ quan Quản lý Thực phẩm và Dược phẩm Mỹ (FDA), thuốc kháng virus remdesivir giảm thời gian nằm viện trung bình từ 10-15 ngày với các bệnh nhân Covid-19 nặng. Mỗi đợt điều trị kéo dài 5 ngày có giá 2.340 USD.
Kịch bản ra mắt vaccine Covid-19 đầu tháng 11
Trung tâm Kiểm soát và Phòng ngừa Dịch bệnh Mỹ (CDC) vạch ra kịch bản phê duyệt vaccine Covid-19 vào tháng 11, với hai loại "Vaccine A" và "Vaccine B" giả định.
CDC đã thông báo cho giới chức y tế ở 50 bang và 5 thành phố lớn là New York, Chicago, Philadelphia, Houston và San Antonio, chuẩn bị phân phối các liều chủng ngừa Covid-19 cho nhân viên y tế và nhóm có nguy cơ cao nhiễm bệnh. Hướng dẫn của CDC là dấu hiệu mới nhất về sự tăng tốc của Mỹ trong cuộc chạy đua tìm cách đẩy lùi đại đại dịch.
Ba tài liệu liên quan đã được CDC gửi đi hôm 27/8, cùng ngày với phát biểu của Tổng thống Donald Trump tại Hội nghị Quốc gia Đảng Cộng hòa, rằng vaccine Covid-19 sẽ ra mắt trong năm nay.
CDC phác thảo kịch bản chi tiết phân phối hai ứng viên tiềm năng không xác định, tạm gọi là "Vaccine A" và "Vaccine B", mỗi loại đều cần dùng hai liều, cách nhau vài tuần. Chương trình tiêm chủng dự kiến triển khai tại các bệnh viện, phòng khám, cơ sở y tế. Trung tâm đưa ra các đặc điểm kỹ thuật cần thiết, liên quan đến khâu vận chuyển, điều chế và quản lý.
Các đặc điểm này dường như phù hợp với sản phẩm của hãng dược Pfizer và Moderna.
Các yêu cầu khác, bao gồm nhiệt độ bảo quản bắt buộc, thời gian giữa các mũi tiêm và loại trung tâm y tế có thể đáp ứng lưu trữ, cũng khớp với những gì hai hãng cam kết về sản phẩm của mình.
Trong kịch bản giả định, "ứng viên" từ Pfizer giống với "Vaccine A", sẽ ra mắt khoảng hai triệu liều. Sản phẩm từ Moderna đáp ứng những yêu cầu của "Vaccine B", phân phối khoảng một triệu liều.
Nhiệt độ bảo quản của sản phẩm từ Pfizer là âm 70 độ C, có nghĩa nó không thể sử dụng ở hầu hết các địa điểm nhỏ. Vaccine của Moderna cần trữ đông ở nhiệt độ âm 20 độ C.
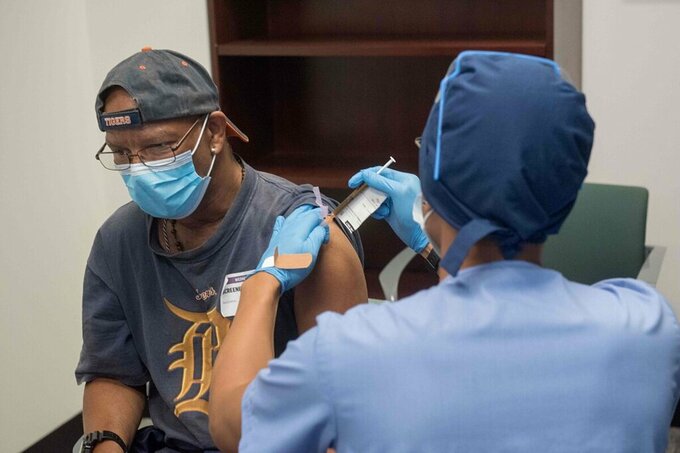
Tình nguyện viên tiêm thử vaccine của Moderna tại Detroit vào tháng 8/2020. Ảnh: AFP
Tại cuộc thảo luận ngày 26/8 của Ủy ban Tư vấn về Thực hành Tiêm chủng, Tiến sĩ Kathleen Dooling, thành viên CDC, đưa ra các tình huống: Vaccine A (giả định là vacicne Pfizer) hoặc Vaccine B (giả định là vaccine) được chấp thuận. Trường hợp còn lại, cả hai "ứng viên" đều nhận được cái gật đầu của cơ quan y tế.
Tài liệu của CDC cho biết sẽ cung cấp miễn phí các liều tiêm cho người dùng. Song nếu chúng được phê duyệt khẩn cấp thay vì chấp thuận theo tiêu chuẩn hiện hành, nhà sản xuất sẽ không được hoàn trả chi phí hành chính.
Theo tiến sĩ Anthony Fauci, Viện trưởng Viện Dị ứng và Bệnh truyền nhiễm Quốc gia, nếu kết quả khả quan, vaccine có thể được phân phối trước khi hoàn thành thử nghiệm lâm sàng. Chuyên gia y tế công cộng cho rằng các cơ quan chính phủ cần khẩn trương chuẩn bị cho nỗ lực lớn và phức tạp cuối cùng, đảm bảo tiêm chủng cho hàng trăm triệu người Mỹ.
Hướng dẫn lưu ý các nhân viên y tế, chăm sóc sức khỏe dài hạn, lực lượng an ninh quốc gia sẽ được ưu tiên. Người từ 65 tuổi trở lên, công dân Mỹ bản địa, thuộc "nhóm dân tộc thiểu số", có nguy cơ cao mắc bệnh hoặc dễ diễn tiến nặng cũng được sử dụng vaccine đầu tiên.
"Đây là kế hoạch tích cực bởi nó không chỉ chú trọng đến những người sống tại vùng ngoại ô giàu có, thu nhập cao", tiến sĩ Cedric Dark, Đại học Y Baylor ở Texas, nhận định.
Trong hướng dẫn, CDC cũng nhấn mạnh: "Các liều vaccine Covid-19 giới hạn có thể ra mắt đầu tháng 11". Cùng ngày, tiến sĩ Robert Redfield, giám đốc CDC, đã gửi một lá thư ngỏ cho các thống đốc, yêu cầu họ chuẩn bị địa điểm phân phối trước 1/11.
Kế hoạch chấp thuận khẩn cấp khiến nhiều người e ngại rằng chính quyền Tổng thống Donald Trump đang tìm cách gấp rút phân phối vaccine trước ngày bầu cử 3/11.
Đối với một quốc gia đang phải vật lộn với những thách thức hậu Covid-19, nguồn lực y tế bị phân tán, thiếu sót, việc cung cấp hàng triệu liều tiêm là thách thức lớn, đặc biệt khi chúng cần được bảo quản ở nhiệt độ chuẩn. Ngay cả hướng dẫn của CDC cũng thừa nhận kịch bản này chỉ là giả định, dựa trên những điều kiện cần.
Tiến sĩ Anthony Fauci phát biểu trong buổi họp Quốc hội Mỹ hồi tháng 6/2020. Ảnh: NY Times
"Viễn cảnh về vaccine Covid-19 chưa chắc chắn và còn tiếp tục phát triển, và nó có thể thay đổi khi có nhiều thông tin hơn", người phát ngôn của CDC nói.
Các chuyên gia lo ngại quá trình này khó có thể diễn ra mà không gặp phải bất cứ trở ngại nào, do sự cạnh tranh vào phút cuối.
Tiến sĩ Cedric Dark nhận định: "Khung thời gian được đặt ra có vẻ hơi tham vọng. Chỉ còn 30 ngày nữa là đến tháng 10".
Giai đoạn thử nghiệm lâm sàng có thể kéo dài nhiều năm nếu muốn cho ra kết quả đáng tin cậy. Padmini Pillai, chuyên gia nghiên cứu vaccine và miễn dịch học tại Viện Công nghệ Massachusetts, cho rằng chỉ nên kết luận sớm nếu sản phẩm đạt hiệu quả rất lớn, người đã tiêm chủng được bảo vệ hoàn toàn khỏi bệnh tật.
Rủi ro đáng kể có thể bộc lộ trong thử nghiệm pha ba, khi vaccine được dùng cho hàng chục nghìn người. Lúc này, tác dụng phụ hiếm gặp nhưng nguy hiểm sẽ dần xuất hiện. Các nhà nghiên cứu cũng cần thời gian để kiểm tra trên công dân từ nhiều quốc gia, đánh giá xem sản phẩm có hoạt động trên các cộng đồng, chủng tộc khác nhau hay không.
Tài liệu của CDC lưu ý giới chức y tế công cộng nên xem xét lại bài học kinh nghiệm từ chiến dịch tiêm chủng trong đại dịch H1N1 năm 2009. Khi ấy ,lượng vaccine ngay từ đầu đã không đủ để đáp ứng nhu cầu quốc gia.
Covid-19 có thể không biến mất dù có vaccine  Chuyên gia nghiên cứu vaccine tại Đại học Texas Medical Branch cho rằng mối nguy hiểm từ Covid-19 có thể giảm bớt do miễn dịch cộng đồng, song khó biến mất hoàn toàn. Ông Vineet Menachery, một nhà nghiên cứu về nCoV tại Đại học Texas Medical Branch chia sẻ với NPR's Weekend Edition về viễn cảnh thế giới trong tương lai do...
Chuyên gia nghiên cứu vaccine tại Đại học Texas Medical Branch cho rằng mối nguy hiểm từ Covid-19 có thể giảm bớt do miễn dịch cộng đồng, song khó biến mất hoàn toàn. Ông Vineet Menachery, một nhà nghiên cứu về nCoV tại Đại học Texas Medical Branch chia sẻ với NPR's Weekend Edition về viễn cảnh thế giới trong tương lai do...
 Ý tưởng gây sốc của Tổng thống Trump về Dải Gaza08:59
Ý tưởng gây sốc của Tổng thống Trump về Dải Gaza08:59 Iran công bố tên lửa đạn đạo mới nhất08:23
Iran công bố tên lửa đạn đạo mới nhất08:23 Phản ứng dữ dội sau đề xuất chấn động của ông Trump về Gaza08:43
Phản ứng dữ dội sau đề xuất chấn động của ông Trump về Gaza08:43 Ông Trump rút Mỹ khỏi cơ quan trực thuộc Liên Hiệp Quốc08:04
Ông Trump rút Mỹ khỏi cơ quan trực thuộc Liên Hiệp Quốc08:04 Ông Trump cấm người chuyển giới tham gia các môn thể thao dành cho nữ08:45
Ông Trump cấm người chuyển giới tham gia các môn thể thao dành cho nữ08:45 Nga sắp cho chạy thử 'chiến hạm mạnh nhất thế giới' sau cuộc đại tu?10:04
Nga sắp cho chạy thử 'chiến hạm mạnh nhất thế giới' sau cuộc đại tu?10:04 Triều Tiên lần đầu chỉ trích chính quyền Tổng thống Trump08:06
Triều Tiên lần đầu chỉ trích chính quyền Tổng thống Trump08:06 Rộ tin ông Putin muốn gặp ông Trump ở UAE hoặc Ả Rập Xê Út10:29
Rộ tin ông Putin muốn gặp ông Trump ở UAE hoặc Ả Rập Xê Út10:29 Mỹ chuẩn bị kế hoạch rút quân khỏi Syria?02:37
Mỹ chuẩn bị kế hoạch rút quân khỏi Syria?02:37 Ông Trump được tặng máy nhắn tin bằng vàng, ca ngợi 'chiến dịch tuyệt vời' của Israel08:58
Ông Trump được tặng máy nhắn tin bằng vàng, ca ngợi 'chiến dịch tuyệt vời' của Israel08:58 Iran trình làng tàu chiến chở UAV đầu tiên01:05
Iran trình làng tàu chiến chở UAV đầu tiên01:05Tiêu điểm
Tin đang nóng
Tin mới nhất

Châu Âu nhóm họp sau bài phát biểu gây "sốc" của Phó Tổng thống Mỹ

Mỹ sẽ tái tập trung ưu tiên quân sự để đối phó Trung Quốc?
Mùa cúm dữ dội và bất thường ở Mỹ

Trung Quốc tuyên bố "chơi đến cùng" với Mỹ

Sau nhôm thép, ông Trump sắp áp thuế với ô tô

Giải pháp của Ấn Độ trước sức ép năng lượng từ Nga và Mỹ
Ngoại trưởng Ba Lan bình luận về chiến thuật đàm phán của Mỹ liên quan Ukraine

Hezbollah yêu cầu chính phủ Liban dỡ bỏ lệnh cấm đối với máy bay Iran

Israel và Mỹ khẳng định có cách tiếp cận chung trong vấn đề Gaza

Tổng thống Phần Lan tuyên bố cứng rắn về Nga trước đàm phán về xung đột Ukraine

Phần Lan nêu quan điểm về các cuộc đàm phán Mỹ - Nga

Ukraine trải qua ngày khốc liệt nhất trên chiến trường kể từ đầu năm 2025
Có thể bạn quan tâm

Còn gần tuần nữa mới ra mắt, bom tấn tháng 2 bất ngờ tung demo miễn phí, game thủ thoải mái trải nghiệm
Mọt game
06:53:20 17/02/2025
Omega-3 có nhiều nhất trong thực phẩm nào?
Sức khỏe
06:19:52 17/02/2025
Cuộc chiến tài sản của Từ Hy Viên: Còn 2 nhân vật bí ẩn, quyền lực đang ở đâu?
Sao châu á
06:16:59 17/02/2025
Sao nữ Vbiz từng vướng tin hẹn hò đồng giới nay công khai video tình tứ bên người mới
Sao việt
06:10:10 17/02/2025
Vào mùa xuân nên ăn nhiều 3 loại rau mầm này, vừa mát gan giải nhiệt lại tăng sức đề kháng khi thời tiết thay đổi
Ẩm thực
06:07:14 17/02/2025
'Trung tâm chăm sóc chấn thương' ăn khách, bộ ba diễn viên chính được săn đón
Hậu trường phim
06:02:56 17/02/2025
Học trò Đàm Vĩnh Hưng gây tiếc nuối ở 'Giọng hát Việt' ra sao sau 10 năm?
Nhạc việt
06:00:40 17/02/2025
Phim Việt gây chấn động vì cảnh 2 đại mỹ nhân vạch mặt nhau căng thẳng như Diên Hi Công Lược
Phim việt
05:59:39 17/02/2025
Phim Hoa ngữ cực hay nhưng bị nhà đài chê thẳng mặt: Cặp chính đẹp như tiên đồng ngọc nữ cũng "hết cứu"?
Phim châu á
05:59:04 17/02/2025
(Review): 'The Gorge': Phim tình cảm 'sến' và dữ dội của Anya Taylor-Joy
Phim âu mỹ
05:58:23 17/02/2025
 Hy Lạp mua loạt vũ khí giữa căng thẳng với Thổ Nhĩ Kỳ
Hy Lạp mua loạt vũ khí giữa căng thẳng với Thổ Nhĩ Kỳ Vaccine Covid-19 Oxford nối lại thử nghiệm
Vaccine Covid-19 Oxford nối lại thử nghiệm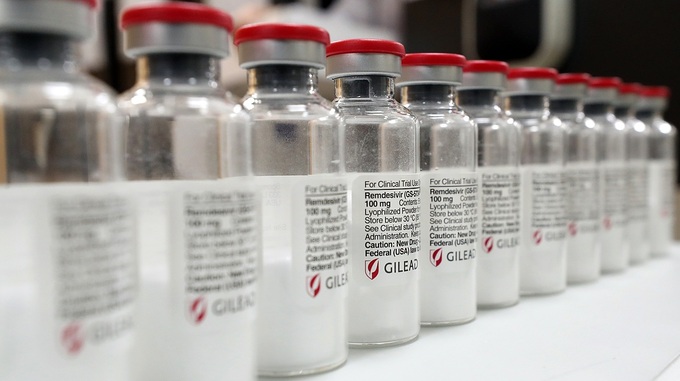

 Trung Quốc tố Mỹ 'vu khống hiểm độc'
Trung Quốc tố Mỹ 'vu khống hiểm độc' Cảnh người dân thế giới sống chung với COVID-19
Cảnh người dân thế giới sống chung với COVID-19
 Mỹ điều tra mối liên hệ Covid-19 giữa Đại học Texas với Trung Quốc
Mỹ điều tra mối liên hệ Covid-19 giữa Đại học Texas với Trung Quốc Các nhà du hành vũ trụ đang gặp nguy hiểm trong không gian
Các nhà du hành vũ trụ đang gặp nguy hiểm trong không gian Kinh tế tơi tả, châu Âu rụt rè 'mở cửa lại'
Kinh tế tơi tả, châu Âu rụt rè 'mở cửa lại' Nhìn lại quan điểm của Tổng thống Trump trong đàm phán với Nga về hòa bình Ukraine
Nhìn lại quan điểm của Tổng thống Trump trong đàm phán với Nga về hòa bình Ukraine Tổng thống Ukraine tiết lộ quan chức Nga duy nhất ông muốn đàm phán
Tổng thống Ukraine tiết lộ quan chức Nga duy nhất ông muốn đàm phán Ukraine muốn có đội quân 1,5 triệu người nếu không được vào NATO
Ukraine muốn có đội quân 1,5 triệu người nếu không được vào NATO Nga đáp trả "tối hậu thư" của Mỹ về Ukraine
Nga đáp trả "tối hậu thư" của Mỹ về Ukraine Nỗi lo của Ukraine và châu Âu từ cuộc điện đàm giữa nguyên thủ hai nước Nga - Mỹ
Nỗi lo của Ukraine và châu Âu từ cuộc điện đàm giữa nguyên thủ hai nước Nga - Mỹ Ukraine đề xuất để châu Âu tiếp cận "kho báu" nghìn tỷ USD
Ukraine đề xuất để châu Âu tiếp cận "kho báu" nghìn tỷ USD Hungary cảnh báo Ukraine trở thành Afghanistan với châu Âu
Hungary cảnh báo Ukraine trở thành Afghanistan với châu Âu Bước ngoặt bất ngờ trong lập trường của Mỹ về Ukraine
Bước ngoặt bất ngờ trong lập trường của Mỹ về Ukraine Vụ Kim Sae Ron qua đời ở nhà riêng: Được phát hiện trong tình trạng bất tỉnh ngừng tim, không còn khả năng cứu chữa khi vào bệnh viện
Vụ Kim Sae Ron qua đời ở nhà riêng: Được phát hiện trong tình trạng bất tỉnh ngừng tim, không còn khả năng cứu chữa khi vào bệnh viện Vì sao dân mạng sốc khi Kim Sae Ron qua đời ngay đúng ngày sinh nhật của Kim Soo Hyun?
Vì sao dân mạng sốc khi Kim Sae Ron qua đời ngay đúng ngày sinh nhật của Kim Soo Hyun? Con gái nuôi Phi Nhung kết hôn
Con gái nuôi Phi Nhung kết hôn Kim Sae Ron sống cô độc, liên tục vào viện điều trị 1 vấn đề ngay trước khi qua đời
Kim Sae Ron sống cô độc, liên tục vào viện điều trị 1 vấn đề ngay trước khi qua đời Sao nam Vbiz và vợ kém 17 tuổi có con thứ 2?
Sao nam Vbiz và vợ kém 17 tuổi có con thứ 2? Ca sĩ Hoài Lâm livestream bán hàng, nghệ sĩ Trường Giang lạ lẫm
Ca sĩ Hoài Lâm livestream bán hàng, nghệ sĩ Trường Giang lạ lẫm Bộ phim đỉnh nhất của Kim Sae Ron: Diễn xuất xứng đáng phong thần, làm nên điều không tưởng ở Cannes
Bộ phim đỉnh nhất của Kim Sae Ron: Diễn xuất xứng đáng phong thần, làm nên điều không tưởng ở Cannes Mâu thuẫn tiền bạc, anh rể cưa phá hàng trăm gốc cây trong vườn nhà em dâu
Mâu thuẫn tiền bạc, anh rể cưa phá hàng trăm gốc cây trong vườn nhà em dâu Lễ tiễn biệt Từ Hy Viên: Gia đình ca hát vui vẻ, chồng Hàn gầy rộc sút hơn 7 kg sau biến cố
Lễ tiễn biệt Từ Hy Viên: Gia đình ca hát vui vẻ, chồng Hàn gầy rộc sút hơn 7 kg sau biến cố Cú "ngã ngựa" cay đắng của mỹ nữ 1m5 đình đám nhất Vbiz
Cú "ngã ngựa" cay đắng của mỹ nữ 1m5 đình đám nhất Vbiz Người mẫu Xuân Mai đột ngột qua đời ở tuổi 29
Người mẫu Xuân Mai đột ngột qua đời ở tuổi 29 Tình cũ Thiều Bảo Trâm muốn yên lặng nhưng sao Hoa hậu Lê Hoàng Phương vẫn không ngừng úp mở?
Tình cũ Thiều Bảo Trâm muốn yên lặng nhưng sao Hoa hậu Lê Hoàng Phương vẫn không ngừng úp mở? Sự thật về thông tin trâu chọi ở Vĩnh Phúc bị chích điện đến chết giữa sân đấu
Sự thật về thông tin trâu chọi ở Vĩnh Phúc bị chích điện đến chết giữa sân đấu Sao nữ Vbiz nhiễm cúm B với 1 triệu chứng nặng, sững người khi bác sĩ nói tình trạng bệnh
Sao nữ Vbiz nhiễm cúm B với 1 triệu chứng nặng, sững người khi bác sĩ nói tình trạng bệnh Tậu xe sang 7 tỷ ở tuổi 19, Lọ Lem kiếm tiền từ đâu?
Tậu xe sang 7 tỷ ở tuổi 19, Lọ Lem kiếm tiền từ đâu? Nữ sinh "điên cuồng" ra rạp xem Na Tra 31 lần trong 8 ngày bị chê phung phí, người cha tiết lộ nguyên nhân đau lòng phía sau
Nữ sinh "điên cuồng" ra rạp xem Na Tra 31 lần trong 8 ngày bị chê phung phí, người cha tiết lộ nguyên nhân đau lòng phía sau
 Cô giáo mang thai bất ngờ bị nhóm phụ huynh tố cáo lên hiệu trưởng, lý do được tiết lộ khiến netizen bức xúc: Không thể hiểu nổi!
Cô giáo mang thai bất ngờ bị nhóm phụ huynh tố cáo lên hiệu trưởng, lý do được tiết lộ khiến netizen bức xúc: Không thể hiểu nổi!