WHO: Biến thể mới XE có thể là phiên bản dễ lây lan nhất của virus SARS-CoV-2
Tổ chức Y tế Thế giới (WHO) mới đây đưa ra một báo cáo trong đó có một số phát hiện sơ bộ về biến thể mới gọi là XE.
Khả năng lây lan của XE sẽ cao hơn tới 43% so với Omicron
“Tái tổ hợp XE lần đầu tiên được phát hiện ở Vương quốc Anh vào ngày 19/1 và hơn 600 trình tự chuỗi gene XE đã được báo cáo và xác nhận kể từ đó. Các ước tính ban đầu cho thấy tốc độ tăng trưởng lây nhiễm trong cộng đồng của XE là lớn hơn khoảng 10% so với BA.2, tuy nhiên, phát hiện này cần được xác nhận thêm” – tài liệu của WHO cho biết.
Được biết, trong thời gian qua, giới khoa học đã theo dõi 3 biến thể mới gồm XD, XF và XE. Trong đó, 2 biến thể XD và XF là những dạng kết hợp của biến thể Delta và BA.1, hay gọi là Deltacron. Hai biến thể này đã đươc nhắc tới từ vài tháng nay nhưng chưa thực sự gây ra những thay đổi đáng kể trong diễn biến dịch bệnh thế giới.
Còn lại, biến thể XE là một dạng biến thể tái tổ hợp – kết hợp của chính các biến thể BA.1 và BA.2 của Omicron. Biến thể tái tổ hợp xuất hiện khi một người nhiễm cùng lúc 2 hoặc 3 biến thể của virus, tạo điều kiện cho các vật chất di truyền của các biến thể pha trộn trong cơ thể người bệnh. Đây không phải điều bất thường vì đã từng xảy ra một số lần trong thời gian đại dịch COVID-19 hoành hành.
Theo WHO, việc xác nhận thêm về biến thể XE đang ngày càng trở nên khó khăn hơn trong tuần này bởi cái gọi là “sự giảm đáng kể” gần đây về việc thực hiện xét nghiệm SARS-CoV-2 tại nhiều quốc gia. “Điều này ngăn cản chúng tôi trong việc theo dõi virus đang ở đâu, lây lan như thế nào và tiến triển ra sao. Đó vốn là những thông tin và phân tích rất quan trọng để biết được đâu là thời điểm chấm dứt giai đoạn cấp tính của đại dịch” – WHO cho biết.
Hồi tuần trước, Cơ quan An ninh y tế Anh (UKHSA) cũng đã trình báo cáo vắn tắt cho WHO trong đó có một số nội dung liên quan biến thể XE.Theo UKHSA, có bằng chứng cho thấy biến thể XE lây lan trong cộng đồng ở vùng England dù mới chỉ ở mức 1% tổng số mẫu được đưa đi phân tích. Những dữ liệu ban đầu về tỷ lệ tăng trưởng số ca mắc do nhiễm XE không cho thấy sự khác biệt đáng kể với BA.2.
Tuy nhiên, dựa trên các dữ liệu mới nhất tính đến ngày 16/3 thì tốc độ tăng trưởng số ca mắc do nhiễm biến thể này có thể cao hơn 9,8% so với BA.2.
Giáo sư Susan Hopkins, Cố vấn y khoa chính tại UKHSA cho biết XE là một biến thể tái tổ hợp đặc biệt, có tốc độ tăng trưởng lây nhiễm không giống các biến thể trước và cần thêm thời gian để xác định cụ thể các đặc tính của biến thể này. UKHSA vẫn đang tiếp tục theo dõi tình hình.
Hiện XE vẫn chiếm phần rất nhỏ trong tổng số ca mắc bệnh trên toàn thế giới nhưng nếu thực sự tốc độ tăng trưởng số ca mắc do nhiễm biến thể này cao hơn 10% so với BA.2 thì khả năng lây lan của XE sẽ cao hơn tới 43% so với Omicron, biến thể hoành hành trên toàn thế giới trong những tháng vừa qua.
Dù vậy, những lo ngại rằng BA.2, biến thể chủ đạo hiện nay, có thể gây ra những làn sóng lây nhiễm mới vẫn chưa có dấu hiệu trở thành hiện thực kể cả khi nhiều nước đã dỡ bỏ các biện pháp hạn chế. Giới khoa học hy vọng xu hướng dịch bệnh do XE gây ra cũng sẽ diễn biến tương tự như các biến thể khác trước đó.
WHO không chấp nhận kit test của Công ty Việt Á: Bộ Y tế nói gì?
Theo một thông báo của Tổ chức Y tế thế giới ( WHO) vào tháng 10.2020, bộ kit test Covid-19 đầu tiên của Việt Nam do Công ty CP công nghệ Việt Á sản xuất không được WHO công nhận.
Không đạt tiêu chuẩn của WHO
Cụ thể, thông báo công khai của WHO như sau: sản phẩm LightPower iVA SARS-CoV-2 Bộ RT-PCR có mã số EUL 0524-210-00 không được chấp nhận. Đây là sản phẩm của Công ty CP công nghệ Việt Á (VietACorp), có địa chỉ tại số 372A/8 Hồ Văn Huê, P.9, Q.Phú Nhuận, TP.HCM.
"Sản phẩm do Việt Nam sản xuất, không đủ điều kiện để mua sắm của WHO", WHO nêu rõ.
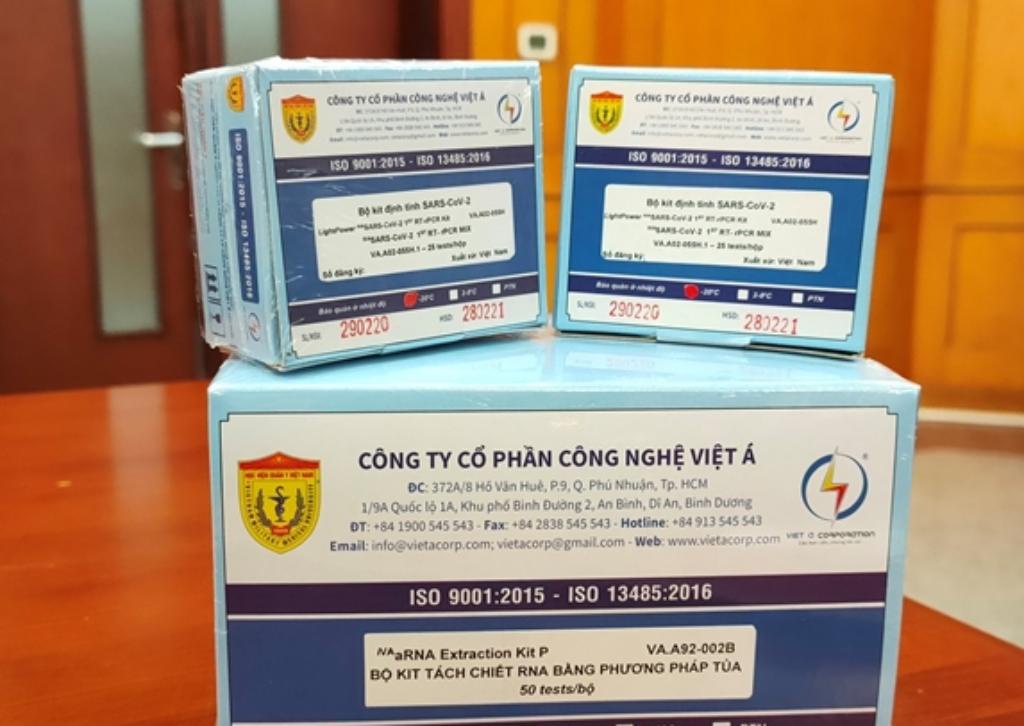
Sản phẩm kit test của Công ty CP công nghệ Việt Á. Ảnh T.S
Nguyên nhân, theo WHO, VietACorp được yêu cầu cung cấp thông tin cập nhật về tình trạng của hệ thống quản lý chất lượng. Sau khi xem xét tài liệu được đệ trình, WHO hỗ trợ đánh giá về Hệ thống quản lý chất lượng của nhà sản xuất. Kết quả, thông tin được cung cấp không phải là bằng chứng đầy đủ về việc tuân thủ tiêu chuẩn ISO 13485:2016.
ISO 13458:2016 là tiêu chuẩn đã được chấp nhận và được áp dụng rộng rãi cho các nhà sản xuất thiết bị y tế trên toàn thế giới, và là một yêu cầu cần phải có nếu như một tổ chức sản xuất thiết bị y tế muốn sản phẩm của mình được công nhận rộng rãi trên thế giới. Phiên bản ISO 13458:2016 của WHO là "Hướng dẫn về Yêu cầu nộp hồ sơ: Chẩn đoán trong ống nghiệm (IVD) Phát hiện Axit nucleic SARS-CoV-2, PQDx_ 347".
Thông báo của WHO về việc sản phẩm LightPower iVA SARS-CoV-2 Bộ RT-PCR có mã số EUL 0524-210-00 của Công ty CP công nghệ Việt Á không được chấp nhận. Ảnh WHO
Về quy trình EUL (đánh giá sử dụng khẩn cấp) trong thông báo ở trên, WHO đưa ra nhằm thúc đẩy sự sẵn có của các thiết bị y tế in vitro (trong ống nghiệm) cần cho các tình huống khẩn cấp về sức khỏe, để hỗ trợ thông tin cho các cơ quan mua sắm và các nước thành viên Liên Hiệp Quốc.
Trang thiết bị y tế chẩn đoán in vitro gồm thuốc thử, chất hiệu chuẩn, vật liệu kiểm soát, dụng cụ, máy, thiết bị hoặc hệ thống được sử dụng riêng rẽ hoặc kết hợp theo chỉ định của chủ sở hữu để phục vụ cho việc kiểm tra các mẫu vật có nguồn gốc từ cơ thể người.
Trên cơ sở đánh giá sử dụng khẩn cấp, các quốc gia có thể quyết định phê duyệt, sử dụng các sản phẩm cụ thể đã được chấp thuận trong bối cảnh khẩn cấp về y tế, dựa trên dữ liệu về chất lượng, an toàn và hiệu quả đã được thẩm định.
Lãnh đạo HCDC khẳng định không mua kit test Covid-19 của Công ty Việt Á vì giá cao Bộ Y tế nói gì?
Về việc WHO không chấp nhận kit của VietACorp, thông tin từ Bộ Y tế chiều nay 20.12, cho biết: "WHO đưa ra danh sách EUL về một số sản phẩm để các đơn vị của WHO tham khảo và mua sắm khẩn cấp phục vụ phòng chống dịch, chứ không liên quan đến chất lượng hay tiêu chuẩn cấp phép".
Theo Bộ Y tế, sản xuất trang thiết bị y tế trong nước, bao gồm kit test chẩn đoán từ ngày 1.1.2020, phải đạt tiêu chuẩn ISO 13485. Theo đó, VietACorp đã đạt tiêu chuẩn này khi sản xuất kit test xét nghiệm Covid-19.
Như vậy, có thể thấy, sản phẩm kit test của Công ty CP công nghệ Việt Á đạt tiêu chuẩn trong nước nhưng không đạt tiêu chuẩn và được WHO chấp nhận. Trong khi đó, liên quan đến sản phẩm kit test này, vào thời điểm tháng 4.2020, có rất nhiều thông tin từ các cơ quan chức năng khẳng định WHO chấp thuận được sử dụng rộng rãi. Trong đó, trang web của Bộ KH-CN nhiều lần đưa tin WHO đã chấp nhận, tuy nhiên đến nay tất cả đã không còn truy cập được.
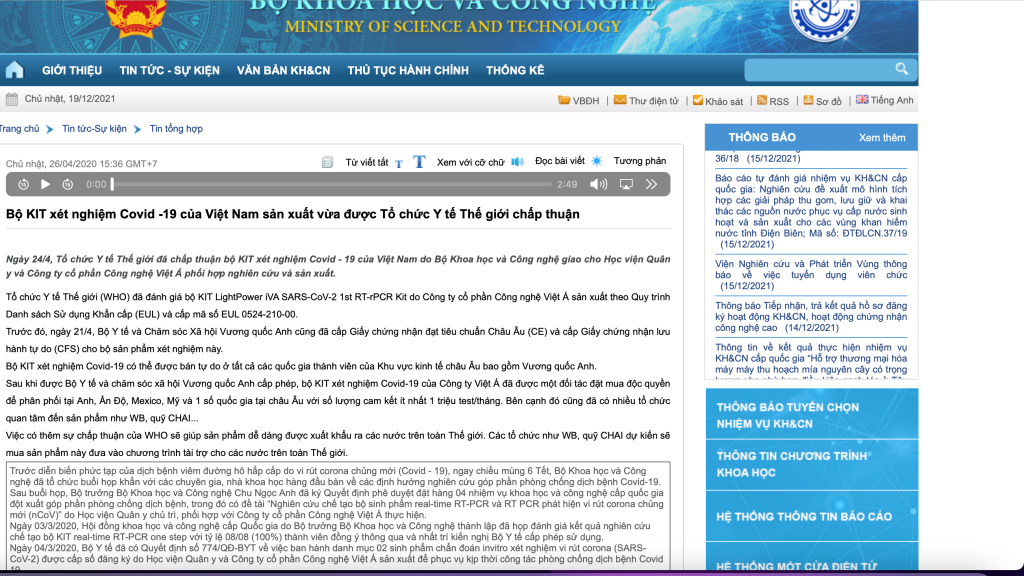
Bản lưu tin WHO chấp nhận kit test của VietACorp vẫn còn trên trang tìm kiếm của Google nhưng link gốc bị gỡ. Ảnh CHỤP MÀN HÌNH
Trước đó, ông Phan Quốc Việt (41 tuổi), Tổng giám đốc VietACorp, cùng nhiều thuộc cấp đã bị Bộ Công an khởi tố, điều tra về hành vi "thổi giá" kit xét nghiệm Covid-19.
VietACorp quảng cáo đây là bộ kit chẩn đoán SARS-CoV-2 đầu tiên tại Việt Nam, được Bộ Y tế cấp số đăng ký; Bộ Y tế và Chăm sóc xã hội Anh cấp giấy chứng nhận đạt tiêu chuẩn châu Âu (CE), cấp giấy chứng nhận lưu hành tự do (CFS); WHO cấp chứng nhận chất lượng sản phẩm cho phép lưu hành toàn cầu.
Cũng theo quảng bá, năng lực sản xuất của Công ty CP công nghệ Việt Á khoảng 30.000 kit xét nghiệm/ngày. Bộ kit xét nghiệm này cho kết quả chính xác 100% sau 2 giờ và đáp ứng được các tiêu chí tương đương các bộ sinh phẩm do CDC Mỹ và WHO hướng dẫn.
Bản tin Covid-19 ngày 20.12: Cả nước 14.977 ca | "Nóng" sau vụ bê bối thổi giá kit test của Công ty Việt Á
Dịch COVID-19: TP HCM cần tăng cường điều tra dịch tễ nơi nguy cơ cao, lưu ý sự xuất hiện các biến thể mới  Phó Thủ tướng Chính phủ Vũ Đức Đam nhấn mạnh: Ngành y tế TP HCM cần tăng cường xét nghiệm điều tra dịch tễ cộng đồng ở những nơi nguy cơ cao như các chợ truyền thống, trung tâm thương mại, trong đó lưu ý sự xuất hiện các biến thể mới của SARS-CoV-2. Phó Thủ tướng Vũ Đức Đam, Tổ công tác...
Phó Thủ tướng Chính phủ Vũ Đức Đam nhấn mạnh: Ngành y tế TP HCM cần tăng cường xét nghiệm điều tra dịch tễ cộng đồng ở những nơi nguy cơ cao như các chợ truyền thống, trung tâm thương mại, trong đó lưu ý sự xuất hiện các biến thể mới của SARS-CoV-2. Phó Thủ tướng Vũ Đức Đam, Tổ công tác...
 Quán bún Hà Nội xin lỗi vụ bán 1,2 triệu đồng 3 bát bún riêu ngày Tết, nói chỉ là 'hiểu lầm'09:39
Quán bún Hà Nội xin lỗi vụ bán 1,2 triệu đồng 3 bát bún riêu ngày Tết, nói chỉ là 'hiểu lầm'09:39 Củng cố hồ sơ để xử lý TikToker có nồng độ cồn, livestream khi bị cảnh sát giao thông kiểm tra01:03
Củng cố hồ sơ để xử lý TikToker có nồng độ cồn, livestream khi bị cảnh sát giao thông kiểm tra01:03 Vụ xe ôtô lao xuống mương 7 người tử vong: Công an công bố nguyên nhân ban đầu14:39
Vụ xe ôtô lao xuống mương 7 người tử vong: Công an công bố nguyên nhân ban đầu14:39 11 'quái xế' chạy vào cao tốc Nghi Sơn - Diễn Châu bị phạt 78 triệu đồng501:27
11 'quái xế' chạy vào cao tốc Nghi Sơn - Diễn Châu bị phạt 78 triệu đồng501:27 CSGT hú còi mở đường cho xe chở người bị điện giật nguy kịch đi cấp cứu01:10
CSGT hú còi mở đường cho xe chở người bị điện giật nguy kịch đi cấp cứu01:10 Thông tin về ô tô 'tự di chuyển' ở sân bay Tân Sơn Nhất09:00
Thông tin về ô tô 'tự di chuyển' ở sân bay Tân Sơn Nhất09:00 Cảnh sát Liên Hiệp Quốc bổ nhiệm sĩ quan công an Việt Nam làm chánh văn phòng cố vấn09:41
Cảnh sát Liên Hiệp Quốc bổ nhiệm sĩ quan công an Việt Nam làm chánh văn phòng cố vấn09:41 Xe tải bốc cháy trên đường giữa trưa08:24
Xe tải bốc cháy trên đường giữa trưa08:24 Mới sinh con 3 tháng, người mẹ trẻ không có đối thủ trên sới vật02:34
Mới sinh con 3 tháng, người mẹ trẻ không có đối thủ trên sới vật02:34Tiêu điểm
Tin đang nóng
Tin mới nhất

Người phụ nữ tử vong bất thường tại tầng 2 ở nhà riêng

Sở Y tế Quảng Nam làm rõ nguyên nhân 3 trẻ em tử vong dịp Tết

Tự ý lắp còi hú, đèn nháy ưu tiên sẽ bị phạt tới 6 triệu đồng

Tìm thấy thi thể 3 thanh niên mất tích khi tắm sông ở Bến Tre

Tài xế tử vong trong ô tô khi chờ khách ở Ba Vì

Chi tiết 12 tuyến metro của TPHCM, sẽ kết nối đến Cần Giờ và Củ Chi

Mùng 1 Tết, nữ cán bộ phường giật mình với cuộc điện thoại lúc nửa đêm

Xe máy va chạm với container, một cô gái trẻ tử vong

Đề xuất tội làm giàu bất chính và "chặn" tham nhũng qua tiền ảo

Cá voi thoi thóp lụy vào bãi biển trước Lăng Ông Nam Hải

Xử phạt người bán nhang ở Nha Trang xô xát với khách Trung Quốc

Tài xế ô tô dừng xe, trải chiếu cho gia đình ăn cơm trên đường cao tốc
Có thể bạn quan tâm

Hải Tú thông báo 2 việc sau Tết, cái nào cũng gây bất ngờ
Netizen
23:10:28 04/02/2025
Cặp đôi "phim giả tình thật" hot nhất lúc này: Nhà gái là Hoa hậu, nhà trai lộ rõ vẻ si mê khó chối cãi
Hậu trường phim
22:58:43 04/02/2025
Cuộc đời Từ Hy Viên từng mong cưới một mỹ nam: Tiết lộ bất ngờ từ em gái Từ Hy Đệ
Sao châu á
22:45:57 04/02/2025
Phim Hoa ngữ thất bại thảm hại nhất hiện tại: Lỗ nặng 3.500 tỷ, kịch bản ngớ ngẩn coi thường khán giả
Phim châu á
22:40:32 04/02/2025
Đề nghị truy tố cựu Thứ trưởng Bộ Tài nguyên và Môi trường
Pháp luật
22:35:29 04/02/2025
Cựu thủ lĩnh đối lập Syria trở thành tổng thống lâm thời, nêu 4 ưu tiên
Thế giới
22:28:04 04/02/2025
Doãn Hải My đẹp rạng rỡ, mặt mộc Mai Phương Thúy 'bất bại'
Sao việt
22:26:07 04/02/2025
Xôn xao giá vé fanmeeting của thành viên đẹp nhất BLACKPINK tại Hà Nội, dự đoán một cuộc "đại chiến" khốc liệt!
Nhạc quốc tế
22:23:29 04/02/2025
Bằng chứng cho thấy người Việt Nam cực kỳ thích hát karaoke, đến Jennie và các "anh trai" cũng phải chào thua
Nhạc việt
22:20:57 04/02/2025
Phim của đạo diễn Việt 'gây sốt' trên Netflix
Phim việt
22:01:59 04/02/2025
 Ngày 1/4: Số mắc mới COVID-19 giảm sâu, còn 72.556 ca; Vĩnh Phúc bổ sung hơn 13.000 F0
Ngày 1/4: Số mắc mới COVID-19 giảm sâu, còn 72.556 ca; Vĩnh Phúc bổ sung hơn 13.000 F0 NÓNG: Tạm giữ cô gái phóng hỏa nhà trọ 7 tầng khiến 6 người thương vong ở Hà Nội
NÓNG: Tạm giữ cô gái phóng hỏa nhà trọ 7 tầng khiến 6 người thương vong ở Hà Nội

 Vụ tử vong vì không được cấp cứu: Định danh vi phạm của 6 cơ sở y tế
Vụ tử vong vì không được cấp cứu: Định danh vi phạm của 6 cơ sở y tế Tổ chức Y tế thế giới (WHO) nói gì về bộ xét nghiệm PCR do Công ty Việt Á sản xuất?
Tổ chức Y tế thế giới (WHO) nói gì về bộ xét nghiệm PCR do Công ty Việt Á sản xuất?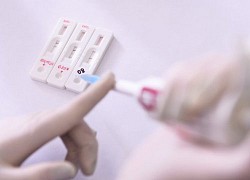 WHO không phê duyệt bộ xét nghiệm của Việt Á
WHO không phê duyệt bộ xét nghiệm của Việt Á Chủ động mua sắm thiết bị xét nghiệm, vật tư y tế phòng, chống dịch COVID-19
Chủ động mua sắm thiết bị xét nghiệm, vật tư y tế phòng, chống dịch COVID-19 Quảng Ninh ra thông báo khẩn tìm người đi xe Limousin từ TX Đông Triều đến Móng Cái
Quảng Ninh ra thông báo khẩn tìm người đi xe Limousin từ TX Đông Triều đến Móng Cái Sóc Trăng: Xây dựng 849 căn nhà cho hộ nghèo khó khăn về nhà ở
Sóc Trăng: Xây dựng 849 căn nhà cho hộ nghèo khó khăn về nhà ở Vụ thanh niên mất tích bí ẩn khi đi chùa Đại Tuệ: Tìm thấy thi thể
Vụ thanh niên mất tích bí ẩn khi đi chùa Đại Tuệ: Tìm thấy thi thể Cả gia đình bị tai nạn giao thông trên cao tốc ở Thanh Hóa, 2 con tử vong
Cả gia đình bị tai nạn giao thông trên cao tốc ở Thanh Hóa, 2 con tử vong 3 thanh niên ở Bến Tre bất ngờ mất tích khi bị hút vào cống dẫn nước
3 thanh niên ở Bến Tre bất ngờ mất tích khi bị hút vào cống dẫn nước Người đàn ông bỏ lại xe máy ở khu vực chùa Đại Tuệ rồi mất tích
Người đàn ông bỏ lại xe máy ở khu vực chùa Đại Tuệ rồi mất tích Công an tiết lộ tin nóng vụ ô tô lao xuống mương khiến 7 người tử vong, đã có kết quả nồng độ cồn
Công an tiết lộ tin nóng vụ ô tô lao xuống mương khiến 7 người tử vong, đã có kết quả nồng độ cồn Cháy nhà trọ 6 tầng ở Cầu Giấy, cảnh sát giải cứu được 7 người
Cháy nhà trọ 6 tầng ở Cầu Giấy, cảnh sát giải cứu được 7 người Tài xế dính phạt nguội, CSGT xóa lỗi vì hành động 'đúng và đẹp'
Tài xế dính phạt nguội, CSGT xóa lỗi vì hành động 'đúng và đẹp' Tài xế ô tô chờ 7 tiếng chưa qua được phà Cát Lái tối mùng 5 Tết
Tài xế ô tô chờ 7 tiếng chưa qua được phà Cát Lái tối mùng 5 Tết Thắt lòng tin nhắn cuối cùng của Từ Hy Viên với bạn thân trước khi đột ngột qua đời
Thắt lòng tin nhắn cuối cùng của Từ Hy Viên với bạn thân trước khi đột ngột qua đời CĂNG: 1 sao nam Vbiz bị đạo diễn tố tác động vật lý con gái anh trong hậu trường, cho thời hạn 3 ngày để chờ giải quyết
CĂNG: 1 sao nam Vbiz bị đạo diễn tố tác động vật lý con gái anh trong hậu trường, cho thời hạn 3 ngày để chờ giải quyết Lan truyền kết quả khám nghiệm tử thi Từ Hy Viên, nữ diễn viên liều mạng sống chỉ vì 1 lí do?
Lan truyền kết quả khám nghiệm tử thi Từ Hy Viên, nữ diễn viên liều mạng sống chỉ vì 1 lí do?
 2 tờ vé số trúng độc đắc 4 tỷ đồng nhưng bị rách nát, hé lộ thông tin gây tiếc nuối về chủ nhân
2 tờ vé số trúng độc đắc 4 tỷ đồng nhưng bị rách nát, hé lộ thông tin gây tiếc nuối về chủ nhân Kwon Sang Woo sững sờ nhận kết quả chụp phổi trắng xóa: "Tôi sắp chết rồi sao?"
Kwon Sang Woo sững sờ nhận kết quả chụp phổi trắng xóa: "Tôi sắp chết rồi sao?" Từ Hy Viên nói gì về cái chết?
Từ Hy Viên nói gì về cái chết? Tình cũ Châu Du Dân đau đớn, đăng đến 20 ảnh tưởng nhớ Từ Hy Viên?
Tình cũ Châu Du Dân đau đớn, đăng đến 20 ảnh tưởng nhớ Từ Hy Viên? Tang thương bao trùm Cbiz: Thêm nam diễn viên đột ngột qua đời ở tuổi 27
Tang thương bao trùm Cbiz: Thêm nam diễn viên đột ngột qua đời ở tuổi 27 Thi hài Từ Hy Viên được hỏa táng ở Nhật, di ngôn hé lộ tâm nguyện sau lần thập tử nhất sinh 9 năm trước
Thi hài Từ Hy Viên được hỏa táng ở Nhật, di ngôn hé lộ tâm nguyện sau lần thập tử nhất sinh 9 năm trước SỐC: Từ Hy Viên 3 lần cấp cứu vì nguy kịch ở Nhật, tử vong chỉ sau 5 ngày phát bệnh
SỐC: Từ Hy Viên 3 lần cấp cứu vì nguy kịch ở Nhật, tử vong chỉ sau 5 ngày phát bệnh Chấn động: Từ Hy Viên qua đời
Chấn động: Từ Hy Viên qua đời Sốc: Từ Hy Viên không được làm tim phổi nhân tạo trong lúc nguy kịch, nguyên nhân tử vong chính thức được công bố
Sốc: Từ Hy Viên không được làm tim phổi nhân tạo trong lúc nguy kịch, nguyên nhân tử vong chính thức được công bố Nóng: Không tìm thấy chồng Từ Hy Viên
Nóng: Không tìm thấy chồng Từ Hy Viên Rò rỉ thỏa thuận tiền hôn nhân "3 không" của Từ Hy Viên, chồng ca sĩ Hàn sẽ mất quyền thừa kế?
Rò rỉ thỏa thuận tiền hôn nhân "3 không" của Từ Hy Viên, chồng ca sĩ Hàn sẽ mất quyền thừa kế? Từ Hy Viên vừa qua đời: Chồng mới - chồng cũ lao vào cuộc chiến tranh chấp tài sản?
Từ Hy Viên vừa qua đời: Chồng mới - chồng cũ lao vào cuộc chiến tranh chấp tài sản?