Vaccine Covid-19 của Moderna hiệu quả 94,5%
Hãng dược Moderna tuyên bố vaccine Covid-19 của mình hiệu quả 94,5%, dựa trên dữ liệu sơ bộ thử nghiệm giai đoạn cuối.
Tuyên bố đưa ra ngày 16/11, Moderna trở thành nhà sản xuất thứ hai ở Mỹ báo cáo kết quả vaccine vượt xa mong đợi. Như vậy, cùng sản phẩm của Pfizer, Mỹ có hai loại vaccine Covid-19, dự kiến được phê duyệt khẩn cấp tháng 12 năm nay.
“Vaccine của chúng tôi có thể ngăn chặn Covid-19″, Chủ tịch Moderna Stephen Hoge cho biết. Thử nghiệm giai đoạn ba của hãng được tiến hành trên 30.000 tình nguyện viên. Hai mũi tiêm cách nhau 28 ngày. Sau thời gian tiêm chủng, 95 người đã nhiễm nCoV. Trong số đó, chỉ 5 trường hợp tiêm vaccine, còn lại dùng giả dược.
Eleanor Riley, giáo sư miễn dịch học và bệnh truyền nhiễm tại Đại học Edinburgh, cho biết: “Có nhiều hơn một vaccine hiệu quả sẽ làm tăng nguồn cung toàn cầu. Nếu may mắn, chúng ta có thể trở lại cuộc sống bình thường năm 2021″.
Cả hai “ứng viên” đều được phát triển bằng công nghệ mới RNA thông tin, có khả năng kích thích tế bào người tạo ra protein virus. Sau đó, hệ miễn dịch tiếp xúc với protein và sinh ra kháng thể, các tế bào miễn dịch nhận biết và tiêu diệt mầm bệnh.
Moderna dự kiến nộp đơn xin phê duyệt khẩn cấp cho giới chức Mỹ trong tuần tới nếu có đủ dữ liệu an toàn.
Video đang HOT
Vaccine Covid-19 của Moderna hiệu quả 94,5%. Ảnh: Reuters
Ưu điểm của vaccine Moderna là không cần bảo quản cực lạnh như sản phẩm của Pfizer, giúp quá trình phân phối dễ dàng hơn. Các liều tiên có thể được lưu trữ ở tủ lạnh y tế thông thường, mức nhiệt 2-8 độ C trong vòng 30 ngày.
Dữ liệu từ Moderna cũng cho thấy vaccine ngăn ngừa được các trường hợp mắc Covid-19 nghiêm trọng. Đây là câu hỏi còn bỏ ngỏ đối với “ứng viên” từ Pfizer. Trong số 95 tình nguyện viên dương tính, 11 trường hợp nghiêm trọng. Tất cả đều là người dùng giả dược.
Vaccine của Moderna là một phần trong Chiến dịch Thần tốc của Chính phủ Mỹ. Chương trình dự kiến sản xuất 20 triệu liều tiêm cho người dân nước này trong năm nay.
“Nếu được cấp phép, chúng tôi sẵn sàng giao hàng qua Chiến dịch Thần tốc trong vài giờ. Như vậy, vaccine có thể được phân phối ngay lập tức”, ông Hoge nói.
Hầu hết tác dụng phụ của vaccine Moderna là từ nhẹ đến trung bình. Song nhiều tình nguyện viên cũng gặp triệu chứng dữ dội hơn sau khi tiêm mũi thứ hai. 10% bị mệt mỏi nghiêm trọng, không thể sinh hoạt bình thường. 9% khác bị đau cơ. Đại diện Moderna cho biết tình trạng này không kéo dài. Peter Openshaw, giáo sư tại Cao đẳng Hoàng gia London, giải thích: “Đây là các phản ứng dễ đoán đối với một loại vaccine hiệu quả và tạo ra miễn dịch tốt”.
Pfizer thông báo vaccine mà hãng hợp tác sản xuất với công ty dược phẩm BioNTech của Đức đạt hiệu quả 90% hôm 9/11. Đây được coi là tin tuyệt vời đối với khoa học và nhân loại. Thử nghiệm giai đoạn 3 được thực hiện trên hơn 40.000 người. Sau khi tiêm chủng, 94 tình nguyện viên đã nhiễm virus.
Đến nay, toàn thế giới có hơn 100 loại vaccine đang được phát triển. 12 “ứng viên” đã tiến đến thử nghiệm lâm sàng giai đoạn cuối, thuộc về Mỹ, Đức, Trung Quốc, Anh, Nga, Ấn Độ. Hồi tháng 8, Nga đã chấp thuận khẩn cấp vaccine Sputnik V trước khi hoàn thành thử nghiệm giai đoạn 3. Ngày 12/11, Quỹ đầu tư trực tiếp Nga (RDIF) cho biết Sputnik V đạt hiệu quả 90% và vài ngày sau “sửa” lại 92%, song không công bố các dữ liệu chi tiết mà “dựa trên quan sát”.
Moderna hoàn tất thử nghiệm vaccine Covid-19 giai đoạn 3
Hãng dược Moderna cho biết đã hoàn thành thử nghiệm vaccine giai đoạn 3 cho 30.000 tình nguyện viên tham gia.
Quá trình nghiên cứu được theo dõi chặt chẽ để đảm bảo sự đa dạng tình nguyện viên. Theo dữ liệu của công ty, 1/5 tình nguyện viên đến từ Tây Ban Nha và 10% là người da đen. Tình nguyện viên trên 65 tuổi, đối tượng có nguy cơ cao nhiễm nCoV, chiếm 25%.
"Tôi nghĩ rằng chúng tôi đang làm khá tốt, yếu tố nhân khẩu của thử nghiệm vaccine Moderna khá đa dạng", Larry Corey, chuyên gia virus tại Trung tâm Nghiên cứu Ung thư Fred Hutchinson, nhận định. Ông Corey đang tiến hành các thử nghiệm lâm sàng trong Chiến dịch Thần tốc - nỗ lực liên bang nhằm đẩy nhanh tiến độ phát triển vaccine.
"Chúng tôi hy vọng sẽ tiếp tục cải thiện điều này. Đây mới là thử nghiệm đầu tiên hoàn thành, chúng ta còn hai loại khác nữa. Chặng đường đến với vaccine Covid-19 chỉ mới bắt đầu", ông Corey nói, đề cập đến hai loại vaccine khác của hai nhà nghiên cứu Pfizer và Johnson & Johnson.
Hơn một nửa số tình nguyện viên của Moderna đều là người khỏe mạnh, không dễ nhiễm nCoV. 25% khác là người cao tuổi, 17% trẻ hơn, song mắc các bệnh nền như tiểu đường hoặc béo phì, khiến họ nằm trong nhóm rủi ro cao.
Dữ liệu đánh giá thử nghiệm vaccine của Moderna được lưu tại Trung tâm nghiên cứu Mỹ ở Hollywood, Florida. Ảnh: AFP
Tiến sĩ Stephen Hoge, chủ tịch của Moderna, cho biết chủng ngừa cho 30.000 tình nguyện viên "chỉ là cột mốc quan trọng, không phải thành tựu". 50% trong đó đã nhận vaccine, số còn lại tiêm giả dược là nước muối sinh lý. Hai mũi tiêm cách nhau 4 tuần.
Moderna dự kiến công bố dữ liệu sơ bộ của thử nghiệm giai đoạn 3 trong tháng 11. Sau hai tháng theo dõi, công ty sẽ xác định liệu sản phẩm có đủ tiêu chuẩn đệ trình lên cơ quan quản lý để xin cấp phép hay không. Họ kỳ vọng hoàn thành toàn bộ quá trình trước Lễ Tạ ơn, ngày 26/11 năm nay.
Hiện Moderna, Pfizer và Johnson & Johnson là ba hãng dược dẫn đầu cuộc đua phát triển vaccine tại Mỹ. Moderna khởi động thử nghiệm giai đoạn 3 ngày 27/2, cùng ngày với Pfizer. Vaccine do Johnson & Johnson sản xuất bắt đầu tiêm thử ngày 23/9, song phải ngừng sau chưa đầy ba tuần vì một tình nguyện viên bị ốm. AstraZeneca, hãng dược của Anh, gặp tình trạng tương tự.
Thử nghiệm lâm sàng các loại vaccine bao gồm ba giai đoạn. Ở giai đoạn một, các nhà khoa học tiêm vaccine cho số tình nguyện viên hạn chế để kiểm tra độ an toàn và xác định liều lượng. Giai đoạn hai, thử nghiệm diễn ra trên hàng trăm người, chia thành các nhóm, chẳng hạn trẻ em, người già, để xem liệu liều tiêm có tạo ra phản ứng khác nhau ở từng đối tượng hay không. Trong thử nghiệm giai đoạn ba, các nhà nghiên cứu tiêm vaccine hoặc giả dược trên hàng chục nghìn người, chia làm hai nhóm. Tình nguyện sau đó trở về vùng dịch sinh sống nhằm so sánh tỷ lệ lây nhiễm.
Sau thử nghiệm giai đoạn ba, đơn vị nghiên cứu sẽ đệ trình dữ liệu lên cơ quan quản lý để xin cấp phép. Trong thời kỳ đại dịch, một số loại vaccine được phê duyệt khẩn cấp khi đang trong nghiên cứu giai đoạn 3.
Khi đã được cơ quan quản lý chấp thuận, các nhà nghiên cứu tiếp tục theo dõi phản ứng của nhóm tình nguyện viên nhằm tìm ra các tác dụng phụ tiềm ẩn. Đây gọi là quá trình đánh giá sau phê duyệt. Nếu vaccine được chứng minh là an toàn và hiệu quả, nhà sản xuất sẽ tiến hành phân phối hàng loạt đến các cơ sở y tế, phục vụ cho chương trình tiêm chủng.
Thông thường toàn bộ quy trình từ nghiên cứu đến cấp phép, phân phối ra thị trường của một loại vaccine mới mất ít nhất hai năm. Trong bối cảnh Covid-19 lan rộng, một số chính phủ thúc đẩy quá trình nghiên cứu cấp phép vaccine này nhanh hơn bình thường. Thậm chí Nga đã cấp phép cho hai loại vaccine Covid-19 trước khi tiến hành các giai đoạn thử nghiệm lâm sàng, dẫn đến nhiều hoài nghi của các nhà khoa học về chất lượng sản phẩm.
Đến nay 6 loại vaccine Covid-19 được phê duyệt khẩn cấp, đều thuộc về Trung Quốc và Nga. Hai "ứng viên" của Nga là Sputnik V và EpiVacCorona. Bốn loại vaccine của Trung Quốc do hãng dược nhà nước và các Viện Sinh phẩm điều chế, chủ yếu dựa trên virus bất hoạt.
5 người gặp phản ứng phụ khi tham gia thử nghiệm 2 loại vaccine Covid-19 hàng đầu tại Mỹ  Cả 5 người tham gia thử nghiệm cho biết họ bị sốt cao, đau nhức cơ thể, đau đầu, kiệt sức suốt cả ngày và các triệu chứng khác sau khi tiêm. 5 trong số những tình nguyện viên người Mỹ tham gia thử nghiệm giai đoạn cuối loại vaccine ngừa Covid-19 tiềm năng của hai hãng Moderna và Pfizer đã bắt gặp...
Cả 5 người tham gia thử nghiệm cho biết họ bị sốt cao, đau nhức cơ thể, đau đầu, kiệt sức suốt cả ngày và các triệu chứng khác sau khi tiêm. 5 trong số những tình nguyện viên người Mỹ tham gia thử nghiệm giai đoạn cuối loại vaccine ngừa Covid-19 tiềm năng của hai hãng Moderna và Pfizer đã bắt gặp...
 Trung Quốc tung chatbot đấu ChatGPT, cổ phiếu Phố Wall chao đảo bốc hơi 1.000 tỉ14:53
Trung Quốc tung chatbot đấu ChatGPT, cổ phiếu Phố Wall chao đảo bốc hơi 1.000 tỉ14:53 Ý tưởng gây sốc của Tổng thống Trump về Dải Gaza08:59
Ý tưởng gây sốc của Tổng thống Trump về Dải Gaza08:59 Tàu vận tải Nga cập cảng Syria, chuẩn bị cho cuộc rút quân09:12
Tàu vận tải Nga cập cảng Syria, chuẩn bị cho cuộc rút quân09:12 Hé lộ kế hoạch mới của ông Trump về xung đột Nga-Ukraine08:31
Hé lộ kế hoạch mới của ông Trump về xung đột Nga-Ukraine08:31 Ông Trump nói muốn gặp ông Putin ngay lập tức08:46
Ông Trump nói muốn gặp ông Putin ngay lập tức08:46 "Hỏa thần nhiệt áp" Nga ra đòn, nhằm thẳng cứ điểm Ukraine ở Kursk08:59
"Hỏa thần nhiệt áp" Nga ra đòn, nhằm thẳng cứ điểm Ukraine ở Kursk08:59 Tổng thống Trump lên tiếng về 'thảm kịch' hàng không ở thủ đô Washington DC10:41
Tổng thống Trump lên tiếng về 'thảm kịch' hàng không ở thủ đô Washington DC10:41 Iran công bố tên lửa đạn đạo mới nhất08:23
Iran công bố tên lửa đạn đạo mới nhất08:23 Nga xác nhận có cơ hội đàm phán với chính quyền Tổng thống Trump14:35
Nga xác nhận có cơ hội đàm phán với chính quyền Tổng thống Trump14:35 Phương Tây đang học hỏi từ chiến sự Ukraine09:10
Phương Tây đang học hỏi từ chiến sự Ukraine09:10 Hamas vừa thả 4 nữ binh sĩ Israel, sẽ nhận lại được gì?02:38
Hamas vừa thả 4 nữ binh sĩ Israel, sẽ nhận lại được gì?02:38Tiêu điểm
Tin đang nóng
Tin mới nhất

Thế giới vừa trải qua tháng 1 nóng nhất lịch sử

Nga đã vô hiệu hóa vũ khí hạt nhân chiến thuật của Ukraine như thế nào?

Hé lộ nguồn tài nguyên là 'nhân tố bí ẩn' của kế hoạch tiếp quản Gaza

Sắc màu cuộc sống: Nghệ thuật xoa dịu nỗi đau sau thảm họa động đất tại Thổ Nhĩ Kỳ

Từ đâu ông Trump đưa ra tuyên bố táo bạo về tiếp quản Gaza?

Người Palestine nghĩ gì về kế hoạch tiếp quản Gaza của ông Trump?

Ngoại trưởng Mỹ giải thích tuyên bố của ông Trump về 'tiếp quản Gaza'

Ông Trump cấm người chuyển giới tham gia các môn thể thao dành cho nữ

Argentina theo chân Mỹ rút khỏi Tổ chức Y tế Thế giới

Thái Lan tiêu hủy hơn 60 tấn sầu riêng xuất khẩu bị nhiễm hóa chất gây ung thư

Tòa án Hiến pháp Hàn Quốc nối lại xét xử Tổng thống Yoon Suk Yeol

Bác sĩ bị phát hiện lén dùng máy CT của bệnh viện chụp cho mèo cưng
Có thể bạn quan tâm

Bé trai khóc thét khi rơi thẳng từ mái nhà xuống đất: Đoạn camera khiến gia chủ run rẩy
Netizen
23:23:18 06/02/2025
Trấn Thành: "Tôi tự tin mình sẽ làm ra bộ phim ngàn tỷ đầu tiên của Việt Nam"
Hậu trường phim
23:00:44 06/02/2025
Những cảnh giường chiếu gây sốc nhất trong phim Hàn
Phim châu á
22:45:39 06/02/2025
Người đàn ông cứu được con mèo đã kinh ngạc khi biết sự thật về sinh vật này
Lạ vui
22:24:48 06/02/2025
Chàng trai Hải Dương cao 1,88m thi Nam vương Du lịch Thế giới
Sao việt
22:20:57 06/02/2025
Lâm Y Thần tiết lộ lý do lập di chúc khi ở đỉnh cao sự nghiệp
Sao châu á
22:13:40 06/02/2025
Vợ Ryan Reynolds lại bị kiện, đòi bồi thường 7 triệu USD
Sao âu mỹ
22:06:38 06/02/2025
Thầy giáo gặp cảnh 'con anh, con em' với vợ kém tuổi khiến Hồng Vân xót xa
Tv show
22:04:02 06/02/2025
Hà Nội: Thiếu niên bị đâm nhập viện tại lễ hội chùa Đậu
Pháp luật
22:03:56 06/02/2025
Học sinh THPT ở Đồng Nai cho bạn vay nặng lãi, cao gấp 12-28 lần lãi ngân hàng
Tin nổi bật
22:02:22 06/02/2025

 Đội ngũ ông Trump đang “giăng bẫy” ông Biden?
Đội ngũ ông Trump đang “giăng bẫy” ông Biden?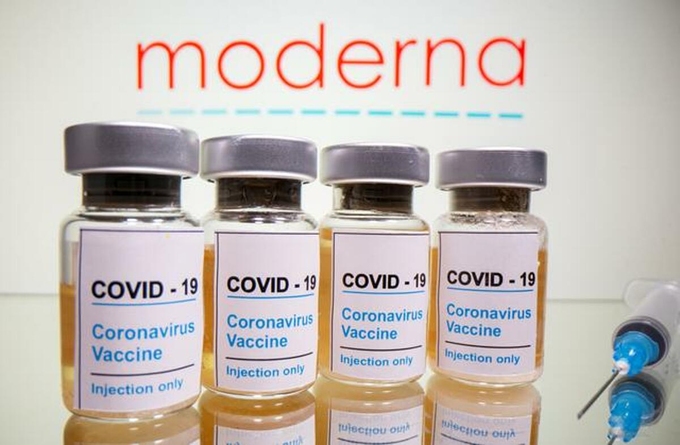

 Vaccine Oxford 'hẹn' ra mắt cuối năm nay
Vaccine Oxford 'hẹn' ra mắt cuối năm nay Những lo ngại khi vaccine Oxford tạm dừng thử nghiệm
Những lo ngại khi vaccine Oxford tạm dừng thử nghiệm Phiền toái khi vaccine Covid-19 cần tiêm hai liều
Phiền toái khi vaccine Covid-19 cần tiêm hai liều Mỹ đặt mua thêm 100 triệu liều vaccine ngừa Covid-19
Mỹ đặt mua thêm 100 triệu liều vaccine ngừa Covid-19 Mỹ sẵn sàng chia sẻ vaccine chống Covid-19 với thế giới
Mỹ sẵn sàng chia sẻ vaccine chống Covid-19 với thế giới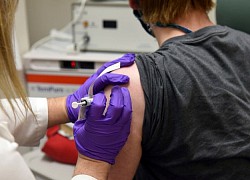 Mỹ thử nghiệm vaccine Covid-19 quy mô lớn
Mỹ thử nghiệm vaccine Covid-19 quy mô lớn
 Tỉ phú Musk kiểm soát hệ thống thanh toán của Bộ Tài chính Mỹ
Tỉ phú Musk kiểm soát hệ thống thanh toán của Bộ Tài chính Mỹ

 Nga bắt đầu áp dụng chế độ trục xuất người nước ngoài vi phạm
Nga bắt đầu áp dụng chế độ trục xuất người nước ngoài vi phạm Nhân tố then chốt hàng đầu trong Chính quyền của Tổng thống Trump
Nhân tố then chốt hàng đầu trong Chính quyền của Tổng thống Trump Chiến dịch trấn áp người nhập cư bắt đầu 'làm nóng' đường phố Mỹ
Chiến dịch trấn áp người nhập cư bắt đầu 'làm nóng' đường phố Mỹ Trộm cuỗm 100.000 quả trứng giá cả tỉ đồng giữa 'lạm phát' tại Mỹ
Trộm cuỗm 100.000 quả trứng giá cả tỉ đồng giữa 'lạm phát' tại Mỹ Thi thể thiếu niên 16 tuổi bị cột vào đầu bơm nước, nổi trên kênh ở Đồng Tháp
Thi thể thiếu niên 16 tuổi bị cột vào đầu bơm nước, nổi trên kênh ở Đồng Tháp Bạn thân tiết lộ tình trạng của Uông Tiểu Phi: Tái phát bệnh tâm thần, liên tục gào thét "Tôi muốn chết"
Bạn thân tiết lộ tình trạng của Uông Tiểu Phi: Tái phát bệnh tâm thần, liên tục gào thét "Tôi muốn chết" NS Lê Quốc Nam tiếp tục lên tiếng sau khi tố Minh Dự: "Tôi nhận lời xin lỗi, họ xin làm sự việc nhẹ lại"
NS Lê Quốc Nam tiếp tục lên tiếng sau khi tố Minh Dự: "Tôi nhận lời xin lỗi, họ xin làm sự việc nhẹ lại"
 Chồng Từ Hy Viên chính thức "tuyên chiến" với chồng cũ nữ diễn viên, nói 1 câu về khối tài sản khiến dân mạng dậy sóng!
Chồng Từ Hy Viên chính thức "tuyên chiến" với chồng cũ nữ diễn viên, nói 1 câu về khối tài sản khiến dân mạng dậy sóng! Cô gái được Vũ Cát Tường cầu hôn sau nhiều năm hẹn hò bí mật là ai?
Cô gái được Vũ Cát Tường cầu hôn sau nhiều năm hẹn hò bí mật là ai? 5 năm yêu đương kín tiếng của Vũ Cát Tường và bạn gái vũ công
5 năm yêu đương kín tiếng của Vũ Cát Tường và bạn gái vũ công
 Vụ cô gái rơi khỏi ô tô đang chạy trên đường: Quá say nên tự lột đồ?
Vụ cô gái rơi khỏi ô tô đang chạy trên đường: Quá say nên tự lột đồ? Bi kịch Vườn Sao Băng: Từ Hy Viên và 4 ngôi sao khác lần lượt qua đời khi chưa đầy 50 tuổi
Bi kịch Vườn Sao Băng: Từ Hy Viên và 4 ngôi sao khác lần lượt qua đời khi chưa đầy 50 tuổi Những dấu hiệu vi phạm trong vụ clip cô gái rơi khỏi ô tô khi xe đang chạy
Những dấu hiệu vi phạm trong vụ clip cô gái rơi khỏi ô tô khi xe đang chạy Truy tố nữ DJ ở TPHCM cầm đầu đường dây mua bán hơn 100kg ma túy
Truy tố nữ DJ ở TPHCM cầm đầu đường dây mua bán hơn 100kg ma túy Đàm Vĩnh Hưng mất hơn 4 ngón chân?
Đàm Vĩnh Hưng mất hơn 4 ngón chân? Bé gái trộm bộ trang sức trị giá 3,4 tỷ đồng của mẹ để bán với giá chỉ 200.000 đồng, mục đích phía sau gây tranh cãi
Bé gái trộm bộ trang sức trị giá 3,4 tỷ đồng của mẹ để bán với giá chỉ 200.000 đồng, mục đích phía sau gây tranh cãi
 Người đàn ông chui ra khỏi taxi rồi băng qua cao tốc TP HCM – Trung Lương
Người đàn ông chui ra khỏi taxi rồi băng qua cao tốc TP HCM – Trung Lương Rộ hình ảnh nhiều vết tiêm bất thường trên tay Từ Hy Viên khi qua đời, cái chết nghi có uẩn khúc
Rộ hình ảnh nhiều vết tiêm bất thường trên tay Từ Hy Viên khi qua đời, cái chết nghi có uẩn khúc Xôn xao clip cô gái không mặc quần áo bất ngờ rơi khỏi xe ôtô
Xôn xao clip cô gái không mặc quần áo bất ngờ rơi khỏi xe ôtô