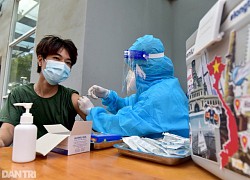
Tháng 8, Bộ Y tế sẽ xem xét cấp phép khẩn cấp vắc xin Nanocovax
Bộ Y tế đề nghị Công ty Nanogen trước ngày 15/8 gửi báo cáo dữ liệu nghiên cứu pha 2 và bước đầu pha 3, để từ đó Hội đồng đạo đức và Hội đồng cấp phép của Bộ xem xét cấp phép khẩn cấp.
Ngày 2/8, GS.TS Trần Văn Thuấn, Thứ trưởng Bộ Y tế chủ trì cuộc họp trực tuyến về rà soát tiến độ, thúc đẩy quá trình thử nghiệm lâm sàng, đôn đốc báo cáo kết quả nghiên cứu giai đoạn 1, 2, 3 (a,b) của vắc xin Nanocovax do Công ty cổ phần Công nghệ sinh học dược Nanogen sản xuất.
Công ty đang triển khai theo đề cương nghiên cứu. Cụ thể, pha 3 được thử nghiệm trên 13.000 người, chia làm 2 giai đoạn nhỏ (3a: 1.000 người và 3b: 12.000 người).
Kết quả D42 của 1.000 người pha 3a được thu thập cho thấy 100% đối tượng được tiêm Nanocovax có kháng thể trung hòa Surrogate trên ngưỡng 30%. 99,2% đối tượng chuyển đổi huyết thanh của kháng thể IgG kháng Protein S gấp 4 lần so với nền. Công ty tiếp tục theo dõi 1.000 đối tượng giai đoạn 3a và 12.000 đối tượng pha 3b theo đề cương nghiên cứu.
Nanocovax: Vắc xin an toàn và có tính sinh miễn dịch tương đối cao
Song song với việc xin cấp phép sử dụng khẩn cấp có điều kiện, Công ty Nanogen cũng kiến nghị Bộ Y tế, Hội đồng Đạo đức trong Nghiên cứu Y sinh học Quốc gia xem xét việc triển khai nghiên cứu giai đoạn 3c (tiêm cho khoảng 500.000 – 1.000.000 người). Đồng thời, nghiên cứu trên trẻ em từ 12 đến 18 tuổi, sau khi được cấp phép.
Sau khi nghe báo cáo kết luận của các chuyên gia đầu ngành, GS Trần Văn Thuấn khẳng định, Bộ Y tế rất mong sớm có vắc xin tự sản xuất trong nước để bảo vệ người dân, để giảm sự lệ thuộc về vắc xin nhập khẩu.
“Có tín hiệu mừng, vui là vắc xin an toàn và có tính sinh miễn dịch tương đối cao. Tuy nhiên, chúng ta chưa có dữ liệu chắc chắn về hiệu quả bảo vệ của vắc xin đến đâu. Chúng ta cần chờ thêm thời gian và kết quả nghiên cứu”, GS Thuấn nói.
Bộ Y tế luôn ủng hộ, mong muốn và tạo điều kiện thuận lợi nhất cho các công ty, cá nhân tham gia vào quá trình sản xuất vắc xin phòng chống Covid-19. Vì vậy, Bộ đã huy động nhiều nhà khoa học đầu ngành của đất nước tham gia vào đánh giá, nghiên cứu và thẩm định.
Bộ Y tế đề nghị Công ty Nanogen trước ngày 15/8, phải gửi báo cáo dữ liệu nghiên cứu pha 2 và bước đầu pha 3, từ đó Bộ Y tế có số liệu gửi Hội đồng đạo đức và Hội đồng cấp phép của Bộ Y tế xem xét cấp phép trong tình trạng khẩn cấp.
Bên trong "công xưởng" sản xuất vắc xin Covid-19 Việt Nam
Dự kiến, đến cuối năm nay dây chuyền này có thể cho ra lò 30-50 triệu liều vắc xin Nanocovax mỗi tháng.
"Soi" công nghệ sản xuất vắc xin Nanocovax
Vắc xin Covid-19 "made in Vietnam" Nanocovax của Công ty Nanogen hiện đang bước vào giai đoạn thử nghiệm lâm sàng thứ 3, với quy mô thử nghiệm lên đến 13.000 người.
Để sản xuất vắc xin Nanocovax, Nanogen đã sử dụng công nghệ protein tái tổ hợp. Đây là con đường khác với nhiều hãng dược đang làm là cấy đoạn gen virus trực tiếp vào người.
Cận cảnh "công xưởng" sản xuất vắc xin Covid-19 Việt Nam
Công nghệ protein tái tổ hợp cũng là một trong những hướng phát triển vắc xin Covid-19 tiên tiến nhất hiện nay. Nanocovax là vắc xin được xếp loại protein tiểu đơn vị (protein subunit). Theo Tổ chức Y tế Thế giới, tính đến ngày 4/6, số lượng ứng viên vắc xin sử dụng công nghệ tiểu đơn vị protein đứng đầu trong giai đoạn thử nghiệm lâm sàng với 32 trên tổng số 102 ứng viên.
Bằng công nghệ ADN tái tổ hợp, Nanogen tạo ra dòng tế bào sản xuất protein S (CHO-RSP).
Cụ thể, Nanogen sử dụng tế bào CHO - một loại tế bào có thiết kế gần như tế bào người (được độc quyền bởi Nanogen) - làm môi trường tạo nên protein gai S.
Tuy sản lượng protein gai S sản xuất được từ tế bào CHO là ít và giá của tế bào CHO cao nhưng Nanogen vẫn quyết định sử dụng vì protein gai S tạo ra từ tế bào CHO có chất lượng tốt (giống gai S thật) nên sẽ kích thích được khả năng đáp ứng miễn dịch cao cho cơ thể khi tiêm vắc xin.
Tế bào tái tổ hợp CHO-RSP sau khi phân lập được bảo quản ở nhiệt độ -150 độ C để sử dụng cho quá trình tổng hợp protein S, đây là thành phần kháng nguyên của Nanocovax.
Protein gai S sau đó được thu hoạch, tinh sạch và trộn cùng tá dược để tạo nên thành phẩm vắc xin. Do không dùng bất kì thành phần sống nào của virus nên Nanocovax có độ an toàn cao.
Một bước trong quá trình tinh chế protein S bằng hệ thống máy sắc ký.
Mẫu kháng nguyên tinh sạch được pha chế thành dung dịch kháng nguyên và lọc vô trùng bởi hệ thống pha chế tự động. Sau đó, tá dược được bổ sung để tạo thành vắc xin bán thành phẩm.
TS Hồ Nhân, Tổng giám đốc Công ty Nanogen chia sẻ: "Cách làm vắc xin bằng cấy gen trực tiếp tuy nhanh hơn nhưng tính mạo hiểm cao hơn nhiều. Mục tiêu mà Nanogen hướng tới là tạo nên vắc xin có thể bảo vệ cơ thể 100%".
Dây chuyền đóng gói vắc xin Nanocovax.
Nói đến công nghệ protein tái tổ hợp, ngoài Nanocovax, một ứng viên nổi bật trên thế giới là vắc xin Novavax hay Sanofi - GSK.
Hiện Novavax vẫn chưa được cấp phép ở bất kỳ quốc gia nào. Mặc dù có hiệu quả 86% trong việc bảo vệ chống lại biến thể virus ở Anh.
Dự kiến đến cuối năm có 50 triệu liều Nanocovax được ra lò
Nanogen có 4 nhà máy, 3 nhà máy tại TPHCM với diện tích lần lượt là 5.000 m2, 10.000 m2, 24.000 m2, một nhà máy ở Lâm Đồng có diện tích 34.000 m2 và một Trung tâm Nghiên cứu và Phát triển với tổng diện tích là 73.000 m2.
Công suất sản xuất vắc xin Covid-19 hiện tại của Nanogen là khoảng 8.000.000 liều/tháng. Nanogen đã đặt hàng tank pha chế 1000L (tháng 8 sẽ lắp đặt và vận hành), sau khi lắp đặt, tổng công suất sản xuất tối đa sẽ đạt 10.000.000 liều/tháng cho cả 2 dây chuyền bơm tiêm và lọ.
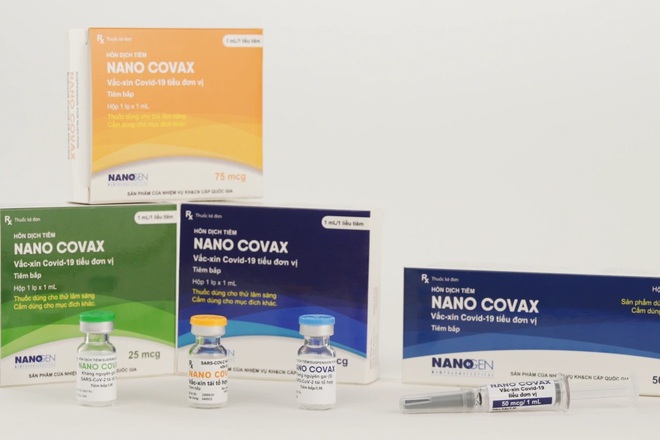
Vắc xin Nanocovax.
"Từ giờ cho đến tháng 10, dây chuyền sản xuất của Nanogen có thể đạt công suất 10 - 12 triệu liều/tháng và sau tháng 10 dự kiến có thể nâng công suất lên 30 - 50 triệu liều/tháng, để cung cấp trong nước và cả nước ngoài", TS Hồ Nhân chia sẻ.
Trong quá trình nghiên cứu và sản xuất, các mẫu nguyên liệu, bán thành phẩm và thành phẩm được kiểm nghiệm liên tục, nhằm đảm bảo vắc xin đạt tiêu chuẩn cao nhất.
Dựa trên kế hoạch và năng lực hiện tại, dự kiến đến cuối năm 2021, Nanogen sẽ sản xuất được khoảng 50 triệu liều vắc xin Nanocovax và sẽ ưu tiên trong nước.
Nanogen cũng đang cố gắng hoàn thiện, mở rộng hệ thống kho lạnh với sức chứa 10 triệu liều và đội ngũ xe lạnh đạt chuẩn đạt chuẩn quốc tế (giữ nhiệt 2-8C) để vận chuyển vắc xin.
Sáng 25/6, Bộ Y tế đã tổ chức họp khẩn với các đơn vị liên quan đánh giá tiến độ thử nghiệm và kế hoạch mở rộng địa điểm thử nghiệm vắc xin Nanocovax.
Dựa trên kết quả nghiệm thu giữa kỳ giai đoạn 2 vào ngày 28/5, Hội đồng Hội đồng Đạo đức trong nghiên cứu y sinh học Quốc gia đánh giá vắc xin Nanocovax có tính an toàn và tính sinh miễn dịch ở giai đoạn thử nghiệm này. Để đánh giá hiệu lực bảo vệ của vắc xin thì cần thêm thời gian và số lượng mẫu, đặc biệt kết quả đánh giá trong phòng thí nghiệm.
Sau khi xem xét, Bộ Y tế, Hội đồng thống nhất với Viện Pasteur TPHCM và Học viện Quân y đẩy nhanh tốc độ thử nghiệm trên toàn bộ 13.000 tình nguyện viên. Dự kiến đến ngày 15/7 sẽ tiêm xong mũi một cho 13.000 người tình nguyện của giai đoạn 3 và ngày 15/8 sẽ tiêm xong mũi 2 cho 13.000 người tình nguyện của giai đoạn 3. Trong tháng 8, các đơn vị phải có dữ liệu thử nghiệm giai đoạn 3 để báo cáo Bộ Y tế.
Bộ Y tế họp khẩn về tiến độ thử nghiệm vắc xin Nanocovax  Sáng nay, Cục Khoa học Công nghệ-Đào tạo, Hội đồng đạo đức của Bộ Y tế có cuộc họp trực tuyến nhằm đánh giá tiến độ và xem xét mở rộng địa điểm nghiên cứu thử nghiệm lâm sàng vắc xin Nanocovax. Cuộc họp do lãnh đạo Cục Khoa học công nghệ - Đào tạo, lãnh đạo Hội đồng Đạo đức nghiên cứu...
Sáng nay, Cục Khoa học Công nghệ-Đào tạo, Hội đồng đạo đức của Bộ Y tế có cuộc họp trực tuyến nhằm đánh giá tiến độ và xem xét mở rộng địa điểm nghiên cứu thử nghiệm lâm sàng vắc xin Nanocovax. Cuộc họp do lãnh đạo Cục Khoa học công nghệ - Đào tạo, lãnh đạo Hội đồng Đạo đức nghiên cứu...
 Vụ dụ dỗ người dân tu tập mê tín: Một bị hại phải bán 3 căn nhà ở Hà Nội01:02
Vụ dụ dỗ người dân tu tập mê tín: Một bị hại phải bán 3 căn nhà ở Hà Nội01:02 Công an xác minh clip người đàn ông khuyết tật bị hai thanh niên đi xe máy không mũ bảo hiểm tát vào đầu01:20
Công an xác minh clip người đàn ông khuyết tật bị hai thanh niên đi xe máy không mũ bảo hiểm tát vào đầu01:20 Thực hư clip xe cứu thương chế còi "cố lên, sắp tới rồi" chạy ở TPHCM00:28
Thực hư clip xe cứu thương chế còi "cố lên, sắp tới rồi" chạy ở TPHCM00:28 Xác minh clip 2 tài xế ô tô cầm kiếm dọa chém nhau giữa đường ở TPHCM00:52
Xác minh clip 2 tài xế ô tô cầm kiếm dọa chém nhau giữa đường ở TPHCM00:52 Ô tô đâm sập cửa nhà dân ở Thái Nguyên, cuốn người đàn ông vào gầm08:05
Ô tô đâm sập cửa nhà dân ở Thái Nguyên, cuốn người đàn ông vào gầm08:05 Thông tin về clip CSGT quật ngã người đàn ông ở TPHCM07:30
Thông tin về clip CSGT quật ngã người đàn ông ở TPHCM07:30 Vụ trâu húc 2 người nhập viện ở Bình Chánh: Do nạn nhân chọc ghẹo trâu09:16
Vụ trâu húc 2 người nhập viện ở Bình Chánh: Do nạn nhân chọc ghẹo trâu09:16 Phú bà rinh hết gia sản 'dằn mặt' mẹ chồng, ngày cưới kéo tới 3 thứ khủng?04:38
Phú bà rinh hết gia sản 'dằn mặt' mẹ chồng, ngày cưới kéo tới 3 thứ khủng?04:38 Ô tô con 'phóng như bay' gây tai nạn liên hoàn ở Đồng Nai00:50
Ô tô con 'phóng như bay' gây tai nạn liên hoàn ở Đồng Nai00:50 Hằng Du Mục 'đối đầu' nhóm chống phá, tuyên bố lập vi bằng, 'nhá' loạt chứng cứ?04:05
Hằng Du Mục 'đối đầu' nhóm chống phá, tuyên bố lập vi bằng, 'nhá' loạt chứng cứ?04:05 Vụ mất con ở BV Phụ Sản Trung ương: người nhà tố 1 câu đắng lòng?03:19
Vụ mất con ở BV Phụ Sản Trung ương: người nhà tố 1 câu đắng lòng?03:19Tiêu điểm
Tin đang nóng
Tin mới nhất

Vụ cháy gần ngã tư Bình Phước may mắn không thiệt hại về người

Vĩnh Phúc: Khắc phục vụ cháy tại thị trấn Thổ Tang

TPHCM: Cháy kho đồ nhựa gần ngã tư Bình Phước, hàng chục xe chữa cháy được huy động

Thót tim cảnh nhấc xe bán tải cứu bé trai bị kẹt dưới gầm

Đột ngột chuyển sai hướng, ô tô gây tai nạn liên hoàn ở Đắk Lắk

Cùng nhóm bạn ra đập tắm, 2 học sinh bị chết đuối

Hóa chất lạ nghi là dầu bị đổ trên đèo Prenn

Mua ô tô mà không đăng ký sang tên có thể bị phạt tới 12 triệu đồng

Tuyên dương 2 người dập lửa cứu nạn nhân vụ 'con dùng xăng đốt mẹ ruột'

Cháy cửa hàng điện thoại ở Đồng Hới, nhiều tài sản bị thiêu rụi

Lâm Đồng: Xe tải chở bia cháy rụi cabin khi qua đèo Mimosa

Nhanh chóng khống chế đám cháy phòng trà trong khu dân cư ở Đà Nẵng
Có thể bạn quan tâm

"Nam thần mơ ước của các cô gái" lộ nhan sắc thật qua cam thường
Sao châu á
13:27:18 01/03/2025
1 Chị Đẹp thừa nhận thấy "quá dở" khi nghe lại nhạc của mình, đáp 3 chữ "cảm lạnh" vì fan đòi remix lại hit cũ
Nhạc việt
13:15:47 01/03/2025
Sự thật video nữ y tá quỳ xin lỗi bệnh nhân thu hút 100 triệu lượt xem
Netizen
13:15:04 01/03/2025
Vì sao Văn Toàn dễ dàng cho Hoà Minzy vay 4 tỷ nhưng lần thứ hai cô bạn thân hỏi vay tiếp thì say "No"?
Sao thể thao
13:13:42 01/03/2025
Tổng thống Trump có thể ký sắc lệnh ghi nhận tiếng Anh là ngôn ngữ chính thức của Mỹ
Thế giới
13:09:29 01/03/2025
7 thị trấn kỳ lạ nhất thế giới siêu hút khách du lịch: Có nơi chỉ được sống nhưng không thể chết
Lạ vui
12:58:56 01/03/2025
Ngoại hình biến đổi gây sốc của Lisa (BLACKPINK)
Nhạc quốc tế
12:50:32 01/03/2025
Cách dùng nha đam trị mụn
Làm đẹp
12:46:54 01/03/2025
Trà đen: lợi ích sức khỏe và những lưu ý khi sử dụng
Sức khỏe
12:43:09 01/03/2025
Mặc đẹp với quần jeans và áo tank top, bộ đôi đơn giản mà sành điệu
Thời trang
12:24:19 01/03/2025
 Bộ trưởng Y tế: “Nhiều địa phương triển khai tiêm vắc xin quá dè dặt”
Bộ trưởng Y tế: “Nhiều địa phương triển khai tiêm vắc xin quá dè dặt” Đi xem tai nạn, 51 người ở Phú Thọ trở thành F1
Đi xem tai nạn, 51 người ở Phú Thọ trở thành F1








 Trước khi xin cấp phép khẩn cấp, kết quả thử nghiệm của Nanocovax ra sao?
Trước khi xin cấp phép khẩn cấp, kết quả thử nghiệm của Nanocovax ra sao? Vắc xin của Việt Nam có thể thử nghiệm giai đoạn 3 cùng lúc tại Philippines và Mozambique
Vắc xin của Việt Nam có thể thử nghiệm giai đoạn 3 cùng lúc tại Philippines và Mozambique Dự kiến thử nghiệm Nanocovax giai đoạn ba vào tuần sau
Dự kiến thử nghiệm Nanocovax giai đoạn ba vào tuần sau
 Tiến sĩ sinh học kể về quá trình sản xuất vaccine COVID-19 'made in Vietnam'
Tiến sĩ sinh học kể về quá trình sản xuất vaccine COVID-19 'made in Vietnam'
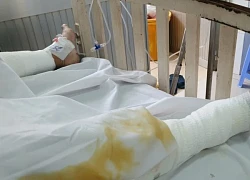 Con tạt xăng đốt mẹ: Nạn nhân bỏng nặng, giám định tâm thần con trai
Con tạt xăng đốt mẹ: Nạn nhân bỏng nặng, giám định tâm thần con trai Người đàn ông ở Bình Dương mua gần 400 tờ vé số, bất ngờ trúng thưởng 32 tỉ đồng
Người đàn ông ở Bình Dương mua gần 400 tờ vé số, bất ngờ trúng thưởng 32 tỉ đồng Phát hiện người đàn ông tử vong trong ô tô tại Hà Nội
Phát hiện người đàn ông tử vong trong ô tô tại Hà Nội Hành khách bị ép ngồi cạnh người vừa qua đời trên máy bay
Hành khách bị ép ngồi cạnh người vừa qua đời trên máy bay
 Nam sinh lớp 6 nhảy xuống sông cứu bạn: Tìm thấy 2 thi thể
Nam sinh lớp 6 nhảy xuống sông cứu bạn: Tìm thấy 2 thi thể Nữ tài xế ô tô đánh nhau với người lái xe máy sau va chạm giao thông
Nữ tài xế ô tô đánh nhau với người lái xe máy sau va chạm giao thông Vụ tai nạn giao thông khiến 3 người tử vong ở Hà Nội: Ô tô có phải đền xe máy?
Vụ tai nạn giao thông khiến 3 người tử vong ở Hà Nội: Ô tô có phải đền xe máy? Nóng: Huy Khánh và Mạc Anh Thư ly hôn sau 12 năm chung sống
Nóng: Huy Khánh và Mạc Anh Thư ly hôn sau 12 năm chung sống Bố chồng kẹt sỉ lén lút cầm sổ tiết kiệm 3 tỷ vào phòng con dâu, chưa kịp phản ứng thì mẹ chồng chạy vào tiết lộ sự thật ngã ngửa
Bố chồng kẹt sỉ lén lút cầm sổ tiết kiệm 3 tỷ vào phòng con dâu, chưa kịp phản ứng thì mẹ chồng chạy vào tiết lộ sự thật ngã ngửa Chị chồng và mẹ chồng dọa đuổi khỏi nhà, tôi nhẹ nhàng đưa ra một thứ khiến cả hai sửng sốt
Chị chồng và mẹ chồng dọa đuổi khỏi nhà, tôi nhẹ nhàng đưa ra một thứ khiến cả hai sửng sốt Thương anh rể cảnh "gà trống nuôi con", tôi biếu 500 triệu, nào ngờ anh từ chối nhận và đưa ra một nguyện vọng làm tôi điêu đứng
Thương anh rể cảnh "gà trống nuôi con", tôi biếu 500 triệu, nào ngờ anh từ chối nhận và đưa ra một nguyện vọng làm tôi điêu đứng Bố bỏ đi theo nhân tình khi mẹ tôi đang mang thai đứa con gái thứ 5, gần 20 năm sau ông quay lại với thân thể tàn tạ và muốn các con gái đón về chăm sóc
Bố bỏ đi theo nhân tình khi mẹ tôi đang mang thai đứa con gái thứ 5, gần 20 năm sau ông quay lại với thân thể tàn tạ và muốn các con gái đón về chăm sóc Người mẹ bật điều hòa giữ xác con gái trong căn chung cư suốt 6 năm
Người mẹ bật điều hòa giữ xác con gái trong căn chung cư suốt 6 năm Đêm nào ru cháu ngủ xong, mẹ chồng cũng lén rời nhà, tôi đi theo rồi bật khóc khi thấy bà ngồi giữa đám đông
Đêm nào ru cháu ngủ xong, mẹ chồng cũng lén rời nhà, tôi đi theo rồi bật khóc khi thấy bà ngồi giữa đám đông Khiến Quang Lê 'không thể nào chê', Khánh An giành á quân 'Solo cùng bolero'
Khiến Quang Lê 'không thể nào chê', Khánh An giành á quân 'Solo cùng bolero' Nữ nghệ sĩ đình đám đã bán nốt biệt thự 70 tỷ ở Việt Nam
Nữ nghệ sĩ đình đám đã bán nốt biệt thự 70 tỷ ở Việt Nam Người mẹ nguy kịch vì bị con trai tạt xăng dã man: "Tôi không bao giờ giận con..."
Người mẹ nguy kịch vì bị con trai tạt xăng dã man: "Tôi không bao giờ giận con..." Thêm 1 sao Việt tung tin nhắn, "bóc trần" mẹ bé Bắp nói chuyện trước sau bất nhất?
Thêm 1 sao Việt tung tin nhắn, "bóc trần" mẹ bé Bắp nói chuyện trước sau bất nhất? Mẹ Bắp lên tiếng về chiến dịch gây quỹ trên Give.Asia và mối quan hệ với gia đình chồng cũ
Mẹ Bắp lên tiếng về chiến dịch gây quỹ trên Give.Asia và mối quan hệ với gia đình chồng cũ Mẹ bé Bắp: 'Ba mẹ ở quê đi chợ mua đồ nhưng không ai bán, nhà có gì ăn nấy'
Mẹ bé Bắp: 'Ba mẹ ở quê đi chợ mua đồ nhưng không ai bán, nhà có gì ăn nấy' Nóng: Báo Hàn "bắt gọn" Lee Jong Suk hẹn hò Moon Ga Young, chuyện tình với IU đã toang?
Nóng: Báo Hàn "bắt gọn" Lee Jong Suk hẹn hò Moon Ga Young, chuyện tình với IU đã toang? Mỹ nhân Việt đổi đời chỉ nhờ 1 cái bĩu môi, cả body lẫn nhan sắc đều thăng hạng đỉnh cao sau 8 năm
Mỹ nhân Việt đổi đời chỉ nhờ 1 cái bĩu môi, cả body lẫn nhan sắc đều thăng hạng đỉnh cao sau 8 năm Kỳ thú hiện tượng "Thất tinh liên châu" - 7 hành tinh hội tụ hiếm gặp, ở Việt Nam quan sát được không?
Kỳ thú hiện tượng "Thất tinh liên châu" - 7 hành tinh hội tụ hiếm gặp, ở Việt Nam quan sát được không? Chồng H'Hen Niê có 1 hành động chứng minh nàng Hậu là cô gái số hưởng của Vbiz!
Chồng H'Hen Niê có 1 hành động chứng minh nàng Hậu là cô gái số hưởng của Vbiz! Sao Việt 28/2: Đan Trường thân thiết bên vợ cũ, Bảo Thanh kỷ niệm 15 năm cưới
Sao Việt 28/2: Đan Trường thân thiết bên vợ cũ, Bảo Thanh kỷ niệm 15 năm cưới