Hội đồng Đạo đức sắp họp thẩm định báo cáo vaccine Nano Covax
Sau khi nhà sản xuất và nhóm nghiên cứu vaccine Nano Covax nộp hồ sơ bổ sung về thử nghiệm lâm sàng, Hội đồng Đạo đức sẽ tổ chức thẩm định báo cáo kết quả.
Thông tin tại cuộc họp về nghiên cứu, chuyển giao công nghệ, thử nghiệm lâm sàng sản xuất thuốc, vaccine phòng Covid-19 chiều 14/9, ông Nguyễn Ngô Quang, Phó cục trưởng Cục Khoa học công nghệ và Đào tạo (Bộ Y tế), cho biết Việt Nam đang có 3 ứng viên vaccine phòng Covid-19 đang triển khai nghiên cứu thử nghiệm lâm sàng. Dự kiến, cuối năm 2021 có ít nhất có 1 loại vaccine Covid-19 được cấp phép lưu hành.
Đối với vaccine Nano Covax, loại đầu tiên được cấp phép thử nghiệm lâm sàng ở Việt Nam, ông Quang cho biết cuối giờ chiều 14/9, theo yêu cầu của Bộ Y tế, nhà sản xuất và nhóm nghiên cứu vaccine này sẽ nộp hồ sơ hoàn thiện, bổ sung về thử nghiệm lâm sàng và đăng ký vaccine.
“Dự kiến ngày mai (15/9), Hội đồng Đạo đức trong nghiên cứu y sinh học quốc gia tổ chức thẩm định báo cáo kết quả giữa kỳ thử nghiệm lâm sàng giai đoạn 3a với đầy đủ các kết quả xét nghiệm đánh giá tính sinh miễn dịch của vaccine Nano Covax và báo cáo giữa kỳ thử nghiệm lâm sàng giai đoạn 3b của vaccine này. Sau đó, Hội đồng tư vấn cấp giấy đăng ký lưu hành thuốc, nguyên liệu làm thuốc sẽ xem xét hồ sơ”, ông Nguyễn Ngô Quang cho biết.
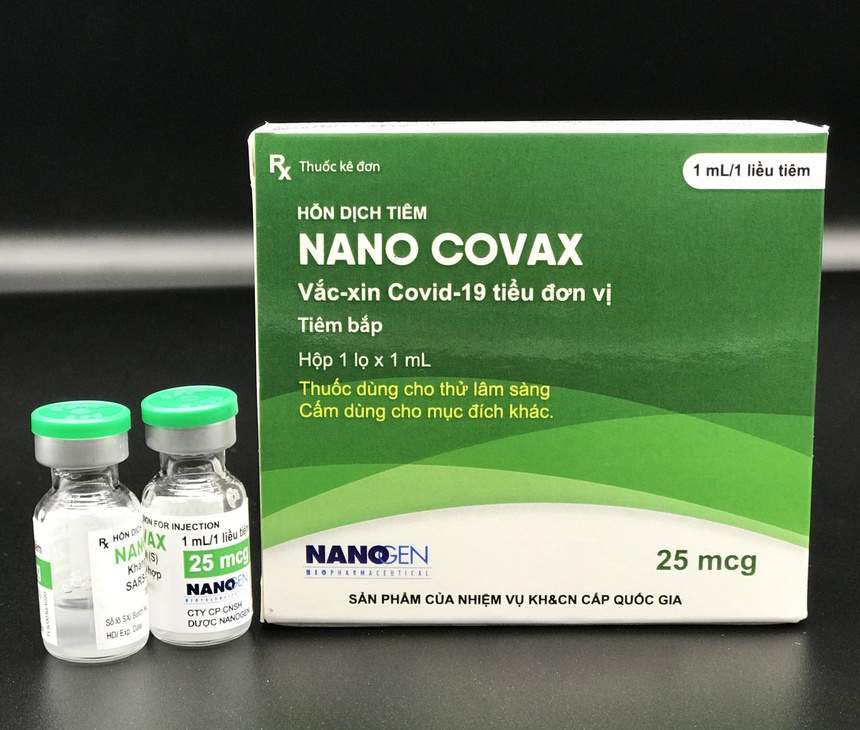
Nano Covax là 1 trong 3 ứng viên vaccine phòng Covid-19 đang nghiên cứu thử nghiệm lâm sàng ở Việt Nam. Ảnh: Nanogen.
Cũng theo lãnh đạo Cục Khoa học công nghệ và Đào tạo, ngoài việc yêu cầu nộp hồ sơ bổ sung để xem xét cấp phép khẩn cấp, Bộ Y tế cũng yêu cầu nhà sản xuất và đơn vị thử nghiệm Nano Covax tiếp tục triển khai nghiên cứu theo đúng đề cương đã được phê duyệt.
Trước đó, tại cuộc họp rà soát, đẩy nhanh tiến độ triển khai nghiên cứu phát triển, thử nghiệm lâm sàng vaccine Covid-19 trong nước hôm 10/9, Thứ trưởng Trần Văn Thuấn yêu cầu nhóm nghiên cứu Nano Covax phải hoàn thành việc nộp báo cáo bổ sung trước ngày 15/9.
Đối với vaccine Covivac , ngày 15/9, nhóm nghiên cứu sẽ tiêm thử nghiệm mũi 2 giai đoạn 2 tại Thái Bình. Tuy nhiên, ông Quang cho hay với việc đẩy mạnh tốc độ tiêm các loại vaccine phòng Covid-19 đã được cấp phép, độ bao phủ của vaccine đang nâng cao nên các nhóm nghiên cứu rất vất vả thu tuyển tình nguyện tham gia nghiên cứu.
Với vaccine ARCT-154 chuyển giao công nghệ từ Mỹ, ông Nguyễn Ngô Quang cho biết cuối tuần qua, lãnh đạo Bộ Y tế đã có văn bản cho phép triển khai cuốn chiếu giai đoạn 2 và giai đoạn 3 của vaccine này.
Sau khi họp với nhóm nghiên cứu, việc triển khai thử nghiệm lâm sàng vaccine ARCT-154 không chỉ thực hiện tại Hà Nội và TP.HCM mà sẽ được mở rộng địa bàn nghiên cứu ở nhiều tỉn như Bắc Ninh, Bắc Giang, Hải Dương, Hưng Yên, Đồng Nai, Tiền Giang, An Giang, Long An để đảm bảo tiến độ triển khai. Trước 20/12, vaccine ARCT-154 phải có đủ dữ liệu thử nghiệm lâm sàng giai đoạn 1, 2, 3.
Vaccine Nano Covax được Nanogen phát triển từ tháng 5/2020, dựa trên công nghệ protein tái tổ hợp.
Sau khi nghiệm thu kết quả thử nghiệm lâm sàng giai đoạn 1 vào tháng 8, vaccine này đang tiếp tục thu thập dữ liệu đánh giá tính an toàn, tính sinh miễn dịch và hiệu quả bảo vệ của vaccine theo đề cương nghiên cứu.
Chiến dịch tiêm chủng và xét nghiệm thần tốc ở Hà Nội .Cùng với việc gấp rút xét nghiệm sàng lọc, Hà Nội thực hiện kế hoạch tiêm mũi một vaccine Covid-19 cho toàn bộ người từ 18 tuổi trong vòng 7 ngày.
Nanogen báo cáo kết quả thử nghiệm lâm sàng Nano Covax với WHO
Đây là thông tin nằm trong hội thảo trực tuyến do WHO tổ chức giữa các học giả quốc tế về những vaccine Covid-19 triển vọng.
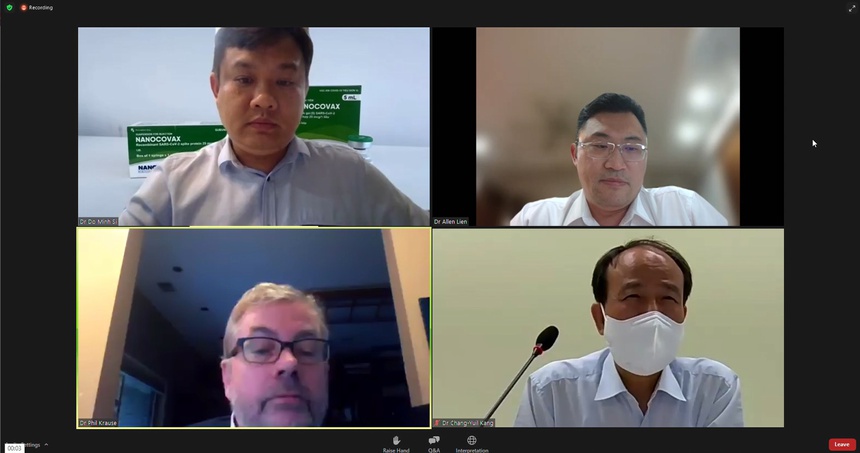
Tối 3/9 (theo giờ Việt Nam), ông Đỗ Minh Sĩ, Giám đốc Nghiên cứu và Phát triển, Công ty Cổ phần công nghệ sinh học Dược Nanogen, đã báo cáo kết quả thử nghiệm lâm sàng vaccine Covid-19 Nano Covax với Tổ chức Y tế Thế giới (WHO).
Nội dung này nằm trong hội thảo trực tuyến do WHO tổ chức, bàn luận về các vaccine Covid-19 mới với hơn 20 học giả, nhà nghiên cứu trên thế giới tham gia.
Tất cả tình nguyện viên thử nghiệm vaccine đều an toàn, khỏe mạnh
Đây là lần đầu tiên Nanogen báo cáo kết quả thử nghiệm lâm sàng với WHO. Tại buổi hội thảo, ông Đỗ Minh Sĩ cho biết Nano Covax sử dụng công nghệ protein tái tổ hợp, lấy trình tự một đoạn S protein gai trên nCoV, tích hợp nó vào một dòng tế bào động vật đang nuôi cấy để tạo ra protein của virus, rồi pha chế với các tá dược khác nhằm tạo ra vaccine.
Hiện tại, vaccine thử nghiệm lâm sàng với 4 liều là 25 mcg/ml, 50 mcg/ml, 75 mcg/ml và 100 mcg/ml.
Trong bản báo cáo với WHO và các học giả, đại diện Nanogen cho hay Nano Covax đã trải qua 3 giai đoạn thử nghiệm lâm sàng trên người. Trong đó, tổng số tình nguyện viên tham gia tiêm thử là 13.620 người, độ tuổi 18-50, sức khỏe bình thường.
Ông Đỗ Minh Sĩ (bên trái, hàng trên), đại diện Nanogen trình bày kết quả thử nghiệm lâm sàng với WHO trong hội thảo tối 3/9. Ảnh chụp từ màn hình buổi hội thảo.
Riêng pha 3, số lượng tình nguyện viên tham gia tiêm thử là 13.000 người, chia làm 2 nhóm. Nhóm 1 gồm 1.000 tình nguyện viên, tỷ lệ tiêm giả dược là 6:1 (850 người tiêm Nano Covax, 150 người tiêm giả dược). Nhóm 2 gồm 12.000 người, tỷ lệ giả dược và vaccine là 2:1 (4.000 người tiêm giả dược, 8.000 người tiêm Nano Covax).
Ông Đỗ Minh Sĩ cho hay tất cả tình nguyện viên đều có sức khỏe ổn định, an toàn, vaccine có hiệu quả.
Tạo kháng thể trung hòa virus tốt
Trong bản trình bày, do thời gian có hạn (mỗi đại diện chỉ có 3-5 phút), ông Sĩ tập trung đưa các thông tin về giai đoạn 3 thử nghiệm lâm sàng trên người, cũng là giai đoạn có số mẫu tiêm thử nhiều nhất.
Ở pha 3, kết quả Nanogen đưa ra với các học giả, chuyên gia của WHO là tỷ lệ chuyển đổi huyết thanh (hàm lượng kháng thể Anti-S IgG, hoạt tính trung hòa virus) tại ngày 42 ở người tiêm vaccine Nano Covax (liều 25 mcg) là 99,2%. Ngoài ra, 0,8% tình nguyện viên không chuyển đổi huyết thanh. Ở nhóm giả dược, 100% người tiêm thử không chuyển đổi huyết thanh.
Ngoài ra, sau 42 ngày tiêm vaccine Covid-19, tỷ lệ người sinh phản ứng với protein tái tổ hợp của nCoV là 98,8%. Trong khi đó, con số ở nhóm người tiêm giả dược thấp hơn rất nhiều - 1,6%.
Bên cạnh đó, hiệu giá kháng thể trung hòa PNRT50 tại giai đoạn 2 và 3a tại các ngày 35, 42 và 90 của Nano Covax đều cao hơn so với nhóm hồi phục.
Theo ông Sĩ, việc đánh giá này dựa theo các hướng dẫn của WHO và tài liệu y văn thế giới. Căn cứ kết quả trên, Nano Covax 25 mcg có hiệu quả bảo vệ tương đương hoặc cao hơn so với nhóm hồi phục.
Vaccine Nano Covax đang thử nghiệm lâm sàng giai đoạn 3. Ảnh: Nanogen.
Với các biến chủng mới, hiệu giá kháng thể trung hòa PRNT50 trong nhóm giả dược không thay đổi tại ngày 42. Trong khi đó, nhóm tiêm Nano Covax 25 mcg đã tăng đáng kể, trên chủng Vũ Hán có 90,2% mẫu huyết thanh có khả năng trung hòa virus sống trên nuôi cấy tế bào từ 20 lần trở lên, tỷ lệ này ở chủng Delta là 62,2%. Nếu xét khả năng trung hòa từ 10 lần trở lên thì tỷ lệ này còn cao hơn.
Như vậy, tuy trung bình nhân hiệu giá kháng thể trung hòa với chủng Ấn Độ thấp hơn chủng Vũ Hán, tỷ lệ phần trăm có đáp ứng trung hòa với chủng Ấn Độ vẫn ở mức khá cao là 62,2%.
PRT50 được coi là "tiêu chuẩn vàng" để phát hiện và đo lường các kháng thể có khả năng vô hiệu hóa virus hay không. Trong phòng thí nghiệm, máu của người tiêm vaccine sẽ được pha loãng, trộn chung với virus sống để đánh giá hiệu quả bảo vệ của vaccine.
Trước đó, ngày 1/9, Công ty Cổ phần công nghệ sinh học Dược Nanogen gửi báo cáo giải trình các yêu cầu của Bộ Y tế liên quan hồ sơ xin cấp phép khẩn vaccine Nano Covax. Các thông tin được trình bày trong hội thảo với WHO giống với bản báo cáo giải trình Nanogen gửi Bộ Y tế.
Hiện tại, Nanogen là vaccine Covid-19 nội đầu tiên của Việt Nam hoàn thành thử nghiệm lâm sàng trên người pha 3. Trước đó, Nanogen đã gửi đơn xin Bộ Y tế cấp phép khẩn vaccine Nano Covax.
Hội đồng Đạo đức đã thông qua báo cáo giữa kỳ pha 3a vaccine Nano Covax. Hội đồng Tư vấn cấp giấy đăng ký lưu hành thuốc, nguyên liệu làm thuốc (Hội đồng Cấp phép) và Hội đồng Đạo đức y sinh học quốc gia (Hội đồng Đạo đức), Bộ Y tế, đang xem xét hồ sơ của dược phẩm này trước khi cấp phép sử dụng khẩn cấp.
Nano Covax là vaccine ngừa Covid-19 do Việt Nam nghiên cứu và sản xuất. Trước khi đưa ra thử nghiệm lâm sàng, Nano Covax đã đạt tất cả chỉ tiêu tiền lâm sàng, được các cơ quan chức năng kiểm duyệt nghiêm ngặt. Mũi tiêm đầu tiên được thực hiện vào ngày 17/12/2020.
Giá bán của vaccine này chỉ khoảng 120.000 đồng/liều. Đến nay, công suất sản xuất của nhà máy ước đạt 8-12 triệu liều/tháng.
Dựa trên kế hoạch và năng lực hiện tại, công ty dự kiến đến tháng 12 năm nay có thể cung cấp đủ 50 triệu liều và 100 triệu liều vào năm 2022.
Bộ Y tế có thể cho đăng ký lưu hành vắc xin COVID-19 nội khẩn cấp trong 20 ngày 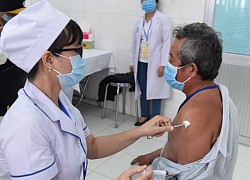 Trong hướng dẫn vừa ban hành ngày 19-8, Bộ Y tế có rất nhiều sửa đổi về quy chế đăng ký vắc xin, mở ra cơ hội đăng ký lưu hành các vắc xin ngừa COVID-19 nội địa và chuyển giao công nghệ. Tiêm Nano Covax cho người tình nguyện tham gia thử nghiệm lâm sàng giai đoạn 2 tại Long An -...
Trong hướng dẫn vừa ban hành ngày 19-8, Bộ Y tế có rất nhiều sửa đổi về quy chế đăng ký vắc xin, mở ra cơ hội đăng ký lưu hành các vắc xin ngừa COVID-19 nội địa và chuyển giao công nghệ. Tiêm Nano Covax cho người tình nguyện tham gia thử nghiệm lâm sàng giai đoạn 2 tại Long An -...
 Khoảnh khắc bé trai 3 tuổi hốt hoảng báo tin bạn đuối nước khiến triệu người thót tim01:19
Khoảnh khắc bé trai 3 tuổi hốt hoảng báo tin bạn đuối nước khiến triệu người thót tim01:19 Nghi án mẹ sát hại 2 con để trục lợi bảo hiểm: Người cô ruột hé lộ thông tin bất ngờ00:57
Nghi án mẹ sát hại 2 con để trục lợi bảo hiểm: Người cô ruột hé lộ thông tin bất ngờ00:57 Vụ 'mẹ giết con' ở Quảng Nam: Cả ngàn người tập trung theo dõi dựng lại hiện trường05:23
Vụ 'mẹ giết con' ở Quảng Nam: Cả ngàn người tập trung theo dõi dựng lại hiện trường05:23 Cảnh sát Việt Nam tìm thấy thi thể bé trai 10 tuổi trong vụ động đất ở Myanmar07:08
Cảnh sát Việt Nam tìm thấy thi thể bé trai 10 tuổi trong vụ động đất ở Myanmar07:08 Vụ tin đồn 'mẹ giết 2 con' gây xôn xao ở Quảng Nam: Người nhà nói gì?01:11
Vụ tin đồn 'mẹ giết 2 con' gây xôn xao ở Quảng Nam: Người nhà nói gì?01:11 Xe khách tông trực diện xe tải, 4 hành khách văng ra ngoài11:06
Xe khách tông trực diện xe tải, 4 hành khách văng ra ngoài11:06 Phổ Nghi 'bán đứng' cố cung, lộ bí mật tranh đấu của thái giám, khét hơn phim?05:18
Phổ Nghi 'bán đứng' cố cung, lộ bí mật tranh đấu của thái giám, khét hơn phim?05:18 4 ô tô đâm nhau trên đèo Bảo Lộc, hóa chất tràn mặt đường01:01
4 ô tô đâm nhau trên đèo Bảo Lộc, hóa chất tràn mặt đường01:01 Cháy ở chung cư HH1A Linh Đàm lúc nửa đêm, hàng trăm người hoảng loạn tháo chạy01:28
Cháy ở chung cư HH1A Linh Đàm lúc nửa đêm, hàng trăm người hoảng loạn tháo chạy01:28 Người Việt hỗ trợ nạn nhân động đất, ám ảnh cả làng bị thiêu rụi ở Myanmar01:02
Người Việt hỗ trợ nạn nhân động đất, ám ảnh cả làng bị thiêu rụi ở Myanmar01:02 Nam vương Campuchia đăng quang vài phút, lộ ảnh 'nhạy cảm', cản bước quốc tế03:06
Nam vương Campuchia đăng quang vài phút, lộ ảnh 'nhạy cảm', cản bước quốc tế03:06Tiêu điểm
Tin đang nóng
Tin mới nhất

Cưới Hỏi Trọn Gói Ngọc Huyền – 10 năm nâng tầm dịch vụ cưới hỏi miền Tây

Điểm phát cháy trong vụ hoả hoạn khiến 2 người tử vong ở Hà Nội

Chủ tịch Hà Nội chỉ đạo khẩn trương điều tra vụ cháy nhà khiến 2 người tử vong

Sạt lở nhà máy thủy điện Nậm Lúc ở Lào Cai
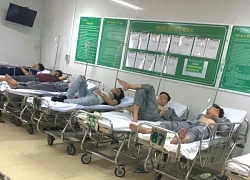
Hàng chục công nhân đi cấp cứu nghi do ngạt khí, 1 người tử vong

Xe tải lật ngang giữa đường, tài xế may mắn thoát chết

Mổ lấy thai lần 3, sản phụ ở Hải Phòng tử vong nghi sốc phản vệ

Quảng Nam: Xác minh giáo viên xách ngược trẻ 20 tháng tuổi, đánh đập dã man

Ví chứa 8.000 USD bị bỏ quên ở sân bay

Vụ DJ ở Hà Nội đánh vợ: Bạo lực nghiêm trọng, xin lỗi, hòa giải là xong chuyện?

Nhiều trưởng phòng lo mất 'quy hoạch' khi không còn cấp huyện

Thực hư vụ bé gái 13 tuổi ở Đạ Huoai nghi bị bắt cóc đưa đi TP.HCM
Có thể bạn quan tâm

Hoa hậu lên tiếng vụ sữa giả, xót vì lý do này, lộ danh tính 2 bác sĩ tiếp tay?
Sao việt
17:50:59 14/04/2025
Chu Thanh Huyền tình tứ bên Quang Hải sau sóng gió, "dát" toàn đồ hiệu sang chảnh, nhan sắc gây chú ý
Sao thể thao
17:41:55 14/04/2025
Ít thôi, nhưng đúng cái mình cần: Đây chính là cách chi tiêu kiểu mới của phụ nữ thông minh
Sáng tạo
17:37:40 14/04/2025
Bảng giá xe máy Super Cub C125 mới nhất tháng 4/2025
Xe máy
17:28:35 14/04/2025
5 mẫu xe hybrid hút khách nhất tại Việt Nam hiện nay
Ôtô
17:24:13 14/04/2025
Lấy 40 triệu đi trả nợ rồi dựng hiện trường giả bị trộm két sắt
Pháp luật
17:14:08 14/04/2025
Bài thuốc chữa bệnh từ cây đinh lăng
Sức khỏe
16:38:18 14/04/2025
Công nghệ sạch thay thế chất làm mát độc hại
Thế giới số
16:27:26 14/04/2025
Hoàng tử George thừa hưởng một khả năng đặc biệt từ Vương phi Kate khiến ai cũng phải chú ý mỗi khi xuất hiện
Netizen
15:16:26 14/04/2025
Mối quan ngại đặc biệt của các nhà thầu quân sự Mỹ giữa cuộc chiến thương mại
Thế giới
15:12:15 14/04/2025
 Lão nông thành công với mô hình nuôi cá lồng bè kết hợp du lịch
Lão nông thành công với mô hình nuôi cá lồng bè kết hợp du lịch Thanh Hóa: Nữ sinh bị hành hung, bắt quỳ gối giữa sân trường
Thanh Hóa: Nữ sinh bị hành hung, bắt quỳ gối giữa sân trường
 Nghiên cứu cắt giảm thủ tục cấp phép khẩn cấp cho vaccine Nano Covax
Nghiên cứu cắt giảm thủ tục cấp phép khẩn cấp cho vaccine Nano Covax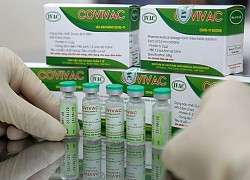 Tiến độ thử nghiệm 2 vaccine COVID-19 Nano Covax và Covivac của Việt Nam
Tiến độ thử nghiệm 2 vaccine COVID-19 Nano Covax và Covivac của Việt Nam Tiêm thử nghiệm lâm sàng vắc xin phòng COVID-19 của Việt Nam tại Hưng Yên
Tiêm thử nghiệm lâm sàng vắc xin phòng COVID-19 của Việt Nam tại Hưng Yên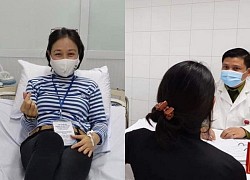 Những ngày đặc biệt của ba tình nguyện viên đầu tiên tiêm vaccine COVID-19 thử nghiệm
Những ngày đặc biệt của ba tình nguyện viên đầu tiên tiêm vaccine COVID-19 thử nghiệm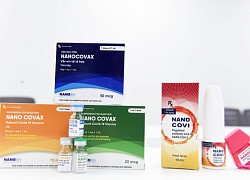 Vì sao Bộ Y tế chưa phê duyệt khẩn cấp vắc xin Nano Covax?
Vì sao Bộ Y tế chưa phê duyệt khẩn cấp vắc xin Nano Covax? Nếu được cấp phép, vắc xin Nano Covax sẽ được dùng ra sao?
Nếu được cấp phép, vắc xin Nano Covax sẽ được dùng ra sao? Dự kiến tên gọi và trung tâm hành chính của 34 tỉnh, thành sau sáp nhập
Dự kiến tên gọi và trung tâm hành chính của 34 tỉnh, thành sau sáp nhập Tạm đình chỉ nữ tiếp viên xe buýt 'tịch thu' thẻ sinh viên
Tạm đình chỉ nữ tiếp viên xe buýt 'tịch thu' thẻ sinh viên Lại xảy ra 2 trận động đất ở Kon Tum
Lại xảy ra 2 trận động đất ở Kon Tum Cháy nhà trong ngõ sâu ở Hà Nội, 2 người tử vong
Cháy nhà trong ngõ sâu ở Hà Nội, 2 người tử vong Hàng xóm kể phút gọi cửa bất thành trong vụ cháy nhà 2 người chết ở Hà Nội
Hàng xóm kể phút gọi cửa bất thành trong vụ cháy nhà 2 người chết ở Hà Nội 7 học sinh lớp 10 rủ nhau đi tắm hồ, 2 em đuối nước tử vong
7 học sinh lớp 10 rủ nhau đi tắm hồ, 2 em đuối nước tử vong Hôm nay, Tổng Bí thư, Chủ tịch Trung Quốc Tập Cận Bình thăm Việt Nam
Hôm nay, Tổng Bí thư, Chủ tịch Trung Quốc Tập Cận Bình thăm Việt Nam Đã bước đầu khống chế được cháy rừng ở Bình Liêu
Đã bước đầu khống chế được cháy rừng ở Bình Liêu Rộ tin nam rapper hot nhất nhì Vbiz hẹn hò 1 đàn chị, "bà hàng xóm" nhiều lần bắt gặp tình tứ ở nhà riêng?
Rộ tin nam rapper hot nhất nhì Vbiz hẹn hò 1 đàn chị, "bà hàng xóm" nhiều lần bắt gặp tình tứ ở nhà riêng? Sập lan can trường học, một số học sinh bị thương
Sập lan can trường học, một số học sinh bị thương 4 mỹ nhân Hoa ngữ có nụ cười "ăn tiền" nhất: Nhan sắc thì nhiều, nhưng cười đẹp thế này thì chỉ vài người có!
4 mỹ nhân Hoa ngữ có nụ cười "ăn tiền" nhất: Nhan sắc thì nhiều, nhưng cười đẹp thế này thì chỉ vài người có! Ái nữ của "ông trùm" bút bi Thiên Long lần đầu lộ diện trong đám cưới, chú rể lái siêu xe chục tỷ đến rước nàng về dinh
Ái nữ của "ông trùm" bút bi Thiên Long lần đầu lộ diện trong đám cưới, chú rể lái siêu xe chục tỷ đến rước nàng về dinh Dọn dẹp chiếc giường cũ, bất ngờ phát hiện gói vàng trị giá 500 triệu đồng
Dọn dẹp chiếc giường cũ, bất ngờ phát hiện gói vàng trị giá 500 triệu đồng Cặp đôi Chị Đẹp - Á hậu hẹn hò đồng giới nghi toang, người trong cuộc có phản ứng gây bàn tán!
Cặp đôi Chị Đẹp - Á hậu hẹn hò đồng giới nghi toang, người trong cuộc có phản ứng gây bàn tán! Sao nam 9X ngoan nhất showbiz đăng clip nhạy cảm: 3 lần ra tuyên bố nóng, càng nói càng dại
Sao nam 9X ngoan nhất showbiz đăng clip nhạy cảm: 3 lần ra tuyên bố nóng, càng nói càng dại Lộ khoảnh khắc siêu mẫu Kỳ Hân phờ phạc ngồi xe lăn trên sân pickleball sau chấn thương gãy chân gây sốc
Lộ khoảnh khắc siêu mẫu Kỳ Hân phờ phạc ngồi xe lăn trên sân pickleball sau chấn thương gãy chân gây sốc Chó pitbull cắn tử vong bé gái 7 tháng tuổi, bố mẹ chứng kiến cảnh ám ảnh: Hiện trường tìm thấy thương tâm
Chó pitbull cắn tử vong bé gái 7 tháng tuổi, bố mẹ chứng kiến cảnh ám ảnh: Hiện trường tìm thấy thương tâm Tình trẻ Diệp Lâm Anh có động thái muốn "công khai", lộ mối quan hệ với hội bạn thân Chị đẹp
Tình trẻ Diệp Lâm Anh có động thái muốn "công khai", lộ mối quan hệ với hội bạn thân Chị đẹp Chàng trai 24 tuổi đạp xe từ Hà Nội vào TP.HCM xem lễ diễu binh kỷ niệm 30/4
Chàng trai 24 tuổi đạp xe từ Hà Nội vào TP.HCM xem lễ diễu binh kỷ niệm 30/4 Kinh hoàng cảnh bác sĩ lôi con rắn dài 1,2m ra khỏi miệng một phụ nữ ở Nga
Kinh hoàng cảnh bác sĩ lôi con rắn dài 1,2m ra khỏi miệng một phụ nữ ở Nga Đang đứng tránh tàu hỏa, nam thanh niên bất ngờ bị đánh nhập viện cấp cứu
Đang đứng tránh tàu hỏa, nam thanh niên bất ngờ bị đánh nhập viện cấp cứu
 Nhã Phương phản ứng ra sao sau khi bị bóc loạt ảnh nhan sắc thật gây sốc?
Nhã Phương phản ứng ra sao sau khi bị bóc loạt ảnh nhan sắc thật gây sốc? Xem lại Tây Du Ký 50 lần tôi mới nhận ra sự thật không ngờ đằng sau: Tôn Ngộ Không bị oan suốt 39 năm
Xem lại Tây Du Ký 50 lần tôi mới nhận ra sự thật không ngờ đằng sau: Tôn Ngộ Không bị oan suốt 39 năm Chính quyền Tổng thống Trump liệt hàng nghìn người nhập cư là đã chết
Chính quyền Tổng thống Trump liệt hàng nghìn người nhập cư là đã chết Sao Việt 14/4: Hà Hồ khoe con gái, Quang Minh tình tứ bên người yêu kém 37 tuổi
Sao Việt 14/4: Hà Hồ khoe con gái, Quang Minh tình tứ bên người yêu kém 37 tuổi