Chờ kết luận thẩm định giai đoạn 3a vắc xin Covid-19 Việt Nam Nanocovax
Hôm nay, Hội đồng Đạo đức, Bộ Y tế đã mở cuộc họp thẩm định kết quả lâm sàng giữa kì giai đoạn 3a của vắc xin Covid-19 Việt Nam Nanocovax .
Công ty Cổ phần công nghệ sinh học dược Nanogen, đơn vị nghiên cứu và phát triển vắc xin Nanocovax, xác nhận thông tin trên. Tại cuộc họp, phía Nanogen đã có báo cáo về tính an toàn và tính sinh miễn dịch của vắc xin Nanocovax trong giai đoạn 3a, cũng như tiến độ thực hiện thử nghiệm lâm sàng.
Kết quả thẩm định báo cáo giữa kì đang chờ Hội đồng Đạo đức kết luận.
Phía Nanogen cũng sẽ công bố rộng rãi kết quả thử nghiệm giai đoạn 3a trong thời gian tới.
Ngày 7/8, Hội đồng Đạo đức trong nghiên cứu y sinh quốc gia cũng đã họp khẩn để nghiệm thu kết quả thử nghiệm lâm sàng giai đoạn một, đánh giá kết quả giữa kỳ thử nghiệm lâm sàng giai đoạn 2 và ghi nhận tiến độ. triển khai thử nghiệm lâm sàng giai đoạn 3a của vắc xin Nanocovax.
Vắc xin Nanocovax.
Tại cuộc họp này, Hội đồng đã thống nhất nghiệm thu kết quả thử nghiệm lâm sàng giai đoạn một vắc xin Nanocovax với dữ liệu theo dõi đến tháng thứ 6 kể từ liều tiêm đầu tiên của giai đoạn một trên 60 người tình nguyện với 3 mức liều 25 mcg, 50 mcg, 75 mcg. Bước đầu các chuyên gia đánh giá, vắc xin Nanocovax an toàn, có tính sinh miễn dịch khá tốt, đặc biệt ở hàm lượng 25mcg. Vì vậy, Hội đồng quyết định tiếp tục cho phép triển khai thử nghiệm lâm sàng giai đoạn 3 với mức liều 25mcg theo đề cương nghiên cứu đã được phê duyệt.
Ở thời điểm hiện tại, vắc xin Nanocovax đã bước sang giai đoạn thử nghiệm lâm sàng 3b. Trong thử nghiệm giai đoạn 3b, phía Bắc do Học viện Quân y làm đầu mối triển khai tiêm cho 2.000 tình nguyện viên tại Hà Nội và phối hợp với Sở Y tế tỉnh Hưng Yên tiêm cho 4.000 tình nguyện viên tại địa bàn này. Tại khu vực phía Nam, Viện Pasteur TPHCM làm đầu mối triển khai, phối hợp với ngành y tế Long An và Tiền Giang.
Trong giai đoạn 3b, nhóm nghiên cứu tiến hành tiêm thử nghiệm theo tỷ lệ 2:1, nghĩa là cứ 2 người tiêm vắc xin sẽ có một người tiêm giả dược.
Sau khoảng một tháng kể từ mũi tiêm đầu tiên, các tình nguyện viên sẽ tiếp tục được tiêm mũi thứ hai.
Nanogen đã sử dụng công nghệ protein tái tổ hợp để phát triển vắc xin Nanocovax. Đây là con đường khác với nhiều hãng dược đang làm là cấy đoạn gen virus trực tiếp vào người. Công nghệ protein tái tổ hợp cũng là một trong những hướng phát triển vắc xin Covid-19 tiên tiến nhất hiện nay.
'Không mở rộng thử nghiệm vaccine Nanocovax'
Hồi đáp đề xuất tiêm thí điểm vaccine Nanocovax của các tỉnh Khánh Hòa, Bình Dương, Bộ Y tế cho biết "chưa phê duyệt mở rộng địa bàn nghiên cứu trong giai đoạn ba".
Trong công văn hồi đáp hôm 14/8, Bộ Y tế "ủng hộ mở rộng địa bàn nghiên cứu thử nghiệm lâm sàng vaccine Nanocovax về mặt chủ trương". Các tiêu chí mở rộng là đảm bảo an toàn, khoa học, khả thi; tuân thủ đạo đức nghiên cứu; hồ sơ nghiên cứu phải được nhóm nghiên cứu xây dựng; Hội đồng Đạo đức trong nghiên cứu y sinh học quốc gia thẩm định và chấp thuận, sau đó trình Bộ Y tế phê duyệt.
Tuy nhiên, theo Bộ Y tế, phản hồi của các đơn vị thử nghiệm lâm sàng Nanocovax là tiếp tục triển khai theo đề cương nghiên cứu được phê duyệt, không mở rộng thêm địa điểm triển khai thử nghiệm lâm sàng giai đoạn ba để đảm bảo tiến độ báo cáo giữa kỳ và hoàn tất nghiên cứu so với kế hoạch được duyệt. Công ty Nanogen cũng đồng ý không mở rộng thử nghiệm do tình hình dịch bệnh phức tạp gây khó khăn trong triển khai trên diện rộng.
"Trên cơ sở ý kiến từ Công ty Nanogen và các đơn vị nghiên cứu vaccine, Bộ Y tế tạm thời chưa phê duyệt mở rộng địa bàn nghiên cứu thử nghiệm lâm sàng giai đoạn ba với vaccine Nanocovax trong giai đoạn hiện nay", công văn phúc đáp.
Bộ Y tế cũng nhấn mạnh "cấm sử dụng vaccine đang trong quá trình thử nghiệm cho mục đích thí điểm hoặc thương mại".
Trước đó, ngày 2 và 3/8, hai tỉnh Khánh Hòa và Bình Dương gửi văn bản đến Bộ Y tế, đề xuất tiêm thí điểm vaccine Nanocovax trong thời gian sớm nhất. Lãnh đạo tỉnh Khánh Hòa cho biết "muốn góp phần sớm đưa Nanocovax vào phục vụ người dân"; lãnh đạo tỉnh Bình Dương mong muốn "thúc đẩy công tác phòng, chống Covid-19, khống chế dịch, không cho bùng phát trên diện rộng".
Nanocovax là vaccine Covid-19 do Công ty Nanogen nghiên cứu, phát triển, đưa vào thử nghiệm lâm sàng từ 17/12/2020. Hai đơn vị phối hợp nghiên cứu vaccine gồm Học viện Quân y và Viện Pasteur TP HCM. Hiện vaccine thử nghiệm lâm sàng giai đoạn ba trên 13.000 người, chia làm hai giai đoạn nhỏ gồm 3a thử nghiệm trên 1.000 người, 3b thử nghiệm trên 12.000 người, sử dụng giả dược để đối chứng. Kết quả đánh giá giai đoạn 3a và giai đoạn một, hai là cơ sở để các chuyên gia xem xét đề xuất cấp phép khẩn cấp đối với Nanocovax, theo Bộ Y tế ngày 22/7.
Cuộc họp thẩm định giai đoạn 3a dự kiến diễn ra ngày 15/8, đã bị hoãn. Theo đại diện Bộ Y tế, nguyên nhân là các đơn vị nghiên cứu gồm Học viện Quân y, Viện Pasteur TP HCM và Nanogen vừa trình kết quả nghiên cứu giai đoạn 3a cho Bộ Y tế và Hội đồng đạo đức trong nghiên cứu y sinh học Quốc gia.
Các chuyên gia dự kiến tổ chức họp thẩm định trong tuần này.
Vaccine Nanocovax do công ty Nanogen nghiên cứu và sản xuất. Ảnh: Quỳnh Trần
Nhiều tỉnh xin tiêm vắc xin Nanocovax, Bộ Y tế không đồng ý 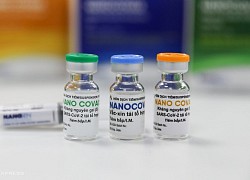 Đơn vị chủ trì nghiên cứu và nhà sản xuất đều kiến nghị không mở rộng địa bàn thử nghiệm lâm sàng giai đoạn 3 của vắc xin Nanocovax. Vì thế, Bộ chưa phê duyệt thêm địa phương tham gia nghiên cứu. Bộ Y tế vừa có công văn gửi UBND các tỉnh thành về việc xem xét bổ sung địa bàn thử...
Đơn vị chủ trì nghiên cứu và nhà sản xuất đều kiến nghị không mở rộng địa bàn thử nghiệm lâm sàng giai đoạn 3 của vắc xin Nanocovax. Vì thế, Bộ chưa phê duyệt thêm địa phương tham gia nghiên cứu. Bộ Y tế vừa có công văn gửi UBND các tỉnh thành về việc xem xét bổ sung địa bàn thử...
Tiêu điểm
Tin đang nóng
Tin mới nhất

Cha chết, con bị thương do nổ bình gas

Vợ chồng bị phóng điện khi dựng cây nêu ngày Tết

Thợ bị tàu cá đè tử vong

Ô tô cẩu làm gãy loạt cột điện xuống đường

Tàu cá bị sóng đánh chìm trên biển Lâm Đồng, một ngư dân thiệt mạng

Vé số trúng giải nhất bị rách, người phụ nữ ở TPHCM vẫn được nhận thưởng

Tai nạn xe máy tại Huế lúc rạng sáng, 2 người chết tại chỗ

Công an "thần tốc" giúp người phụ nữ lấy lại 450 triệu đồng chuyển nhầm

TPHCM bắn pháo hoa 17 điểm đêm giao thừa Tết Bính Ngọ 2026

Cảnh sát kịp thời cứu người nhảy cầu Đồng Nai

Hai học sinh mắc kẹt trên sông Ba khi thủy điện xả lũ

Virus Nipah: Lây nhiễm thấp nhưng tỉ lệ tử vong có thể lên tới 75%
Có thể bạn quan tâm

Sống chung với mẹ kế, tôi chỉ cần vắng nhà là bà sẽ ra vào kiểm tra phòng ngủ của tôi
Góc tâm tình
10:29:49 03/02/2026
Đúng ngày mai, thứ Tư 4/2/2026, 3 con giáp càng làm càng lãi, hoan hỷ đón Lộc, vận khí tươi tốt, sở hữu khối tài sản bạc tỷ
Trắc nghiệm
10:27:07 03/02/2026
Ai khiến Thúy Ngân ra nông nỗi này?
Sao việt
09:32:05 03/02/2026
Ngắm vườn Xuân lộng lẫy bên trong Kinh thành Huế
Du lịch
09:23:17 03/02/2026
Thi đấu hơn chục năm, Peanut nhận trải nghiệm "đắng lòng" sau khi giải nghệ
Mọt game
09:09:09 03/02/2026
SUV dài gần 4,8 mét, siêu tiết kiệm xăng, trang bị ấn tượng
Ôtô
08:49:18 03/02/2026
"Ngựa chiến" Yamaha Tracer 9 GT 2026 ra mắt với loạt nâng cấp đáng giá
Xe máy
08:47:20 03/02/2026
"Nam thần má lúm" Kim Seon Ho lâm cảnh bị tẩy chay dữ dội
Sao châu á
08:43:17 03/02/2026
Ông Trump định xây kho dự trữ chiến lược để đối phó với Trung Quốc
Thế giới
07:22:17 03/02/2026
 Lập tạm khu cách ly F0 tại Viện Pháp y tâm thần trung ương Biên Hòa
Lập tạm khu cách ly F0 tại Viện Pháp y tâm thần trung ương Biên Hòa UBND TP.HCM chỉ thị khẩn: Yêu cầu giãn cách triệt để tại 312 xã phường
UBND TP.HCM chỉ thị khẩn: Yêu cầu giãn cách triệt để tại 312 xã phường
 100 người đầu tiên sắp tiêm thử vaccine Covid thứ ba của Việt Nam
100 người đầu tiên sắp tiêm thử vaccine Covid thứ ba của Việt Nam Quyết tâm cao nhất để có vắc xin sản xuất trong nước vào tháng 9-2021
Quyết tâm cao nhất để có vắc xin sản xuất trong nước vào tháng 9-2021 Thủ tướng: Cấp phép vắc xin Nanocovax giảm thủ tục nhưng phải đúng quy định
Thủ tướng: Cấp phép vắc xin Nanocovax giảm thủ tục nhưng phải đúng quy định Kết quả thử nghiệm ban đầu khả quan của vắc xin Nanocovax
Kết quả thử nghiệm ban đầu khả quan của vắc xin Nanocovax Xem xét tiến tới cấp phép khẩn cấp vắc xin Covid-19 'Made in Vietnam' Nanocovax
Xem xét tiến tới cấp phép khẩn cấp vắc xin Covid-19 'Made in Vietnam' Nanocovax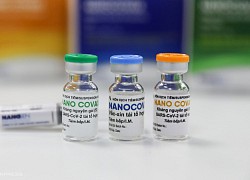 Bình Dương muốn thí điểm tiêm vaccine Nanocovax cho 200.000 người
Bình Dương muốn thí điểm tiêm vaccine Nanocovax cho 200.000 người Tháng 8, Bộ Y tế sẽ xem xét cấp phép khẩn cấp vắc xin Nanocovax
Tháng 8, Bộ Y tế sẽ xem xét cấp phép khẩn cấp vắc xin Nanocovax Việt Nam tiêm 12.000 mũi cuối giai đoạn 3 vắc xin Nanocovax
Việt Nam tiêm 12.000 mũi cuối giai đoạn 3 vắc xin Nanocovax Thủ tướng: Ưu tiên đặc biệt sản xuất vắc xin trong nước nhanh nhất
Thủ tướng: Ưu tiên đặc biệt sản xuất vắc xin trong nước nhanh nhất Xem xét cấp phép khẩn cấp vaccine Nanocovax
Xem xét cấp phép khẩn cấp vaccine Nanocovax Thủ tướng: Phải tăng tốc sản xuất vaccine Covid-19 trong nước
Thủ tướng: Phải tăng tốc sản xuất vaccine Covid-19 trong nước
 Cặp đôi chung vách ở Bắc Ninh cưới nhau, hai nhà chung rạp, rước dâu mất 10 giây
Cặp đôi chung vách ở Bắc Ninh cưới nhau, hai nhà chung rạp, rước dâu mất 10 giây Ngô Kiến Huy - Trường Giang khiến đồng đội bị "đánh đòn" không thương tiếc
Ngô Kiến Huy - Trường Giang khiến đồng đội bị "đánh đòn" không thương tiếc Đang viral màn xin lỗi độc lạ của VĐV Nhật Bản sau sự cố ném bóng trúng cô bé ngoài đường biên
Đang viral màn xin lỗi độc lạ của VĐV Nhật Bản sau sự cố ném bóng trúng cô bé ngoài đường biên Tìm thấy thi thể bé gái 12 tuổi đạp xe rời nhà từ 3 ngày trước
Tìm thấy thi thể bé gái 12 tuổi đạp xe rời nhà từ 3 ngày trước Hai người chết, ba người nhập viện sau khi uống rượu ngâm
Hai người chết, ba người nhập viện sau khi uống rượu ngâm Người phụ nữ lấy nhầm xe máy khi đi mua sắm ở Tây Ninh
Người phụ nữ lấy nhầm xe máy khi đi mua sắm ở Tây Ninh Tìm thấy thi thể người dân trượt ngã, rơi xuống nước tại khu vực Cảng cá Tân Sơn
Tìm thấy thi thể người dân trượt ngã, rơi xuống nước tại khu vực Cảng cá Tân Sơn Người mua vàng bạc lỗ rất nặng
Người mua vàng bạc lỗ rất nặng Người đàn ông mất tích khi lặn tìm máy cày ở lòng hồ thủy điện
Người đàn ông mất tích khi lặn tìm máy cày ở lòng hồ thủy điện Lắp biểu trưng hình giọt nước ở đài tưởng niệm Covid-19
Lắp biểu trưng hình giọt nước ở đài tưởng niệm Covid-19 Đồng Tháp: 2 người tử vong, 3 người nhập viện sau khi uống rượu ngâm
Đồng Tháp: 2 người tử vong, 3 người nhập viện sau khi uống rượu ngâm Top 11 phim cổ trang Trung Quốc có lượt xem nhiều nhất trên các nền tảng
Top 11 phim cổ trang Trung Quốc có lượt xem nhiều nhất trên các nền tảng Hoa hậu Đặng Thu Thảo dạo này lạ quá?
Hoa hậu Đặng Thu Thảo dạo này lạ quá? Măng tre có tác dụng gì?
Măng tre có tác dụng gì? Xe máy điện của Yamaha xuất hiện, giá không rẻ
Xe máy điện của Yamaha xuất hiện, giá không rẻ Nữ ca sĩ Gen Z khoe vòng một tại lễ trao giải Grammy có nguy cơ bị phạt
Nữ ca sĩ Gen Z khoe vòng một tại lễ trao giải Grammy có nguy cơ bị phạt Xe máy điện giá 16,8 triệu đồng ở Việt Nam động cơ 1.500W khỏe, đi 85km/lần sạc rẻ hơn Honda Vision, xe số Wave Alpha phù hợp đô thị
Xe máy điện giá 16,8 triệu đồng ở Việt Nam động cơ 1.500W khỏe, đi 85km/lần sạc rẻ hơn Honda Vision, xe số Wave Alpha phù hợp đô thị Xe tay ga 394cc, thiết kế độc lạ, giá gần 240 triệu đồng
Xe tay ga 394cc, thiết kế độc lạ, giá gần 240 triệu đồng Đừng than vãn nữa: 3 con giáp sắp bước vào thời hoàng kim, nhận vận may rực rỡ trước thềm năm mới
Đừng than vãn nữa: 3 con giáp sắp bước vào thời hoàng kim, nhận vận may rực rỡ trước thềm năm mới Đình Bắc và Văn Toàn nhắn gửi lời đặc biệt đến Hòa Minzy trước 8.000 khán giả
Đình Bắc và Văn Toàn nhắn gửi lời đặc biệt đến Hòa Minzy trước 8.000 khán giả Chồng Hàn của Từ Hy Viên tiều tụy hốc hác, quỳ rạp dưới mưa khóc thương vợ trong dịp giỗ đầu
Chồng Hàn của Từ Hy Viên tiều tụy hốc hác, quỳ rạp dưới mưa khóc thương vợ trong dịp giỗ đầu Bắt khẩn cấp tài xế đánh chết người sau va chạm xe ở Tây Ninh
Bắt khẩn cấp tài xế đánh chết người sau va chạm xe ở Tây Ninh Tử vi tuổi Dần năm 2026 chi tiết từng năm sinh
Tử vi tuổi Dần năm 2026 chi tiết từng năm sinh Tử vi tuần mới 2/2 đến 8/2/2026, 3 con giáp Lộc Lá xum xuê, người người nể phục, giàu to bất chấp khó ai sánh bằng, sống trong Phú Quý
Tử vi tuần mới 2/2 đến 8/2/2026, 3 con giáp Lộc Lá xum xuê, người người nể phục, giàu to bất chấp khó ai sánh bằng, sống trong Phú Quý Người phụ nữ Phú Thọ lấy chồng Pháp kém 6 tuổi sau 'chuyến đi định mệnh'
Người phụ nữ Phú Thọ lấy chồng Pháp kém 6 tuổi sau 'chuyến đi định mệnh' Duyên Quỳnh rơi vào vết xe đổ
Duyên Quỳnh rơi vào vết xe đổ Chồng vừa ra tay giết vợ thì bị rắn độc cắn hôn mê
Chồng vừa ra tay giết vợ thì bị rắn độc cắn hôn mê