Thủ tướng: Cấp phép vắc xin Nanocovax giảm thủ tục nhưng phải đúng quy định
Giảm bớt quy trình, thủ tục hành chính cấp phép vắc xin Nanocovax nhưng cần đảm bảo chặt chẽ theo đúng quy định và thẩm quyền, theo chỉ đạo của Thủ tướng Phạm Minh Chính.
Người dân được khám sàng lọc trước khi tiêm vắc xin Nanocovax – Ảnh: NAM TRẦN
Văn phòng Chính phủ vừa có văn bản truyền đạt chỉ đạo của Thủ tướng Phạm Minh Chính, yêu cầu bộ trưởng Bộ Y tế nghiên cứu, chỉ đạo việc cấp phép và sử dụng vắc xin Nanocovax theo hướng giảm bớt quy trình, thủ tục hành chính, nhưng phải đảm bảo chặt chẽ theo quy định và thẩm quyền.
Trước đó, Văn phòng Chính phủ nhận được văn bản ngày 1-8-2021 của GS.TS Nguyễn Gia Bình, chủ tịch Hội Hồi sức cấp cứu và chống độc Việt Nam, ủy viên hội đồng chuyên môn Ban Bảo vệ chăm sóc sức khỏe trung ương, kiến nghị về việc cấp phép sử dụng vắc xin trong tình huống khẩn cấp.
Vắc xin phòng COVID-19 Nanocovax được Công ty cổ phần Công nghệ sinh học dược Nanogen phát triển từ tháng 5-2020, dựa trên công nghệ protein tái tổ hợp. Vắc xin này đã trải qua 2 giai đoạn thử nghiệm lâm sàng, trong đó giai đoạn 1 bắt đầu từ ngày 18-12-2020 và giai đoạn 2 từ ngày 26-2-2021.
Video đang HOT
Đến nay, vắc xin Nanocovax đang nghiên cứu, thử nghiệm lâm sàng giai đoạn 3 và thực hiện đánh giá 3 yếu tố gồm tính an toàn, tính sinh miễn dịch, hiệu lực bảo vệ trên tình nguyện viên Việt Nam từ 18 tuổi trở lên.
Cụ thể, giai đoạn 3a tiêm cho 1.000 đối tượng, đánh giá giữa kỳ tính an toàn, tính sinh miễn dịch, tỉ lệ tiêm cho nhóm tình nguyện viên vắc xin trên nhóm tiêm giả dược là 6:1. Giai đoạn 3b được tiêm trên 12.000 người, tỉ lệ tiêm cho nhóm tình nguyện viên vắc xin trên nhóm tiêm giả dược là 2:1.
Dự kiến, trước ngày 15-8 sẽ có đánh giá kết quả thử nghiệm lâm sàng giai đoạn 3a. Trên cơ sở này, các cơ quan liên quan sẽ rà soát để có dữ liệu ban đầu về tính sinh miễn dịch và hiệu lực bảo vệ của vắc xin giai đoạn 3a.
Kết quả thử nghiệm ban đầu khả quan của vắc xin Nanocovax
Công ty Nanogen công bố kết quả nghiên cứu ban đầu về hiệu quả bảo vệ của vắc xin Nanonocovax dựa trên kết quả sinh miễn dịch.
Ngày 7/8, Bộ Y tế sẽ họp hội đồng thẩm định pha 2 vắc xin.
Công ty Cổ phần Công nghệ sinh học dược Nanogen vừa có công văn gửi Cục Khoa học công nghệ và Đào tạo; các Hội đồng Đạo đức của Bộ Y tế, Học viện Quân y và Viện Pasteur TPHCM về kết quả nghiên cứu Nanocovax ước tính hiệu quả bảo vệ dựa trên kết quả sinh miễn dịch.
Nghiên cứu do Viện Pasteur TPHCM thực hiện, là một phần trong nghiên cứu giai đoạn 2 vắc xin Nanocovax. Các nhà khoa học đánh giá hiệu giá kháng thể trung hòa virus (bằng PRNT50 ) của những người đã tiêm vắc xin Nanocovax so sánh với người mắc Covid-19 đã khỏi bệnh.
Đánh giá hiệu giá kháng thể trung hòa bằng PRT50 là tiêu chuẩn vàng để phát hiện và đo lường các kháng thể có khả năng vô hiệu hóa virus hay không.
Cụ thể, nhóm nghiên cứu lấy mẫu máu của 112 tình nguyện viên tại thời điểm 42 ngày sau tiêm mũi một vắc xin Nanocovax, sau đó tiến hành xét nghiệm trung hòa giảm đám hoại tử (PRNT) với virus SARS-CoV-2 sống trên nuôi cấy tế bào (PRNT 50) tại phòng xét nghiệm. Kết quả này so sánh với 16 mẫu huyết thanh của nhóm bệnh nhân Covid-19 đã khỏi bệnh (gồm một trường hợp không triệu chứng, 3 trường hợp mức độ nhẹ và 12 trường hợp có mức độ trung bình trở lên).
Kết quả nghiên cứu cho thấy, hiệu giá kháng thể trung hòa của vắc xin Nanocovax cao gấp hơn 2 lần so với nhóm khỏi bệnh, tương đương hiệu quả bảo vệ là 90% trong việc ngăn ngừa Covid-19 có triệu chứng. Sau khi tiêm vắc xin 3 tháng, hàm lượng kháng thể đặc hiệu của người tiêm Nanocovax vẫn cao hơn nhóm khỏi bệnh.
Đây là kết quả nghiên cứu ban đầu của Viện Pasteur TPHCM trên chủng Vũ Hán. Viện Vệ sinh dịch tễ Trung ương đang làm đánh giá trên biến thể Delta (Ấn Độ), bước đầu vắc xin Nanocovax có khả năng trung hòa biến chủng này.
Sáng mai (7/8), Bộ Y tế sẽ họp hội đồng thẩm định pha 2 vắc xin Nanocovax và sẽ có thông cáo chính thức.
Đến thời điểm hiện tại, Nanocovax của Công ty Nanogen là vắc xin Covid-19 đầu tiên của Việt Nam bước sang giai đoạn thử nghiệm lâm sàng thứ 3.
Công ty đang triển khai theo đề cương nghiên cứu. Cụ thể, pha 3 được thử nghiệm trên 13.000 người, chia làm 2 giai đoạn nhỏ (3a: 1.000 người và 3b: 12.000 người). Trong đó, hơn 4.000 tình nguyện viên được tiêm đủ 2 mũi.
Song song với việc xin cấp phép sử dụng khẩn cấp có điều kiện, Công ty Nanogen cũng kiến nghị Bộ Y tế, Hội đồng Đạo đức trong Nghiên cứu Y sinh học Quốc gia xem xét việc triển khai nghiên cứu giai đoạn 3c (tiêm cho khoảng 500.000 - 1.000.000 người). Đồng thời, nghiên cứu trên trẻ em từ 12 đến 18 tuổi, sau khi được cấp phép.
Bộ Y tế đề nghị Công ty Nanogen trước ngày 15/8, phải gửi báo cáo dữ liệu nghiên cứu pha 2 và bước đầu pha 3, từ đó Bộ Y tế có số liệu gửi Hội đồng đạo đức và Hội đồng cấp phép của Bộ Y tế xem xét cấp phép trong tình trạng khẩn cấp. Nếu kết quả đánh giá tốt, Bộ sẽ báo cáo các cấp theo thẩm quyền để xem xét quyết định cấp phép khẩn cấp cho Nanocovax.
Xem xét tiến tới cấp phép khẩn cấp vắc xin Covid-19 'Made in Vietnam' Nanocovax  Bộ Y tế đang xem xét tiến tới cấp phép khẩn cấp cho vắc xin Covid-19 Nanocovax. Tuy nhiên, Việt Nam chưa có nhiều kinh nghiệm trong vấn đề này. Bộ Y tế xem xét tiến tới cấp phép vắc xin Covid-19 Nanocovax sau khi rà soát các dữ liệu nghiên cứu thử nghiệm lâm sàng. ẢNH ANH VĂN Sáng 4.8, Bộ Y...
Bộ Y tế đang xem xét tiến tới cấp phép khẩn cấp cho vắc xin Covid-19 Nanocovax. Tuy nhiên, Việt Nam chưa có nhiều kinh nghiệm trong vấn đề này. Bộ Y tế xem xét tiến tới cấp phép vắc xin Covid-19 Nanocovax sau khi rà soát các dữ liệu nghiên cứu thử nghiệm lâm sàng. ẢNH ANH VĂN Sáng 4.8, Bộ Y...
 TP.HCM: Xôn xao clip nhóm người ngang nhiên chặn xe kiểm tra giấy tờ06:11
TP.HCM: Xôn xao clip nhóm người ngang nhiên chặn xe kiểm tra giấy tờ06:11 Đột ngột chuyển sai hướng, ô tô gây tai nạn liên hoàn ở Đắk Lắk00:50
Đột ngột chuyển sai hướng, ô tô gây tai nạn liên hoàn ở Đắk Lắk00:50 Tiktoker qua Singapore gặp mẹ Bắp, để lọt 1 thứ sốc chưa nói trên livestream?03:36
Tiktoker qua Singapore gặp mẹ Bắp, để lọt 1 thứ sốc chưa nói trên livestream?03:36 TP.HCM: Bảo vệ phố đi bộ Nguyễn Huệ bị người dắt chó đánh trọng thương09:39
TP.HCM: Bảo vệ phố đi bộ Nguyễn Huệ bị người dắt chó đánh trọng thương09:39 Thót tim cảnh nhấc xe bán tải cứu bé trai bị kẹt dưới gầm00:25
Thót tim cảnh nhấc xe bán tải cứu bé trai bị kẹt dưới gầm00:25 Văn Toàn 'ghé sát' môi Hoà Minzy, cảnh tượng sau đó khiến 700 nghìn người sốc03:04
Văn Toàn 'ghé sát' môi Hoà Minzy, cảnh tượng sau đó khiến 700 nghìn người sốc03:04 Vụ vạch tài sản mẹ Bắp: đội pháp lý vào cuộc, vỡ lẽ 1 thứ không ai dám lên tiếng03:08
Vụ vạch tài sản mẹ Bắp: đội pháp lý vào cuộc, vỡ lẽ 1 thứ không ai dám lên tiếng03:08 Nam thanh niên đánh tới tấp người đàn ông sau va chạm giao thông09:49
Nam thanh niên đánh tới tấp người đàn ông sau va chạm giao thông09:49 Sở Y tế Đắk Lắk điều tra kẹo rau củ Quang Linh quảng cáo, kết quả bất ngờ?03:30
Sở Y tế Đắk Lắk điều tra kẹo rau củ Quang Linh quảng cáo, kết quả bất ngờ?03:30 Vụ bắt gian ở Bắc Ninh: Chồng 'cay cú' vì 3 món lạ vợ chưa tẩu tán cùng 'baby3'04:09
Vụ bắt gian ở Bắc Ninh: Chồng 'cay cú' vì 3 món lạ vợ chưa tẩu tán cùng 'baby3'04:09 Tài xế ô tô bật đèn xi nhan, suýt gây tai nạn trên cao tốc TPHCM - Dầu Giây00:27
Tài xế ô tô bật đèn xi nhan, suýt gây tai nạn trên cao tốc TPHCM - Dầu Giây00:27Tiêu điểm
Tin đang nóng
Tin mới nhất

Điều tra nguyên nhân gây hỏa hoạn ở xưởng sơn kèm nhiều tiếng nổ lớn

Người chăn cừu tử vong, nghi bị điện giật

2 xe máy va vào nhau bốc cháy, 2 người tử vong

Xe trung chuyển va chạm xe máy làm 1 người chết

Điều tra vụ hai người đuối nước tử vong ở Củ Chi

Phát hiện thi thể 1 phụ nữ trong rẫy mía sau 3 tháng mất tích

Tìm thấy thi thể nam sinh mất tích khi tắm biển

Ba xe máy đâm nhau trên quốc lộ 21, một người tử vong

Quảng Nam: Thêm một học sinh huyện miền núi tử vong chưa rõ nguyên nhân

Những tỉnh chưa từng sáp nhập từ khi thành lập tới nay

Lái ô tô liên tục quá 4 giờ, tài xế có thể bị phạt tới 5 triệu đồng

Vụ người mặc đồ giống Đặng Lê Nguyên Vũ ẩu đả: Công an làm việc với 4 đối tượng
Có thể bạn quan tâm

UAV ồ ạt tấn công Nga trước thềm hội nghị Ukraine-Mỹ: 91 chiếc ở Moskva và 126 chiếc ở Kursk bị bắn hạ
Thống đốc khu vực Moskva, ông Andrei Vorobyov, cho biết ít nhất một người thiệt mạng và ba người bị thương. Ông Vorobyov cũng đăng một bức ảnh về một căn hộ bị hư hại với cửa sổ bị thổi bay.
Saudi Arabia chuyển mình thành trung gian hòa giải cho các cuộc khủng hoảng toàn cầu
Thế giới
19:45:57 11/03/2025
Sau buổi họp lớp, tôi nhắn tin đòi tiền còn thiếu thì bị bạn học mắng một trận tối tăm mặt mũi: Đã lật lọng còn đòi sĩ diện
Góc tâm tình
19:45:19 11/03/2025
Hoàng Đức nhận 1 tỷ đồng trước giờ lên tuyển Việt Nam
Sao thể thao
19:34:40 11/03/2025
Sau Lê Phương, thêm 1 sao nữ lên livestream ẩn ý về người diễn giả trân trong tang lễ của Quý Bình
Sao việt
19:30:40 11/03/2025
Clip: Tài xế "liều mạng" chạy ngược chiều, lạng lách tránh cảnh sát giao thông, cảnh tượng sau đó khiến ai cũng bất ngờ!
Netizen
18:22:50 11/03/2025
Kim Soo Hyun bị đào lại hình ảnh đi xem concert cùng 1 nữ idol, tiện thể xin số của gái lạ
Sao châu á
18:16:56 11/03/2025
'Bóc giá' nhẫn cưới của hot girl Việt đời đầu và chồng thiếu gia
Phong cách sao
18:14:28 11/03/2025
5 bộ trang phục thời thượng để có vòng eo nhỏ nhắn
Thời trang
18:09:42 11/03/2025
Điều gì xảy ra khi luôn uống một cốc cà phê mỗi sáng?
Sức khỏe
18:04:05 11/03/2025
 Hà Nội: Phát hiện một thi thể nam giới trong nhà hàng Vua chả cá
Hà Nội: Phát hiện một thi thể nam giới trong nhà hàng Vua chả cá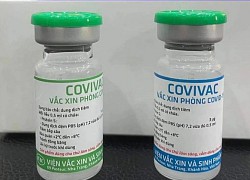 Vắc xin Covid-19 Covivac Việt Nam được đánh giá an toàn, dung nạp tốt
Vắc xin Covid-19 Covivac Việt Nam được đánh giá an toàn, dung nạp tốt
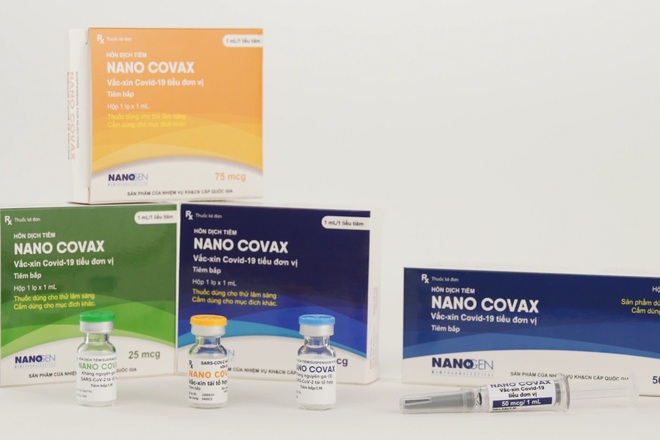
 Bình Dương muốn thí điểm tiêm vaccine Nanocovax cho 200.000 người
Bình Dương muốn thí điểm tiêm vaccine Nanocovax cho 200.000 người Tháng 8, Bộ Y tế sẽ xem xét cấp phép khẩn cấp vắc xin Nanocovax
Tháng 8, Bộ Y tế sẽ xem xét cấp phép khẩn cấp vắc xin Nanocovax Việt Nam tiêm 12.000 mũi cuối giai đoạn 3 vắc xin Nanocovax
Việt Nam tiêm 12.000 mũi cuối giai đoạn 3 vắc xin Nanocovax Thủ tướng: Ưu tiên đặc biệt sản xuất vắc xin trong nước nhanh nhất
Thủ tướng: Ưu tiên đặc biệt sản xuất vắc xin trong nước nhanh nhất Xem xét cấp phép khẩn cấp vaccine Nanocovax
Xem xét cấp phép khẩn cấp vaccine Nanocovax Thủ tướng: Phải tăng tốc sản xuất vaccine Covid-19 trong nước
Thủ tướng: Phải tăng tốc sản xuất vaccine Covid-19 trong nước Nữ tài xế đạp nhầm chân ga tông chết chủ tiệm rửa ô tô
Nữ tài xế đạp nhầm chân ga tông chết chủ tiệm rửa ô tô Hai cậu cháu tử vong cạnh chiếc xe máy
Hai cậu cháu tử vong cạnh chiếc xe máy Vợ chồng tâm thần nuôi 3 con trong căn nhà khiến ai cũng ám ảnh rùng mình
Vợ chồng tâm thần nuôi 3 con trong căn nhà khiến ai cũng ám ảnh rùng mình Thực hư vụ ông Đoàn Văn Báu gây tai nạn giao thông rồi 'chối bỏ trách nhiệm'
Thực hư vụ ông Đoàn Văn Báu gây tai nạn giao thông rồi 'chối bỏ trách nhiệm' Thuyền chở 1,5 tấn cá trích bị sóng đánh lật úp khi vào gần bờ
Thuyền chở 1,5 tấn cá trích bị sóng đánh lật úp khi vào gần bờ Bắc Giang: Hai cháu bé đuối nước thương tâm
Bắc Giang: Hai cháu bé đuối nước thương tâm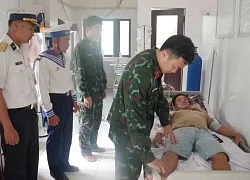 Cấp cứu một ngư dân bị cá biển có độc đâm vào chân tại Trường Sa
Cấp cứu một ngư dân bị cá biển có độc đâm vào chân tại Trường Sa
 Lê Phương gây hoang mang khi đăng status sau tang lễ Quý Bình, nhiều nghệ sĩ vào bình luận ẩn ý
Lê Phương gây hoang mang khi đăng status sau tang lễ Quý Bình, nhiều nghệ sĩ vào bình luận ẩn ý
 NÓNG: Lộ ảnh Kim Soo Hyun hôn má Kim Sae Ron và tin nhắn van xin thống khổ gây sốc của cố diễn viên
NÓNG: Lộ ảnh Kim Soo Hyun hôn má Kim Sae Ron và tin nhắn van xin thống khổ gây sốc của cố diễn viên
 Lê Phương và vợ doanh nhân của cố nghệ sĩ Quý Bình có mối quan hệ thế nào?
Lê Phương và vợ doanh nhân của cố nghệ sĩ Quý Bình có mối quan hệ thế nào? Phóng to hết cỡ bức ảnh chồng và con gái trong phòng ngủ, vợ đau lòng nhìn thứ anh cầm trên tay
Phóng to hết cỡ bức ảnh chồng và con gái trong phòng ngủ, vợ đau lòng nhìn thứ anh cầm trên tay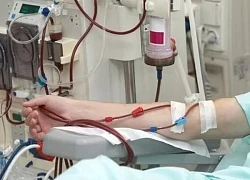 Chảy máu vùng miệng không ngừng, cô gái trẻ được chẩn đoán suy thận giai đoạn cuối
Chảy máu vùng miệng không ngừng, cô gái trẻ được chẩn đoán suy thận giai đoạn cuối Lê Phương chia sẻ ẩn ý sau tang lễ Quý Bình, netizen nghi ngờ liên quan đến vợ của cố nghệ sĩ
Lê Phương chia sẻ ẩn ý sau tang lễ Quý Bình, netizen nghi ngờ liên quan đến vợ của cố nghệ sĩ Drama dồn dập: "Ông hoàng" Châu Kiệt Luân đánh bài thua hơn 3.500 tỷ, phải thế chấp 3 biệt thự và 1 máy bay riêng?
Drama dồn dập: "Ông hoàng" Châu Kiệt Luân đánh bài thua hơn 3.500 tỷ, phải thế chấp 3 biệt thự và 1 máy bay riêng?
 Bị chỉ trích "khóc không có giọt nước mắt" trong đám tang Quý Bình, một nữ nghệ sĩ lên tiếng
Bị chỉ trích "khóc không có giọt nước mắt" trong đám tang Quý Bình, một nữ nghệ sĩ lên tiếng
 Nóng: Kim Soo Hyun trực tiếp lên tiếng về tin hẹn hò Kim Sae Ron 15 tuổi, quấy rối cố diễn viên
Nóng: Kim Soo Hyun trực tiếp lên tiếng về tin hẹn hò Kim Sae Ron 15 tuổi, quấy rối cố diễn viên 'Mỹ nhân phim hành động' Phi Ngọc Ánh mắc ung thư
'Mỹ nhân phim hành động' Phi Ngọc Ánh mắc ung thư
 Nguyễn Đình Như Vân đăng quang Miss Global, BTC xin lỗi vì ồn ào 'đường lưỡi bò'
Nguyễn Đình Như Vân đăng quang Miss Global, BTC xin lỗi vì ồn ào 'đường lưỡi bò' Viên Minh hiếm hoi tung ảnh hạnh phúc bên Công Phượng và cậu quý tử, nhan sắc tiểu thư trâm anh thế phiệt gây chú ý
Viên Minh hiếm hoi tung ảnh hạnh phúc bên Công Phượng và cậu quý tử, nhan sắc tiểu thư trâm anh thế phiệt gây chú ý