Pfizer/BioNTech trình dữ liệu xin cấp phép tiêm chủng trẻ em từ 5-11 tuổi tại Mỹ
Các hãng dược phẩm Pfizer của Mỹ và BioNTech của Đức ngày 28/9 thông báo đã bắt đầu đệ trình dữ liệu lên Cơ quan Quản lý Thực phẩm và Dược phẩm Mỹ (FDA) để xin cấp phép tiêm chủng vaccine ngừa COVID-19 của các hãng này cho trẻ em từ 5-11 tuổi.
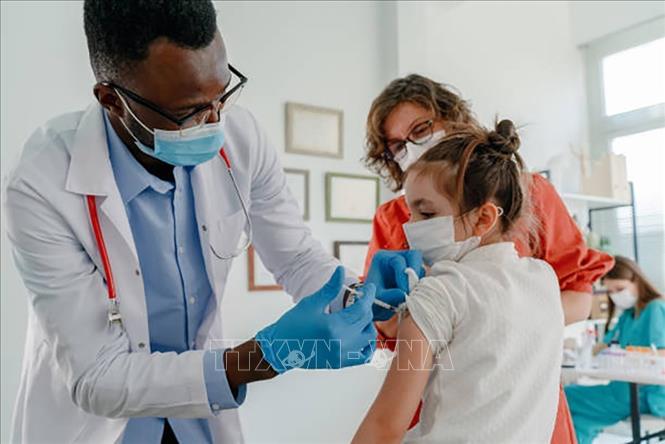
Nhân viên y tế tiêm vaccine ngừa COVID-19 cho trẻ em tại Los Angeles, California (Mỹ), ngày 8/9/2021. Ảnh: Getty Images/TTXVN
Theo phóng viên TTXVN tại Washington, thông báo của 2 hãng dược phẩm cho khẳng định “những dữ liệu đã được chia sẻ với FDA để cơ quan này xem xét bước đầu”. Dự kiến đơn chính thức xin cấp giấy phép sử dụng khẩn cấp (EUA) đối với vaccine ngừa COVID-19 cho trẻ em 5-12 tuổi sẽ được đệ trình trong những tuần tới. Cũng theo thông báo, đơn xin cấp phép tương tự sẽ được đệ trình tới Cơ quan quản lý dược phẩm châu Âu (EMA) và các cơ quan khác.
Thông tin trên được đưa ra 1 tuần sau khi Pfizer/BioNTech thông cáo những kết quả khả quan từ một thử nghiệm lâm sàng toàn cầu cho thấy vaccine ngừa COVID-19 của họ an toàn và tạo ra phản ứng mạnh với những kháng thể trung hòa, qua đó giúp ngăn chặn virus SARS-CoV-2 xâm nhập tế bào.
Video đang HOT
Trong thử nghiệm này, trẻ em từ 5-11 tuổi được áp dụng cơ chế tiêm 2 liều 10 microgam, so với 30 microgam đối với các nhóm tuổi lớn hơn. Các mũi tiêm cách nhau 21 ngày. FDA trước đây đã lưu ý rằng khi việc đệ trình chính thức được hoàn tất, cơ quan này sẽ hoàn thành việc xem xét “có thể trong vài tuần thay vì trong vài tháng”.
Vaccine ngừa COVID-19 của Pfizer/BioNTech đã được cấp phép sử dụng đầy đủ tại Mỹ hồi tháng 8, do đó về mặt kỹ thuật, vaccine này sẽ có sẵn cho trẻ em nếu được bác sĩ kê đơn, tuy nhiên, nhà chức trách Mỹ đã cảnh báo cần có dữ liệu an toàn để cho phép.
Hiện Pfizer/BioNTech cũng đang thử nghiệm vacine ngừa COVID-19 với trẻ sơ sinh từ 6 tháng đến 2 tuổi và trẻ em từ 2-5 tuổi. Dữ liệu ban đầu đối với các nhóm này có thể được đưa ra ngay sau quý 4/2021.
Nhật Bản nới lỏng quy định cách ly đối với khách nhập cảnh đã tiêm vaccine
Chính phủ Nhật Bản ngày 27/9 cho biết kể từ ngày 1/10 tới, nước này sẽ nới lỏng các quy định về cách ly đối với những khách nhập cảnh đã tiêm ngừa COVID-19.

Hành khách tại sân bay Haneda ở Tokyo, Nhật Bản. Ảnh tư liệu: AFP/TTXVN
Quyết định trên được đưa ra trong bối cảnh Nhật Bản đang lên kế hoạch khởi động lại du lịch quốc tế. Phát biểu trong cuộc họp báo, Chánh Văn phòng Nội các Nhật Bản Katsunobu Kato cho biết các trường hợp đã được tiêm phòng COVID-19 khi nhập cảnh Nhật Bản chỉ cần cách ly tại nhà trong 10 ngày - giảm 4 ngày so với quy định trước đó. Sau khi hết thời hạn cách ly, những người đã được tiêm phòng đầy đủ có thể tự do đi lại trong lãnh thổ Nhật Bản nếu họ có xét nghiệm âm tính với virus SARS-CoV-2. Tuy nhiên, quy định nới lỏng này chỉ được áp dụng đối với các trường hợp đã tiêm vaccine ngừa COVID-19 của các hãng Pfizer/BioNTech, Moderna và AstraZeneca.
Trong khi đó, Chính phủ Hàn Quốc đang phẩn bổ ngân sách 36,2 tỷ won (tương đương 30,8 triệu USD) để mua thuốc điều trị COVID-19 dạng uống, đồng thời tiếp tục thảo luận với một số hãng dược trên thế giới để ký hợp đồng đặt mua trước loại thuốc này.
Theo phóng viên TTXVN tại Seoul, các hãng dược của nước này cũng đang phát triển 11 loại thuốc trị COVID-19 dạng uống, song vẫn sẽ mất nhiều thời gian trước khi thuốc có thể chính thức được tung ra thị trường. Chi phí điều trị nếu dùng thuốc dạng uống được ước tính lên tới hơn 900.000 won (hơn 765 USD). Chính phủ dự định chi trả toàn bộ chi phí này cho người bệnh.
Việc phát triển thành công thuốc điều trị COVID-19 dạng uống đang được kỳ vọng là điều kiện cần thiết để đưa cuộc sống sinh hoạt hàng ngày của người dân trở lại bình thường, giảm lo lắng về dịch bệnh, giúp người bệnh dễ dàng điều trị tại nhà.
Hiện 3 hãng dược đi đầu trong phát triển thuốc điều trị COVID-19 dạng uống là MSD và Pfizer (Mỹ), Roche (Thụy Sĩ), đang tiến hành thử nghiệm lâm sàng giai đoạn ba. Kết quả thử nghiệm tạm thời cho thấy thuốc điều trị COVID-19 giúp ngăn tình trạng bệnh tiến triển nặng và rút ngắn thời gian điều trị, song vẫn chưa có báo cáo nào về tính an toàn.
Theo phóng viên TTXVN tại Sydney, vào cuối tuần này, Chính phủ Australia sẽ nhận được khuyến nghị của Cơ quan quản lý sản phẩm điều trị (TGA) về việc có nên công nhận vaccine phòng COVID-19 sản xuất tại Trung Quốc và Ấn Độ hay không.
Hiện TGA mới chỉ công nhận các vaccine được sản xuất tại châu Âu, Mỹ và Australia, bao gồm Pfizer, Johnson & Johnson, Moderna và AstraZeneca. Giám đốc TGA - Giáo sư John Skerritt cho biết cơ quan này đang nỗ lực đánh giá các loại vaccine được sản xuất ở nước ngoài, nhưng thông tin về vaccine của Ấn Độ và Trung Quốc còn khá ít so với các loại vaccine mà châu Âu, Bắc Mỹ và Australia đã chấp thuận. TGA đang liên hệ với các cơ quan có thẩm quyền của hai nước này để có thêm thông tin cần thiết.
Chính quyền bang New South Wales của Australia mới đây đã thông báo sẽ đón nhận 500 sinh viên quốc tế trên hai chuyến bay thuê bao vào tháng 12 tới. Để đủ điều kiện tham gia chương trình, các sinh viên này phải được tiêm chủng đầy đủ loại vaccine được TGA chấp thuận.
Anh nghiên cứu thử nghiệm tiêm kết hợp vaccine ngừa COVID-19 cho trẻ em  Anh sẽ tiến hành nghiên cứu phản ứng miễn dịch của trẻ em thông qua việc tiêm kết hợp các loại vaccine ngừa COVID-19 khác nhau nhằm tìm ra cách thức tiếp cận tốt nhất mũi 2 vaccine ngừa COVID-19 cho thanh, thiếu niên do có những báo cáo trước đó về nguy cơ nhỏ mắc viêm cơ tim. Ảnh minh họa: AFP/TTXVN...
Anh sẽ tiến hành nghiên cứu phản ứng miễn dịch của trẻ em thông qua việc tiêm kết hợp các loại vaccine ngừa COVID-19 khác nhau nhằm tìm ra cách thức tiếp cận tốt nhất mũi 2 vaccine ngừa COVID-19 cho thanh, thiếu niên do có những báo cáo trước đó về nguy cơ nhỏ mắc viêm cơ tim. Ảnh minh họa: AFP/TTXVN...
 Tang lễ Giáo hoàng Francis: Mộ phần đơn giản và thánh đường không ngủ01:37
Tang lễ Giáo hoàng Francis: Mộ phần đơn giản và thánh đường không ngủ01:37 Giáo hoàng Francis về với thánh đường Vatican lần cuối09:39
Giáo hoàng Francis về với thánh đường Vatican lần cuối09:39 Tiết lộ chiến đấu cơ tàng hình tối tân của Mỹ, uy lực số 1 thế giới17:39
Tiết lộ chiến đấu cơ tàng hình tối tân của Mỹ, uy lực số 1 thế giới17:39 Vị thế nước Đức cho an ninh châu Âu08:52
Vị thế nước Đức cho an ninh châu Âu08:52 Houthi lại bắn hạ MQ-9, Mỹ tập kích Yemen dồn dập08:25
Houthi lại bắn hạ MQ-9, Mỹ tập kích Yemen dồn dập08:25 Tổng thống Putin ca ngợi tỉ phú Musk08:48
Tổng thống Putin ca ngợi tỉ phú Musk08:48 Yêu sách mới của Israel tại Gaza08:11
Yêu sách mới của Israel tại Gaza08:11 Bác sĩ kể lại giờ phút cuối và điều tiếc nuối của Giáo hoàng Francis09:47
Bác sĩ kể lại giờ phút cuối và điều tiếc nuối của Giáo hoàng Francis09:47 Tổng thống Trump đến Rome dự tang lễ Giáo hoàng Francis09:43
Tổng thống Trump đến Rome dự tang lễ Giáo hoàng Francis09:43 Hàng hóa trên sàn Temu, Shein bớt rẻ với người Mỹ vì thuế quan08:54
Hàng hóa trên sàn Temu, Shein bớt rẻ với người Mỹ vì thuế quan08:54 Cảnh sát rô bốt AI của Thái Lan lần đầu làm nhiệm vụ07:03
Cảnh sát rô bốt AI của Thái Lan lần đầu làm nhiệm vụ07:03Tiêu điểm
Tin đang nóng
Tin mới nhất

Na Uy bước vào 'kỷ nguyên mới' về sức mạnh không quân với F-35 và tên lửa tiên tiến

Cháy nhà hàng ở Trung Quốc: Cảnh sát bắt giữ quản lý nhà hàng

Tòa châu Âu buộc Malta chấm dứt chương trình 'hộ chiếu vàng'

Tàu chiến Philippines phóng thành công tên lửa đối không Mistral 3

Nhà hàng Trung Quốc bốc cháy dữ dội, 22 người thiệt mạng

Iran công bố nguyên nhân vụ cháy nổ thảm khốc ở cảng

Pakistan cảnh báo nguy cơ chiến tranh với Ấn Độ

Chi tiêu quốc phòng Mỹ có thể đạt kỷ lục hơn 1.000 tỉ USD

Xe lao vào trại hè học sinh tại Mỹ, 4 người thiệt mạng

Tàu sân bay Mỹ cua gấp né hỏa lực Houthi làm tiêm kích F/A-18 rơi xuống biển

Mất điện tại châu Âu: ban bố tình trạng khẩn cấp, không loại trừ nguyên nhân nào

Ông Trump ký sắc lệnh kiểm soát người nhập cư tại các 'thành phố trú ẩn'
Có thể bạn quan tâm
BLACKPINK gây tiếc nuối, 1 ông lớn công khai "kiếm chuyện", Jisoo phát hành phim
Sao châu á
16:14:02 30/04/2025
Alexander-Arnold có thể 'quay xe' với Real Madrid
Sao thể thao
15:56:29 30/04/2025
10 bí quyết duy trì chế độ ăn lành mạnh trong kỳ nghỉ lễ tránh tăng cân
Sức khỏe
15:19:13 30/04/2025
Hóng: Em gái Trấn Thành hẹn hò 1 Anh Trai Say Hi?
Sao việt
15:05:54 30/04/2025
"Con của mẹ đã sống một cuộc đời đáng sống" - câu chuyện khiến triệu người bật khóc trong bộ phim đáng xem nhất thời điểm này
Phim việt
14:40:11 30/04/2025
Hòa Minzy mặc áo bà ba đeo khăn rằn quá xinh, cất giọng hát trong veo nghe là thấy mùa xuân thắng lợi!
Nhạc việt
14:34:32 30/04/2025
Các điểm du lịch Miền Tây rộn ràng đón khách dịp lễ 30-4 và 1-5
Du lịch
14:22:48 30/04/2025
Dòng iPhone 17 Pro 'lỡ hẹn' công nghệ màn hình độc quyền
Thế giới số
14:16:42 30/04/2025
Xe mới ra mắt trong tháng 4: Chuyển dịch "xanh" trên thị trường ô tô Việt
Ôtô
14:07:54 30/04/2025
Người phụ nữ dùng 'chiêu độc' để chiếm đoạt tiền tỷ của hàng trăm bị hại
Pháp luật
14:00:20 30/04/2025
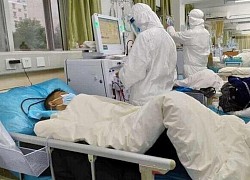 COVID-19 tới 6h sáng 29/9: Cả thế giới giảm, riêng Nga ca tử vong mới cao kỷ lục
COVID-19 tới 6h sáng 29/9: Cả thế giới giảm, riêng Nga ca tử vong mới cao kỷ lục Cuộc tình nhiều toan tính với nữ triệu phú chênh lệch 30 tuổi
Cuộc tình nhiều toan tính với nữ triệu phú chênh lệch 30 tuổi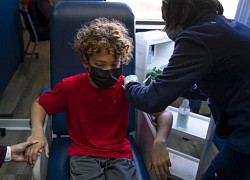 Phản ứng phụ khi tiêm vắc xin Pfizer mũi 2 cho bé trai
Phản ứng phụ khi tiêm vắc xin Pfizer mũi 2 cho bé trai Tăng cường khả năng chống chịu trước đại dịch
Tăng cường khả năng chống chịu trước đại dịch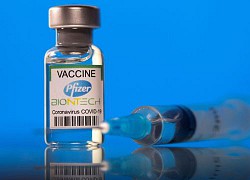 Pfizer và BioNTech hợp tác với Eurofarma phân phối vaccine tại Mỹ Latinh
Pfizer và BioNTech hợp tác với Eurofarma phân phối vaccine tại Mỹ Latinh Bộ Quốc phòng Mỹ yêu cầu các thành viên trong lực lượng tiêm phòng bắt buộc
Bộ Quốc phòng Mỹ yêu cầu các thành viên trong lực lượng tiêm phòng bắt buộc Mỹ chính thức cấp phép đầy đủ cho vắc xin Pfizer
Mỹ chính thức cấp phép đầy đủ cho vắc xin Pfizer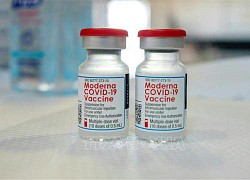 Anh cấp phép sử dụng vaccine của Moderna cho trẻ em từ 12-17 tuổi
Anh cấp phép sử dụng vaccine của Moderna cho trẻ em từ 12-17 tuổi Lo sợ biến thể Delta, nhiều người đến Mỹ để tiêm vaccine tăng cường
Lo sợ biến thể Delta, nhiều người đến Mỹ để tiêm vaccine tăng cường Rộng mở thị trường vaccine thời đại dịch
Rộng mở thị trường vaccine thời đại dịch BioNTech nói chưa cần điều chỉnh vaccine theo biến thể Delta
BioNTech nói chưa cần điều chỉnh vaccine theo biến thể Delta Mỹ sắp cấp phép đầy đủ cho vắc xin Covid-19 đầu tiên
Mỹ sắp cấp phép đầy đủ cho vắc xin Covid-19 đầu tiên Người dân nhiều nước vội vã đi tiêm chủng do lo ngại các biện pháp phòng dịch siết chặt
Người dân nhiều nước vội vã đi tiêm chủng do lo ngại các biện pháp phòng dịch siết chặt EU vượt Mỹ trong chiến dịch tiêm chủng vaccine
EU vượt Mỹ trong chiến dịch tiêm chủng vaccine Ông Trump nói ông Tập Cận Bình đã gọi điện, Trung Quốc khẳng định 'không có'
Ông Trump nói ông Tập Cận Bình đã gọi điện, Trung Quốc khẳng định 'không có'
 Sau chính sách của ông Trump, thu thuế của Mỹ tăng vọt lên mức kỷ lục
Sau chính sách của ông Trump, thu thuế của Mỹ tăng vọt lên mức kỷ lục Chuyên gia Hàn Quốc nêu lý do Nga và Triều Tiên bất ngờ cùng xác nhận việc triển khai quân ở Kursk
Chuyên gia Hàn Quốc nêu lý do Nga và Triều Tiên bất ngờ cùng xác nhận việc triển khai quân ở Kursk Tổng thống Putin lên tiếng sau khi Triều Tiên xác nhận gửi quân hỗ trợ giải phóng Kursk
Tổng thống Putin lên tiếng sau khi Triều Tiên xác nhận gửi quân hỗ trợ giải phóng Kursk Phó Tổng thống Mỹ J.D. Vance dự doán về kết cục của Ukraine khi xung đột với Nga kéo dài
Phó Tổng thống Mỹ J.D. Vance dự doán về kết cục của Ukraine khi xung đột với Nga kéo dài Phát hiện 9 đoạn Vạn Lý Trường Thành 2.000 năm tuổi ở Tây Bắc Trung Quốc
Phát hiện 9 đoạn Vạn Lý Trường Thành 2.000 năm tuổi ở Tây Bắc Trung Quốc Một loạt nước châu Âu mất điện diện rộng, ảnh hưởng hàng triệu người
Một loạt nước châu Âu mất điện diện rộng, ảnh hưởng hàng triệu người Nguyên Trưởng Công an huyện Trà Ôn báo cáo gì vụ tai nạn của con gái nghi phạm bắn người?
Nguyên Trưởng Công an huyện Trà Ôn báo cáo gì vụ tai nạn của con gái nghi phạm bắn người? Bộ Công an thẩm tra lại vụ tai nạn khiến bé gái 14 tuổi ở Vĩnh Long tử vong
Bộ Công an thẩm tra lại vụ tai nạn khiến bé gái 14 tuổi ở Vĩnh Long tử vong

 Đại tá lái Su-30MK2 nhào lộn: bắt cận visual phong độ, nhận cuộc gọi nóng
Đại tá lái Su-30MK2 nhào lộn: bắt cận visual phong độ, nhận cuộc gọi nóng Trang điểm từ 3 giờ sáng, sửa soạn để "lên sóng"
Trang điểm từ 3 giờ sáng, sửa soạn để "lên sóng" Chồng Mỹ của nữ ca sĩ nổi đình đám dặn vợ: "Nếu anh có làm sao thì để anh lại Việt Nam"
Chồng Mỹ của nữ ca sĩ nổi đình đám dặn vợ: "Nếu anh có làm sao thì để anh lại Việt Nam" Sao Việt 30/4: Tuyết Lan mang thai con đầu lòng
Sao Việt 30/4: Tuyết Lan mang thai con đầu lòng CQĐT VKSND Tối cao vào cuộc vụ tai nạn liên quan con gái nghi phạm bắn người rồi tự sát
CQĐT VKSND Tối cao vào cuộc vụ tai nạn liên quan con gái nghi phạm bắn người rồi tự sát Những khiếu nại của người cha vụ nữ sinh tử vong ở Vĩnh Long
Những khiếu nại của người cha vụ nữ sinh tử vong ở Vĩnh Long Cuộc sống viên mãn của nam nghệ sĩ Việt nổi tiếng với vợ hơn 15 tuổi, có 2 con riêng
Cuộc sống viên mãn của nam nghệ sĩ Việt nổi tiếng với vợ hơn 15 tuổi, có 2 con riêng


 Người cha đòi lại công lý cho con gái, tự tay bắn tài xế xe tải rồi tự kết thúc
Người cha đòi lại công lý cho con gái, tự tay bắn tài xế xe tải rồi tự kết thúc Nữ ca sĩ đình đám lần đầu hé lộ gia đình có 3 người mang quân hàm Đại tá
Nữ ca sĩ đình đám lần đầu hé lộ gia đình có 3 người mang quân hàm Đại tá Hoa hậu Kỳ Duyên nói 'rất buồn' và tháo gỡ video gây tranh cãi
Hoa hậu Kỳ Duyên nói 'rất buồn' và tháo gỡ video gây tranh cãi Nam danh hài ở nhà 5 tầng mặt tiền Quận 5 TP.HCM: Định xây 12 tầng nhưng bỏ vì 1 lí do
Nam danh hài ở nhà 5 tầng mặt tiền Quận 5 TP.HCM: Định xây 12 tầng nhưng bỏ vì 1 lí do