Pfizer bắt đầu thử nghiệm thuốc kháng COVID đường uống
Tập đoàn dược phẩm Mỹ Pfizer ngày 23/3 thông báo đã bắt đầu cuộc thử nghiệm giai đoạn đầu tại Mỹ liệu pháp kháng virus COVID-19 bằng đường uống.
Pfizer bắt đầu thử nghiệm thuốc kháng COVID dạng uống. Ảnh minh hoạ
Theo hãng tin Reuters, Pfizer cho biết, ứng cử viên thuốc kháng virus cho thấy hoạt động mạnh mẽ chống lại SARS-CoV-2, virus gây bệnh COVID-19, trong các nghiên cứu tại phòng thí nghiệm.
Hãng cho hay thuốc có thể được kê đơn cho những bệnh nhân có những dấu hiệu đầu tiên nhiễm virus.
Ứng cử viên thuốc kháng COVID-19 của Pfizer, được đặt tên khoa học là PF-07321332, là một chất ức chế protease, đã có hiệu quả ngăn không cho virus nhân bản trong tế bào.
Video đang HOT
Công ty cho biết các chất ức chế protease đã có hiệu quả trong điều trị các mầm bệnh virus khác như HIV, virus viêm gan C, bằng cách sử dụng riêng hoặc kết hợp với các loại thuốc kháng virus khác.
Pfizer tin rằng loại thuốc này có thể cung cấp các phương pháp điều trị dung nạp tốt chống lại COVID-19, trong bối cảnh các phương pháp điều trị hiện có trên thị trường, vốn hoạt động trên cùng một dòng, vẫn chưa báo cáo những mối lo ngại về an toàn.
Công ty cũng đang nghiên cứu một ứng cử viên kháng virus SARS-CoV-2 qua tiêm tĩnh mạch trong một thử nghiệm giai đoạn đầu trên bệnh nhân COVID-19 nhập viện.
“Cùng nhau, cả hai ứng cử viên uống và tiêm tĩnh mạch có tiềm năng tạo ra một mô hình điều trị từ đầu đến cuối, bổ sung cho hoạt động tiêm chủng trong những trường hợp bệnh vẫn xảy ra”, ông Mikael Dolsten, Giám đốc Y tế của Pfizer, cho biết trong một tuyên bố.
Ứng cử viên thuốc mới của Pfizer đứng sau hai liệu pháp kháng virus đường uống khác, đang trong giai đoạn thử nghiệm. Trong đó, phương pháp đầu tiên được phát triển bởi đối thủ Merck & Co hợp tác với Ridgeback Bio, và phương pháp thứ hai từ Roche Holding và Atea Pharmaceuticals.
Thuốc remdesivir của Gilead Sciences hiện là loại thuốc duy nhất được Cục Quản lý Thực phẩm và Dược phẩm Mỹ (FDA) chấp thuận để điều trị COVID-19.
FDA đã cấp phép khẩn cấp cho các liệu pháp tiêm tĩnh mạch từ Eli Lilly – bamlanivimab dùng riêng lẻ hoặc kết hợp với etesevimab, và một liệu pháp kết hợp từ Regeneron.
Philippines phê duyệt khẩn cấp vaccine Sputnik V
Philippines cho phép sử dụng khẩn cấp vaccine Covid-19 Sputnik V của Nga trước tình hình số ca nhiễm mới ngày càng tăng.
Sputnik V trở thành vaccine Covid-19 thứ 4 được cấp phép sử dụng khẩn cấp tại Philippines, sau Pfizer-BioNTech (Mỹ), Oxford-AstraZeneca (Anh) và Sinovac (Trung Quốc). Tuyên bố được Cơ quan Quản lý Thực phẩm và Dược phẩm (FDA) Philippines đưa ra hôm 19/3.
"Những lợi ích đã biết và tiềm năng của Sputnik V do Viện Gamaleya sản xuất nhiều hơn rủi ro", Rolando Enrique Domingo, người đứng đầu FDA Philippines, phát biểu tại cuộc họp báo. "Dữ liệu tạm thời cho thấy hai liều Sputnik V đạt hiệu quả 91,6% ở người trên 18 tuổi".
Philippines hiện là quốc gia có số ca Covid-19 cao thứ hai Đông Nam Á. Nước này đang đứng trước làn sóng lây nhiễm mới, với gần 20.000 ca nhiễm được báo cáo trong bốn ngày qua.
Thị trưởng vùng đô thị Manila hôm 8/3 ra lệnh tái phong tỏa và giờ giới nghiêm vào ban đêm trong hai tuần. Thành phố Quezon cũng bổ sung các lệnh cấm uống rượu, đóng cửa phòng gym, spa, tiệm Internet.
Một lọ vaccine Sputnik V của Nga. Ảnh: Reuters
Chính quyền Philippines đặt mục tiêu triển khai 140,5 triệu liều vaccine tới tháng 12, chủng ngừa 70 triệu người trưởng thành, hướng tới miễn dịch cộng đồng và tái mở cửa nền kinh tế. Chương trình tiêm chủng bắt đầu hôm 1/3 với 600.000 liều vaccine Sinovac ưu tiên cho nhân viên y tế tuyến đầu. Tới nay, nước này đã nhận hơn 1,1 triệu liều vaccine Sinovac và AstraZeneca.
Viện nghiên cứu Gamaleya phát triển vaccine Sputnik V dựa trên công nghệ vector, sử dụng virus vô hại đưa protein của nCoV vào tế bào người, kích thích phản ứng của hệ miễn dịch. Hai liều tiêm cách nhau 21 ngày, bảo quản ở nhiệt độ 2-8 độ C.
Nga hồi tháng 8 trở thành quốc gia đầu tiên trên thế giới cấp phép vaccine Covid-19. Tổng thống Vladimir Putin tuyên bố Sputnik V tạo hệ miễn dịch bền vững, dù chưa hoàn thành thử nghiệm Giai đoạn ba. Hai tháng sau, nước này tiếp tục cấp phép vaccine Covid-19 thứ hai có tên EpiVac Coronado do Viện virus học Vector phát triển.
Giới chức Anh khẳng định vaccine ngừa COVID-19 không gây phản ứng đông máu  Cơ quan Quản lý thuốc và các sản phẩm y tế (MHRA) của Anh ngày 18/3 thông báo các chuyên gia nước này không tìm thấy bất cứ mối liên quan trực tiếp nào giữa việc tiêm vaccine ngừa bệnh viêm đường hô hấp cấp COVID-19 với triệu chứng đông máu ở người được tiêm. Nhân viên y tế chuẩn bị tiêm vaccine...
Cơ quan Quản lý thuốc và các sản phẩm y tế (MHRA) của Anh ngày 18/3 thông báo các chuyên gia nước này không tìm thấy bất cứ mối liên quan trực tiếp nào giữa việc tiêm vaccine ngừa bệnh viêm đường hô hấp cấp COVID-19 với triệu chứng đông máu ở người được tiêm. Nhân viên y tế chuẩn bị tiêm vaccine...
 Trung Quốc tung chatbot đấu ChatGPT, cổ phiếu Phố Wall chao đảo bốc hơi 1.000 tỉ14:53
Trung Quốc tung chatbot đấu ChatGPT, cổ phiếu Phố Wall chao đảo bốc hơi 1.000 tỉ14:53 Ý tưởng gây sốc của Tổng thống Trump về Dải Gaza08:59
Ý tưởng gây sốc của Tổng thống Trump về Dải Gaza08:59 Tàu vận tải Nga cập cảng Syria, chuẩn bị cho cuộc rút quân09:12
Tàu vận tải Nga cập cảng Syria, chuẩn bị cho cuộc rút quân09:12 Hé lộ kế hoạch mới của ông Trump về xung đột Nga-Ukraine08:31
Hé lộ kế hoạch mới của ông Trump về xung đột Nga-Ukraine08:31 Ông Trump nói muốn gặp ông Putin ngay lập tức08:46
Ông Trump nói muốn gặp ông Putin ngay lập tức08:46 Tổng thống Trump lên tiếng về 'thảm kịch' hàng không ở thủ đô Washington DC10:41
Tổng thống Trump lên tiếng về 'thảm kịch' hàng không ở thủ đô Washington DC10:41 Iran công bố tên lửa đạn đạo mới nhất08:23
Iran công bố tên lửa đạn đạo mới nhất08:23 Ông Trump cấm người chuyển giới tham gia các môn thể thao dành cho nữ08:45
Ông Trump cấm người chuyển giới tham gia các môn thể thao dành cho nữ08:45 Phương Tây đang học hỏi từ chiến sự Ukraine09:10
Phương Tây đang học hỏi từ chiến sự Ukraine09:10 Hamas vừa thả 4 nữ binh sĩ Israel, sẽ nhận lại được gì?02:38
Hamas vừa thả 4 nữ binh sĩ Israel, sẽ nhận lại được gì?02:38 CIA có đánh giá mới về nguồn gốc Covid-1908:54
CIA có đánh giá mới về nguồn gốc Covid-1908:54Tiêu điểm
Tin đang nóng
Tin mới nhất

Cơ quan Cảnh sát Mỹ có lãnh đạo mới

Mỹ tìm kiếm máy bay mất tích chở 10 người tại bang Alaska

Ai Cập, Jordan rơi vào thế khó xử vì kế hoạch Gaza của Tổng thống Trump

Panama bác thông tin về thỏa thuận cho tàu Mỹ đi qua kênh đào miễn phí

Ruồi có thể lây lan vi khuẩn kháng thuốc kháng sinh trong bệnh viện

Vụ nổ súng tại Thụy Điển: Các nạn nhân mang nhiều quốc tịch khác nhau

Amazon lãi 'khủng' nhờ mùa mua sắm cuối năm ngoái

Chính phủ Mỹ 'đóng băng' hàng loạt dự án trên toàn quốc

Mỹ cắt đứt tài trợ làm tê liệt cuộc chiến chống nạn đói và sốt rét

Temu và Shein điều chỉnh chiến lược thế nào sau biện pháp thuế quan của Mỹ?

Maroc chặn khoảng 79.000 người di cư tìm cách đến châu Âu năm 2024

WFP kêu gọi quốc tế chung tay hỗ trợ lương thực cho người dân Gaza
Có thể bạn quan tâm

Mẹ ruột Dịch Dương - Nhất Dương lộ diện, chồng cũ tố Hằng Du Mục kèm bằng chứng
Netizen
17:00:49 07/02/2025
Hy Lạp ban bố tình trạng khẩn cấp tại đảo Santorini sau động đất

Năm mới đừng quên cắm ngay loại hoa tượng trưng cho sự vương giả, thành công và hạnh phúc tròn đầy này trong nhà
Trắc nghiệm
16:14:14 07/02/2025
7 mẹo vặt của mẹ khiến tôi "ngả mũ" toàn tập: Rất thiết thực lại còn tiết kiệm ngân sách
Sáng tạo
15:41:25 07/02/2025
Tel tiết lộ lý do chuyển đến Tottenham, thay vì MU
Sao thể thao
15:11:31 07/02/2025
Dậy sóng MXH: Hyun Bin lo sốt vó 1 chuyện khi Son Ye Jin mang thai
Sao châu á
15:00:04 07/02/2025
Đi về miền có nắng - Tập 19: Ông Phan đồng ý cho mẹ con Dương về nhà mình ở
Phim việt
14:56:30 07/02/2025
"Nụ hôn bạc tỷ" vượt mốc doanh thu 100 tỷ đồng
Hậu trường phim
14:50:36 07/02/2025
Tông trực diện vào ô tô bán tải, 2 người đi xe máy tử vong tại chỗ
Tin nổi bật
14:47:36 07/02/2025
 COVID-19 tại ASEAN hết 23/3: Campuchia miễn phí vaccine cho người nước ngoài; Thái Lan tăng vọt ca nhiễm
COVID-19 tại ASEAN hết 23/3: Campuchia miễn phí vaccine cho người nước ngoài; Thái Lan tăng vọt ca nhiễm Trung Quốc và Nga đạt đồng thuận chiến lược
Trung Quốc và Nga đạt đồng thuận chiến lược
 LHQ nói Covid-19 có thể thành 'bệnh theo mùa'
LHQ nói Covid-19 có thể thành 'bệnh theo mùa'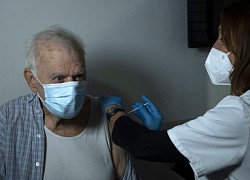 Pháp điều tra biến chủng nCoV nghi 'né xét nghiệm'
Pháp điều tra biến chủng nCoV nghi 'né xét nghiệm'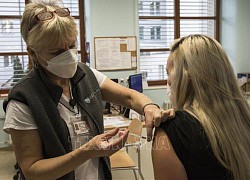 Kêu gọi EU họp thượng đỉnh về tình trạng phân phối vaccine không công bằng
Kêu gọi EU họp thượng đỉnh về tình trạng phân phối vaccine không công bằng Diễn biến COVID-19 tới 6h sáng 12/3: Thế giới trên 119 triệu ca mắc; Một số nước tạm dừng tiêm vaccine AstraZeneca
Diễn biến COVID-19 tới 6h sáng 12/3: Thế giới trên 119 triệu ca mắc; Một số nước tạm dừng tiêm vaccine AstraZeneca Bài học từ quốc gia tiêm vaccine nhanh nhất thế giới
Bài học từ quốc gia tiêm vaccine nhanh nhất thế giới Pfizer chưa tính đến bổ sung điểm sản xuất vaccine ngoài Mỹ và châu Âu
Pfizer chưa tính đến bổ sung điểm sản xuất vaccine ngoài Mỹ và châu Âu


 Chiến dịch trấn áp người nhập cư bắt đầu 'làm nóng' đường phố Mỹ
Chiến dịch trấn áp người nhập cư bắt đầu 'làm nóng' đường phố Mỹ Nga bắt đầu áp dụng chế độ trục xuất người nước ngoài vi phạm
Nga bắt đầu áp dụng chế độ trục xuất người nước ngoài vi phạm Trộm cuỗm 100.000 quả trứng giá cả tỉ đồng giữa 'lạm phát' tại Mỹ
Trộm cuỗm 100.000 quả trứng giá cả tỉ đồng giữa 'lạm phát' tại Mỹ
 Supachok rớt giá thảm hại hậu ASEAN Cup 2024
Supachok rớt giá thảm hại hậu ASEAN Cup 2024 Chấn động: Bằng chứng "nút thắt" trong vụ án của Tangmo Nida lộ diện sau 3 năm, cuộc điều tra liệu có bước ngoặt?
Chấn động: Bằng chứng "nút thắt" trong vụ án của Tangmo Nida lộ diện sau 3 năm, cuộc điều tra liệu có bước ngoặt? Công an Hải Phòng vào cuộc vụ khách đặt phòng qua mạng bị lừa hơn 1 tỷ đồng
Công an Hải Phòng vào cuộc vụ khách đặt phòng qua mạng bị lừa hơn 1 tỷ đồng Lật tẩy "tiểu phẩm" chồng cũ doanh nhân dầm mưa 30 phút, quỳ gối khóc than thương tiếc Từ Hy Viên
Lật tẩy "tiểu phẩm" chồng cũ doanh nhân dầm mưa 30 phút, quỳ gối khóc than thương tiếc Từ Hy Viên Khung hình bị chế giễu nhiều nhất hôm nay: Uông Tiểu Phi quỳ lạy giữa trời mưa
Khung hình bị chế giễu nhiều nhất hôm nay: Uông Tiểu Phi quỳ lạy giữa trời mưa Khởi tố thêm vợ chủ đậu phộng Tân Tân
Khởi tố thêm vợ chủ đậu phộng Tân Tân Hai chị em uống nhầm thuốc diệt chuột: Bé trai đã tử vong
Hai chị em uống nhầm thuốc diệt chuột: Bé trai đã tử vong Chấn động bài "phốt" 1 Anh Trai Vbiz gian lận thi cử, chính chủ đáp trả: "Đào sâu nữa mấy anti sẽ biết thêm..."
Chấn động bài "phốt" 1 Anh Trai Vbiz gian lận thi cử, chính chủ đáp trả: "Đào sâu nữa mấy anti sẽ biết thêm..." Bi kịch Vườn Sao Băng: Từ Hy Viên và 4 ngôi sao khác lần lượt qua đời khi chưa đầy 50 tuổi
Bi kịch Vườn Sao Băng: Từ Hy Viên và 4 ngôi sao khác lần lượt qua đời khi chưa đầy 50 tuổi Thi thể thiếu niên 16 tuổi bị cột vào đầu bơm nước, nổi trên kênh ở Đồng Tháp
Thi thể thiếu niên 16 tuổi bị cột vào đầu bơm nước, nổi trên kênh ở Đồng Tháp Bé gái trộm bộ trang sức trị giá 3,4 tỷ đồng của mẹ để bán với giá chỉ 200.000 đồng, mục đích phía sau gây tranh cãi
Bé gái trộm bộ trang sức trị giá 3,4 tỷ đồng của mẹ để bán với giá chỉ 200.000 đồng, mục đích phía sau gây tranh cãi Đàm Vĩnh Hưng mất hơn 4 ngón chân?
Đàm Vĩnh Hưng mất hơn 4 ngón chân? Truy tố nữ DJ ở TPHCM cầm đầu đường dây mua bán hơn 100kg ma túy
Truy tố nữ DJ ở TPHCM cầm đầu đường dây mua bán hơn 100kg ma túy Thông tin mới vụ xe tải cán qua người đi xe máy 2 lần trên Quốc lộ 51 ở Đồng Nai
Thông tin mới vụ xe tải cán qua người đi xe máy 2 lần trên Quốc lộ 51 ở Đồng Nai Rộ hình ảnh nhiều vết tiêm bất thường trên tay Từ Hy Viên khi qua đời, cái chết nghi có uẩn khúc
Rộ hình ảnh nhiều vết tiêm bất thường trên tay Từ Hy Viên khi qua đời, cái chết nghi có uẩn khúc Nghẹn ngào khoảnh khắc 2 con của Từ Hy Viên cùng cha dượng đưa tro cốt mẹ về nước
Nghẹn ngào khoảnh khắc 2 con của Từ Hy Viên cùng cha dượng đưa tro cốt mẹ về nước Nóng nhất Weibo: Mẹ Từ Hy Viên xóa ảnh chụp với con rể, hối hận vì gả con gái cho nam ca sĩ Hàn?
Nóng nhất Weibo: Mẹ Từ Hy Viên xóa ảnh chụp với con rể, hối hận vì gả con gái cho nam ca sĩ Hàn?