Mỹ cấp phép sử dụng khẩn cấp vaccine COVID-19 cải tiến của hãng Novavax
Ngày 30/8, Cơ quan Quản lý thực phẩm và dược phẩm Mỹ (FDA) đã cấp phép sử dụng khẩn cấp cho phiên bản cải tiến của vaccine ngừa COVID-19 do hãng dược Novavax bào chế.
Vaccine mới được phép dùng cho những người từ 12 tuổi trở lên và sẽ nhắm vào biến thể JN.1.
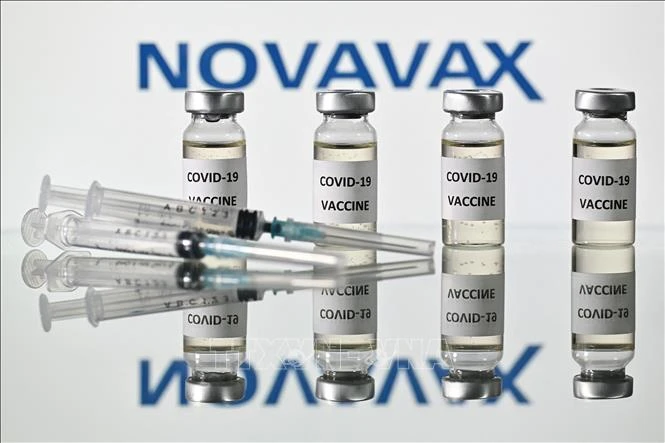
Vaccine phòng COVID-19 của công ty Novavax. Ảnh tư liệu: AFP/TTXVN
Giám đốc Trung tâm Đánh giá và nghiên cứu sinh học của FDA, ông Peter Marks cho biết: “Việc cấp phép hôm nay cung cấp thêm một lựa chọn vaccine phòng COVID-19″.
Về phần mình, công ty Novavax cho biết vaccine mới sẽ có sẵn từ đầu tuần tới. Theo Giám đốc Điều hành (CEO) John Jacobs, vaccine phiên bản nâng cấp nhắm vào ‘chủng gốc’ của các biến thể hiện đang lưu hành và đã cho thấy phản ứng chéo mạnh mẽ với các loại biến thể dòng JN.1, bao gồm KP.2.3, KP.3, KP.3.1.1 và LB.1.
Video đang HOT
Đầu tháng này, FDA đã phê duyệt vaccine COVID-19 cải tiến do các hãng dược Pfizer và Moderna sản xuất nhắm vào biến thể KP.2.
JN.1 là biến thể gây đa số ca mắc COVID-19 tại Mỹ từ đầu năm nay. Theo dữ liệu của Trung tâm Kiểm soát và phòng ngừa dịch bệnh (CDC), dù hiện nay không còn phổ biến nữa, nhưng ước tính biến thể này gây ra 0,2% các trường hợp trong khoảng thời gian hai tuần kết thúc vào ngày 31/8. Biến thể phụ KP.2 ước tính chiếm 3,1%, trong đó KP.3.1.1 hiện chiếm ưu thế ở mức 42,2%.
Tháng 6 vừa qua, cơ quan quản lý y tế đã yêu cầu các nhà sản xuất vaccine COVID-19 nhắm mục tiêu vào biến thể KP.2 để bào chế vaccine cho năm 2024-25.
Vaccine truyền thống của Novavax dựa trên protein cung cấp công nghệ vaccine thay thế cho công nghệ dựa trên RNA thông tin của Moderna, được phát triển chung bởi Pfizer/BioNTech. Novavax dự kiến nhu cầu chung về vaccine COVID-19 tại Mỹ sẽ vẫn tương tự như năm ngoái. Theo số liệu chính thức, số ca nhập viện và tử vong liên quan đến COVID-19 đã tăng trong 3 tháng qua tại Mỹ. Tuy nhiên, nhu cầu vaccine đã giảm mạnh kể từ đỉnh điểm của đại dịch.
FDA Mỹ phê duyệt Vaccine Covid-19 bản cải tiến
Cục Quản lý Thực phẩm và Dược phẩm Mỹ (FDA) vào thứ Năm (22/8) đã phê duyệt các loại vaccine COVID-19 cập nhật do Pfizer và Moderna sản xuất, nhằm phòng ngừa một biến thể mới của bệnh, kịp thời cho chiến dịch tiêm chủng mùa Thu và Đông sắp tới.
Hình ảnh tiêm vaccine tại bệnh viện Florida, Mỹ. Ảnh: Shannon Stapleton
Mẫu biến thể KP.2 đã được phát hiện vào đầu năm nay. Theo các công ty sản xuất dược phẩm, vaccine mới dự kiến sẽ có mặt trên khắp nước Mỹ trong những ngày tới.
Vào tháng 6, cơ quan quản lý y tế đã yêu cầu các nhà sản xuất vaccine có điều chỉnh đối phó với biến thể mới. Những loại vaccine mới nhất được nghiên cứu để nhắm chống lại các triệu chứng của các biến thể hiện đang lưu hành.
"Tiêm vaccin tiếp tục là nền tảng của việc phòng ngừa COVID-19," ông Peter Marks, Giám đốc Trung tâm Đánh giá và Nghiên cứu Sinh học của FDA, cho biết.
Biến thể KP.2 không còn phố biến, tuy nhiên vẫn có tính chất giống với các biến thể khác được ghi nhận tại Mỹ. Các nhà quản lý y tế hy vọng bảo vệ cộng đồng hiệu quả chống lại các biến thể lưu hành bằng cách điều chỉnh vaccine.
FDA đã cho phép sử dụng vaccine của Moderna, có thương hiệu là Spikevax, và Comirnaty, được phát triển chung bởi Pfizer và BioNTech, cho cả trẻ em từ sáu tháng tuổi trở lên và người lớn.
Các mũi tiêm cho trẻ em dưới 12 tuổi được phê duyệt cấp phép khẩn khấp.
Cơ quan quản lý chưa phê duyệt một mũi tiêm truyền thống dựa trên protein do Novavax sản xuất.
Novavax cho biết họ đang làm việc "hiệu quả" với FDA và hy vọng sẽ nhận được sự cho phép kịp thời cho mùa tiêm chủng cao điểm.
Công ty nói với truyền thông rằng họ đã sản xuất các mũi tiêm cập nhật trong suốt nhiều tháng để chờ phê duyệt. Vaccine của Novavax được phát triển trong tế bào côn trùng và mất nhiều tháng để sản xuất. Ví dụ, vào năm 2023, công ty cho biết họ cần sáu tháng để cung cấp đủ lượng vaccine ra thị trường.
Hiện tại số ca nhập viện và tử vong liên quan đến COVID-19 đã tăng trong ba tháng qua tại Mỹ. Tuy nhiên, nhu cầu tiêm vaccine đã giảm mạnh kể từ đỉnh điểm của đại dịch.
Trung Quốc thử nghiệm lâm sàng vaccine điều trị ung thư công nghệ mRNA  Trung tâm Đánh giá thuốc của Cục Quản lý sản phẩm y tế quốc gia Trung Quốc vừa chấp thuận cho thử nghiệm lâm sàng giai đoạn I đối với loại thuốc tiêm mới, là vaccine công nghệ mRNA để điều trị khối u dương tính với virus Epstein-Barr. Liệu pháp trên, do công ty dược phẩm sinh học WestGene tại Thành Đô,...
Trung tâm Đánh giá thuốc của Cục Quản lý sản phẩm y tế quốc gia Trung Quốc vừa chấp thuận cho thử nghiệm lâm sàng giai đoạn I đối với loại thuốc tiêm mới, là vaccine công nghệ mRNA để điều trị khối u dương tính với virus Epstein-Barr. Liệu pháp trên, do công ty dược phẩm sinh học WestGene tại Thành Đô,...
 Tang lễ Giáo hoàng Francis: Mộ phần đơn giản và thánh đường không ngủ01:37
Tang lễ Giáo hoàng Francis: Mộ phần đơn giản và thánh đường không ngủ01:37 Giáo hoàng Francis về với thánh đường Vatican lần cuối09:39
Giáo hoàng Francis về với thánh đường Vatican lần cuối09:39 Tiết lộ chiến đấu cơ tàng hình tối tân của Mỹ, uy lực số 1 thế giới17:39
Tiết lộ chiến đấu cơ tàng hình tối tân của Mỹ, uy lực số 1 thế giới17:39 Yêu sách mới của Israel tại Gaza08:11
Yêu sách mới của Israel tại Gaza08:11 Bác sĩ kể lại giờ phút cuối và điều tiếc nuối của Giáo hoàng Francis09:47
Bác sĩ kể lại giờ phút cuối và điều tiếc nuối của Giáo hoàng Francis09:47 Houthi lại bắn hạ MQ-9, Mỹ tập kích Yemen dồn dập08:25
Houthi lại bắn hạ MQ-9, Mỹ tập kích Yemen dồn dập08:25 Tổng thống Trump đến Rome dự tang lễ Giáo hoàng Francis09:43
Tổng thống Trump đến Rome dự tang lễ Giáo hoàng Francis09:43 Iran công bố nguyên nhân vụ cháy nổ thảm khốc ở cảng01:49
Iran công bố nguyên nhân vụ cháy nổ thảm khốc ở cảng01:49 Chiến hạm nước ngoài đầu tiên đến căn cứ Ream của Campuchia sau quá trình cải tạo08:38
Chiến hạm nước ngoài đầu tiên đến căn cứ Ream của Campuchia sau quá trình cải tạo08:38 NATO tăng mạnh hiện diện quân sự ở biển Baltic08:10
NATO tăng mạnh hiện diện quân sự ở biển Baltic08:10 Xả súng ở trường gà Ecuador, ít nhất 12 người chết01:50
Xả súng ở trường gà Ecuador, ít nhất 12 người chết01:50Tiêu điểm
Tin đang nóng
Tin mới nhất

Apple vi phạm lệnh cấm chống độc quyền App Store

Bí mật công nghệ Rekord SV-98M: Súng bắn tỉa thế hệ mới làm rúng động chiến trường

Hồng y đoàn đặt mục tiêu bầu nhanh giáo hoàng

Mỹ gửi loạt tiêm kích F-16 từ "nghĩa địa máy bay" cho Ukraine

Thỏa thuận đất hiếm Mỹ - Ukraine khó sinh ra lợi nhuận trong 10 năm tới?

Yêu cầu đặc biệt của Ukraine bị bác bỏ trong thỏa thuận khoáng sản với Mỹ

Thỏa thuận khoáng sản nâng vị thế của Ukraine trên bàn đàm phán với Nga

Phó Tổng thống Mỹ JD Vance thừa nhận xung đột Ukraine 'sẽ còn kéo dài'

Xung đột Hamas-Israel: Tàu chở viện trợ cho Gaza bị tấn công ngoài khơi Malta

Chile ban bố cảnh báo sóng thần sau động đất ở vùng cực Nam

Syria tuyên bố bảo vệ chủ quyền sau cuộc không kích của Israel gần dinh tổng thống
Australia phát hiện nguồn lây nhiễm siêu vi khuẩn nguy hiểm
Có thể bạn quan tâm

Tử vi 3 con giáp may mắn nhất thứ Bảy (3/5): Phú quý vây quanh, tiền bạc đổ về đầy túi
Trắc nghiệm
14:50:55 03/05/2025
Vợ Quang Hải ngày càng mất hút, "hết thời", mẹ chồng liền đổi thái độ?
Netizen
14:45:24 03/05/2025
Nữ sinh nói lời "gan ruột" chuyện cựu chiến binh bị đối xử vô lễ
Tin nổi bật
14:44:51 03/05/2025
'Á hậu fan Việt ghét' ứng xử dở tệ vẫn đăng quang MUP, bị cả dàn thí sinh ngó lơ
Sao châu á
14:43:02 03/05/2025
Huyền thoại váy hoa khiến ai ngắm cũng muốn điệu đà hơn trong mùa hè này
Thời trang
14:29:30 03/05/2025
Mối quan hệ thân thiết của NSND Tạ Minh Tâm và sao nữ 1 lần hát live có 20 triệu view
Sao việt
14:23:54 03/05/2025
Khởi tố nhóm "yêng hùng" mang đao kiếm đại náo trên Quốc lộ 6
Pháp luật
14:17:49 03/05/2025
"Kẻ trộm ninja" sa lưới sau hàng chục lần gây án, cảnh tượng lúc bị bắt khiến không ai nhịn được cười
Lạ vui
14:04:40 03/05/2025
One UI 8 giúp bổ sung 12 GB RAM ảo
Thế giới số
14:03:30 03/05/2025
Haval H6 2023: Giá hơn 1 tỷ, đầy ắp công nghệ thông minh
Ôtô
13:54:51 03/05/2025
 Cuba nỗ lực ngăn chặn sự lây lan của virus Oropouche
Cuba nỗ lực ngăn chặn sự lây lan của virus Oropouche LHQ tạm thời đình chỉ hoạt động cứu trợ tại Bờ Tây do giao tranh
LHQ tạm thời đình chỉ hoạt động cứu trợ tại Bờ Tây do giao tranh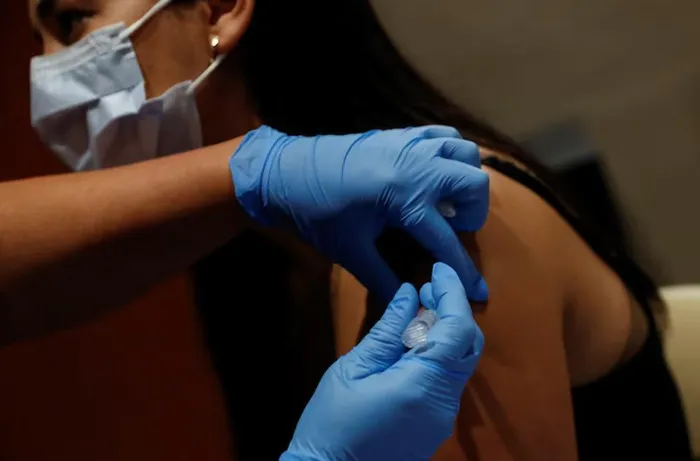
 Chính phủ Mỹ tài trợ 500 triệu USD nghiên cứu các vaccine mới ngừa COVID-19
Chính phủ Mỹ tài trợ 500 triệu USD nghiên cứu các vaccine mới ngừa COVID-19 Mỹ thu thập thông tin về sản phẩm gia vị của Ấn Độ nghi chứa chất gây ung thư
Mỹ thu thập thông tin về sản phẩm gia vị của Ấn Độ nghi chứa chất gây ung thư Làn sóng tỷ lệ sinh thấp kỷ lục càn quét loạt nước phát triển châu Á
Làn sóng tỷ lệ sinh thấp kỷ lục càn quét loạt nước phát triển châu Á Mỹ: Vaccine COVID-19 cải tiến có thể ngừa các dòng phụ mới của biến thể Omicron
Mỹ: Vaccine COVID-19 cải tiến có thể ngừa các dòng phụ mới của biến thể Omicron Novavax chấm dứt hợp đồng mua bán vaccine ngừa COVID-19 với GAVI
Novavax chấm dứt hợp đồng mua bán vaccine ngừa COVID-19 với GAVI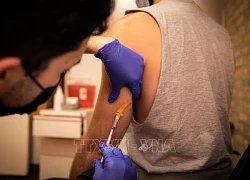 FDA Mỹ phê duyệt tiêm vaccine ACAM2000 ngừa đậu mùa khỉ cho người nguy cơ cao mắc bệnh
FDA Mỹ phê duyệt tiêm vaccine ACAM2000 ngừa đậu mùa khỉ cho người nguy cơ cao mắc bệnh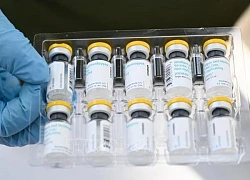 Bất bình đẳng vaccine từ giai đoạn COVID-19 lại gây tranh luận ở dịch đậu mùa khỉ
Bất bình đẳng vaccine từ giai đoạn COVID-19 lại gây tranh luận ở dịch đậu mùa khỉ EC phê duyệt sử dụng vaccine ngừa RSV của Moderna cho người trên 60 tuổi
EC phê duyệt sử dụng vaccine ngừa RSV của Moderna cho người trên 60 tuổi Hàn Quốc cảnh báo số ca mắc COVID-19 sẽ đạt đỉnh vào tháng 9 tới
Hàn Quốc cảnh báo số ca mắc COVID-19 sẽ đạt đỉnh vào tháng 9 tới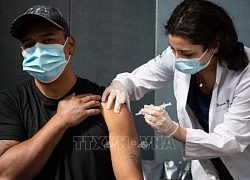 Chuyên gia Mỹ khuyến nghị các biện pháp phòng ngừa khi số ca COVID-19 tăng cao
Chuyên gia Mỹ khuyến nghị các biện pháp phòng ngừa khi số ca COVID-19 tăng cao Trung Quốc: Mỹ đã liên hệ để đàm phán thuế quan
Trung Quốc: Mỹ đã liên hệ để đàm phán thuế quan
 Quyền Tổng thống Hàn Quốc tuyên bố từ chức
Quyền Tổng thống Hàn Quốc tuyên bố từ chức Cái xác chết khô trong tủ quần áo suốt 2 năm và sự thật không ai tin
Cái xác chết khô trong tủ quần áo suốt 2 năm và sự thật không ai tin Nga tuyên bố không chấp nhận khôi phục đường biên giới năm 1991 cho Ukraine
Nga tuyên bố không chấp nhận khôi phục đường biên giới năm 1991 cho Ukraine Tổng thống Donald Trump tiết lộ các nước có thể đạt thỏa thuận thương mại
Tổng thống Donald Trump tiết lộ các nước có thể đạt thỏa thuận thương mại Chuyến tàu cao tốc tê liệt vì một con rắn
Chuyến tàu cao tốc tê liệt vì một con rắn
 VKSND Tối cao: Tài xế xe tải có lỗi trong cái chết của bé gái ở Vĩnh Long
VKSND Tối cao: Tài xế xe tải có lỗi trong cái chết của bé gái ở Vĩnh Long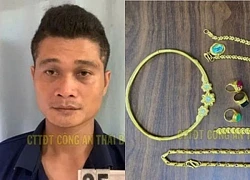 Con trai từ Bình Dương về Thái Bình trộm 39 chỉ vàng, 1.900 USD của mẹ đẻ
Con trai từ Bình Dương về Thái Bình trộm 39 chỉ vàng, 1.900 USD của mẹ đẻ Chia sẻ của nữ tiếp viên hàng không về bức ảnh "đã dùng hết may mắn trong ngày"
Chia sẻ của nữ tiếp viên hàng không về bức ảnh "đã dùng hết may mắn trong ngày" Màn so kè nhan sắc hot nhất đêm: Chu Thanh Huyền tung ảnh cùng Doãn Hải My, quan hệ thế nào sau tuyên bố "không thân"?
Màn so kè nhan sắc hot nhất đêm: Chu Thanh Huyền tung ảnh cùng Doãn Hải My, quan hệ thế nào sau tuyên bố "không thân"?



 Vụ bắn tài xế ở Vĩnh Long: clip hiện trường TX có dấu hiệu vi phạm, xử lý cán bộ
Vụ bắn tài xế ở Vĩnh Long: clip hiện trường TX có dấu hiệu vi phạm, xử lý cán bộ

 Vụ nổ súng rồi tự sát ở Vĩnh Long: Người bạn đi cùng kể lại tai nạn của con gái nghi phạm
Vụ nổ súng rồi tự sát ở Vĩnh Long: Người bạn đi cùng kể lại tai nạn của con gái nghi phạm


 Diễn biến toàn bộ vụ tai nạn làm bé gái tử vong đến việc người cha nổ súng bắn tài xế
Diễn biến toàn bộ vụ tai nạn làm bé gái tử vong đến việc người cha nổ súng bắn tài xế Thông tin gây sốc liên quan đến Tuấn Hưng và Mai Phương Thuý
Thông tin gây sốc liên quan đến Tuấn Hưng và Mai Phương Thuý Vụ phụ nữ Vĩnh Phúc bị hại: Nghi phạm chọn chết, lộ quan hệ khó ngờ với nạn nhân
Vụ phụ nữ Vĩnh Phúc bị hại: Nghi phạm chọn chết, lộ quan hệ khó ngờ với nạn nhân