Moderna hoàn tất thử nghiệm vaccine Covid-19 giai đoạn 3
Hãng dược Moderna cho biết đã hoàn thành thử nghiệm vaccine giai đoạn 3 cho 30.000 tình nguyện viên tham gia.
Quá trình nghiên cứu được theo dõi chặt chẽ để đảm bảo sự đa dạng tình nguyện viên. Theo dữ liệu của công ty, 1/5 tình nguyện viên đến từ Tây Ban Nha và 10% là người da đen. Tình nguyện viên trên 65 tuổi, đối tượng có nguy cơ cao nhiễm nCoV, chiếm 25%.
“Tôi nghĩ rằng chúng tôi đang làm khá tốt, yếu tố nhân khẩu của thử nghiệm vaccine Moderna khá đa dạng”, Larry Corey, chuyên gia virus tại Trung tâm Nghiên cứu Ung thư Fred Hutchinson, nhận định. Ông Corey đang tiến hành các thử nghiệm lâm sàng trong Chiến dịch Thần tốc – nỗ lực liên bang nhằm đẩy nhanh tiến độ phát triển vaccine.
“Chúng tôi hy vọng sẽ tiếp tục cải thiện điều này. Đây mới là thử nghiệm đầu tiên hoàn thành, chúng ta còn hai loại khác nữa. Chặng đường đến với vaccine Covid-19 chỉ mới bắt đầu”, ông Corey nói, đề cập đến hai loại vaccine khác của hai nhà nghiên cứu Pfizer và Johnson & Johnson.
Hơn một nửa số tình nguyện viên của Moderna đều là người khỏe mạnh, không dễ nhiễm nCoV. 25% khác là người cao tuổi, 17% trẻ hơn, song mắc các bệnh nền như tiểu đường hoặc béo phì, khiến họ nằm trong nhóm rủi ro cao.
Video đang HOT
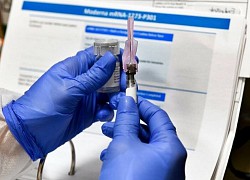
Dữ liệu đánh giá thử nghiệm vaccine của Moderna được lưu tại Trung tâm nghiên cứu Mỹ ở Hollywood, Florida. Ảnh: AFP
Tiến sĩ Stephen Hoge, chủ tịch của Moderna, cho biết chủng ngừa cho 30.000 tình nguyện viên “chỉ là cột mốc quan trọng, không phải thành tựu”. 50% trong đó đã nhận vaccine, số còn lại tiêm giả dược là nước muối sinh lý. Hai mũi tiêm cách nhau 4 tuần.
Moderna dự kiến công bố dữ liệu sơ bộ của thử nghiệm giai đoạn 3 trong tháng 11. Sau hai tháng theo dõi, công ty sẽ xác định liệu sản phẩm có đủ tiêu chuẩn đệ trình lên cơ quan quản lý để xin cấp phép hay không. Họ kỳ vọng hoàn thành toàn bộ quá trình trước Lễ Tạ ơn, ngày 26/11 năm nay.
Hiện Moderna, Pfizer và Johnson & Johnson là ba hãng dược dẫn đầu cuộc đua phát triển vaccine tại Mỹ. Moderna khởi động thử nghiệm giai đoạn 3 ngày 27/2, cùng ngày với Pfizer. Vaccine do Johnson & Johnson sản xuất bắt đầu tiêm thử ngày 23/9, song phải ngừng sau chưa đầy ba tuần vì một tình nguyện viên bị ốm. AstraZeneca, hãng dược của Anh, gặp tình trạng tương tự.
Thử nghiệm lâm sàng các loại vaccine bao gồm ba giai đoạn. Ở giai đoạn một, các nhà khoa học tiêm vaccine cho số tình nguyện viên hạn chế để kiểm tra độ an toàn và xác định liều lượng. Giai đoạn hai, thử nghiệm diễn ra trên hàng trăm người, chia thành các nhóm, chẳng hạn trẻ em, người già, để xem liệu liều tiêm có tạo ra phản ứng khác nhau ở từng đối tượng hay không. Trong thử nghiệm giai đoạn ba, các nhà nghiên cứu tiêm vaccine hoặc giả dược trên hàng chục nghìn người, chia làm hai nhóm. Tình nguyện sau đó trở về vùng dịch sinh sống nhằm so sánh tỷ lệ lây nhiễm.
Sau thử nghiệm giai đoạn ba, đơn vị nghiên cứu sẽ đệ trình dữ liệu lên cơ quan quản lý để xin cấp phép. Trong thời kỳ đại dịch, một số loại vaccine được phê duyệt khẩn cấp khi đang trong nghiên cứu giai đoạn 3.
Khi đã được cơ quan quản lý chấp thuận, các nhà nghiên cứu tiếp tục theo dõi phản ứng của nhóm tình nguyện viên nhằm tìm ra các tác dụng phụ tiềm ẩn. Đây gọi là quá trình đánh giá sau phê duyệt. Nếu vaccine được chứng minh là an toàn và hiệu quả, nhà sản xuất sẽ tiến hành phân phối hàng loạt đến các cơ sở y tế, phục vụ cho chương trình tiêm chủng.
Thông thường toàn bộ quy trình từ nghiên cứu đến cấp phép, phân phối ra thị trường của một loại vaccine mới mất ít nhất hai năm. Trong bối cảnh Covid-19 lan rộng, một số chính phủ thúc đẩy quá trình nghiên cứu cấp phép vaccine này nhanh hơn bình thường. Thậm chí Nga đã cấp phép cho hai loại vaccine Covid-19 trước khi tiến hành các giai đoạn thử nghiệm lâm sàng, dẫn đến nhiều hoài nghi của các nhà khoa học về chất lượng sản phẩm.
Đến nay 6 loại vaccine Covid-19 được phê duyệt khẩn cấp, đều thuộc về Trung Quốc và Nga. Hai “ứng viên” của Nga là Sputnik V và EpiVacCorona. Bốn loại vaccine của Trung Quốc do hãng dược nhà nước và các Viện Sinh phẩm điều chế, chủ yếu dựa trên virus bất hoạt.
5 người gặp phản ứng phụ khi tham gia thử nghiệm 2 loại vaccine Covid-19 hàng đầu tại Mỹ
Cả 5 người tham gia thử nghiệm cho biết họ bị sốt cao, đau nhức cơ thể, đau đầu, kiệt sức suốt cả ngày và các triệu chứng khác sau khi tiêm.
5 trong số những tình nguyện viên người Mỹ tham gia thử nghiệm giai đoạn cuối loại vaccine ngừa Covid-19 tiềm năng của hai hãng Moderna và Pfizer đã bắt gặp các phản ứng phụ.
Trả lời phỏng vấn hãng tin CNBC ngày 1/10, cả năm người tham gia thử nghiệm cho biết họ bị sốt cao, đau nhức cơ thể, đau đầu, kiệt sức suốt cả ngày và các triệu chứng khác sau khi tiêm.
Trong số đó, 3 người thử nghiệm vaccine của Moderna và 2 người thử nghiệm vaccine của Pfizer, đều cho rằng những cảm giác khó chịu mà họ phải trải qua là đáng giá để tự bảo vệ bản thân chống lại virus SARS-CoV-2.
Luke Hutchison, một nhà sinh vật học 44 tuổi ở bang Utah, cho biết ông nằm liệt giường với cơn sốt hơn 101 độ F (38,3 độ C), run rẩy, ớn lạnh, đau đầu dữ dội và khó thở sau khi tiêm liều thứ hai loại vaccine của Moderna . Tuy nhiên, tình trạng nóng sốt chấm dứt trong khoảng 12 tiếng.
Một người khác, đang tham gia thử nghiệm vaccine của Pfize, cũng thức dậy với cảm giác ớn lạnh, run rẩy đến mức nứt một chiếc răng sau khi sử dụng liều thứ hai.
Mặc dù có thể một số triệu chứng được mô tả có thể là do một căn bệnh không liên quan, Moderna và Pfize từng nói rằng một số người tham gia thử nghiệm vaccine giai đoạn một của họ đã trải qua các triệu chứng như mắc bệnh Covid-19 thể nhẹ./.
Vaccine Oxford 'hẹn' ra mắt cuối năm nay  Dù phải ngừng thử nghiệm, giám đốc điều hành (CEO) AstraZeneca cho biết vaccine hãng phối hợp sản xuất với Đại học Oxford có thể ra mắt vào cuối năm nay. CEO Pascal Soriot cho biết tiến độ của khâu đánh giá an toàn sẽ quyết định thời gian diễn ra chương trình tiêm chủng. Ông bày tỏ kỳ vọng có thể hoàn...
Dù phải ngừng thử nghiệm, giám đốc điều hành (CEO) AstraZeneca cho biết vaccine hãng phối hợp sản xuất với Đại học Oxford có thể ra mắt vào cuối năm nay. CEO Pascal Soriot cho biết tiến độ của khâu đánh giá an toàn sẽ quyết định thời gian diễn ra chương trình tiêm chủng. Ông bày tỏ kỳ vọng có thể hoàn...
 Thực hư tin Campuchia điều binh sĩ tới biên giới với Thái Lan sau vụ đối đầu08:43
Thực hư tin Campuchia điều binh sĩ tới biên giới với Thái Lan sau vụ đối đầu08:43 Đòn giáng của ông Trump vào Ukraine trước ngưỡng cửa đàm phán với Nga09:07
Đòn giáng của ông Trump vào Ukraine trước ngưỡng cửa đàm phán với Nga09:07 Xung đột Nga - Ukraine trước bước ngoặt08:59
Xung đột Nga - Ukraine trước bước ngoặt08:59 Lãnh đạo Mỹ - Ukraine khẩu chiến kịch liệt08:41
Lãnh đạo Mỹ - Ukraine khẩu chiến kịch liệt08:41 'Ông Trump rất thất vọng về ông Zelensky, muốn Ukraine thỏa thuận khoáng sản 500 tỉ USD'09:08
'Ông Trump rất thất vọng về ông Zelensky, muốn Ukraine thỏa thuận khoáng sản 500 tỉ USD'09:08 Ông Trump sẽ đích thân kiểm kê kho vàng trị giá 425 tỉ USD của Mỹ09:43
Ông Trump sẽ đích thân kiểm kê kho vàng trị giá 425 tỉ USD của Mỹ09:43 Không chỉ Mỹ, Pháp cũng đàm phán về khoáng sản quan trọng với Ukraine09:14
Không chỉ Mỹ, Pháp cũng đàm phán về khoáng sản quan trọng với Ukraine09:14 Ông Trump bất ngờ nặng lời về ông Zelensky, nhiều bên bị sốc08:41
Ông Trump bất ngờ nặng lời về ông Zelensky, nhiều bên bị sốc08:41 Đặc phái viên Mỹ hé lộ điều Nga - Ukraine phải làm để đạt thỏa thuận hòa bình07:56
Đặc phái viên Mỹ hé lộ điều Nga - Ukraine phải làm để đạt thỏa thuận hòa bình07:56 Vụ trộm bồn cầu làm bằng 98 kg vàng: nghi phạm ra tay trong 5 phút09:08
Vụ trộm bồn cầu làm bằng 98 kg vàng: nghi phạm ra tay trong 5 phút09:08 Xe mất thắng lao xuống rãnh ven đường, ít nhất 18 người thiệt mạng tại Thái Lan01:07
Xe mất thắng lao xuống rãnh ven đường, ít nhất 18 người thiệt mạng tại Thái Lan01:07Tiêu điểm
Tin đang nóng
Tin mới nhất

EU và Ấn Độ đồng ý hoàn tất hiệp định thương mại tự do trong năm nay

ASEAN sẵn sàng thông qua Kế hoạch chiến lược Cộng đồng kinh tế 2026-2030

Tháng lễ Ramadan bắt đầu tại Indonesia

Năng lượng Mặt Trời trở thành 'miếng mồi' hấp dẫn với tin tặc

Hiện tượng hiếm gặp: Bảy hành tinh thẳng hàng trên bầu trời đêm

Israel đề xuất gia hạn giai đoạn 1 của thỏa thuận ngừng bắn tại Gaza

Cơn sốt vàng ở Mỹ 'hút' vàng thỏi từ nhiều quốc gia khác

Mỹ áp thuế nặng lên cáp nhôm sản xuất tại Hàn Quốc sử dụng vật liệu Trung Quốc

Thủ lĩnh PKK bất ngờ kêu gọi buông vũ khí, ngừng xung đột với Thổ Nhĩ Kỳ

Đồng minh hóa đối tác

Trung Quốc: Ít nhất 11 người thiệt mạng trong vụ tai nạn tàu thủy

Ba phương án của EU với 198 tỷ USD tài sản của Liên bang Nga bị đóng băng
Có thể bạn quan tâm

Hoà Minzy ra mắt MV mà cả làng như mở hội xuân: Dàn Anh Trai tháp tùng tận nơi, liền anh liền chị dàn hàng đón chào quan khách
Nhạc việt
20:56:47 01/03/2025
Nữ diễn viên đẹp "kinh thiên động địa" rung động cả nước biến mất bí ẩn
Sao châu á
20:53:29 01/03/2025
Học sinh tiểu học làm phép tính "11 - 4 = 7" bị gạch đỏ, mẹ đi chất vấn giáo viên thì nhận về một câu chí mạng
Netizen
20:51:51 01/03/2025
Nổ lớn gần một chi nhánh ngân hàng
Tin nổi bật
20:45:56 01/03/2025
Lý do Mạc Anh Thư và Huy Khánh ly hôn
Sao việt
20:16:54 01/03/2025
Hoà Minzy "nâng khăn sửa túi" cho Văn Toàn cực tình, ngượng chín mặt khi diễn cảnh hò hẹn, chemistry tràn màn hình
Sao thể thao
18:59:44 01/03/2025
Gã trai dùng clip sex tống tiền nữ Việt kiều Mỹ
Pháp luật
18:48:17 01/03/2025
Ai có thể thay thế Trấn Thành, Trường Giang ở Running Man Việt Nam?
Tv show
18:23:54 01/03/2025
 Quan hệ Mỹ – Trung không phải ‘Chiến tranh Lạnh mới’
Quan hệ Mỹ – Trung không phải ‘Chiến tranh Lạnh mới’ Chỉ 10 ngày, số ca nhiễm COVID-19 ở châu Âu tăng hơn gấp đôi
Chỉ 10 ngày, số ca nhiễm COVID-19 ở châu Âu tăng hơn gấp đôi

 Những lo ngại khi vaccine Oxford tạm dừng thử nghiệm
Những lo ngại khi vaccine Oxford tạm dừng thử nghiệm Mỹ thử nghiệm vaccine Covid-19 quy mô lớn
Mỹ thử nghiệm vaccine Covid-19 quy mô lớn Vaccine Covid-19 Mỹ đầu tiên được bình duyệt
Vaccine Covid-19 Mỹ đầu tiên được bình duyệt Tháng 7 quyết định cuộc đua vaccine
Tháng 7 quyết định cuộc đua vaccine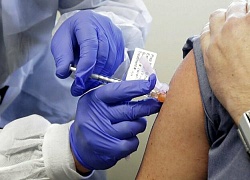 Vaccine tiến đến giai đoạn thử nghiệm cuối cùng
Vaccine tiến đến giai đoạn thử nghiệm cuối cùng Cuộc đua gian khó điều chế vaccine ngừa nCoV
Cuộc đua gian khó điều chế vaccine ngừa nCoV
 Thỏa thuận khoáng sản Mỹ - Ukraine bất thành sau màn tranh cãi cấp nguyên thủ
Thỏa thuận khoáng sản Mỹ - Ukraine bất thành sau màn tranh cãi cấp nguyên thủ Nga và Mỹ thảo luận điều gì trong 6 tiếng tại Thổ Nhĩ Kỳ?
Nga và Mỹ thảo luận điều gì trong 6 tiếng tại Thổ Nhĩ Kỳ? Thẩm phán Mỹ chặn lệnh sa thải hàng loạt của chính quyền ông Trump
Thẩm phán Mỹ chặn lệnh sa thải hàng loạt của chính quyền ông Trump Tổng thống Trump có thể ký sắc lệnh ghi nhận tiếng Anh là ngôn ngữ chính thức của Mỹ
Tổng thống Trump có thể ký sắc lệnh ghi nhận tiếng Anh là ngôn ngữ chính thức của Mỹ Tổng thống Ukraine có phát biểu công khai đầu tiên sau khi gặp Tổng thống Trump
Tổng thống Ukraine có phát biểu công khai đầu tiên sau khi gặp Tổng thống Trump Tổng thống Ukraine đã điện đàm ngay với 2 lãnh đạo châu Âu sau khi gặp Tổng thống Trump
Tổng thống Ukraine đã điện đàm ngay với 2 lãnh đạo châu Âu sau khi gặp Tổng thống Trump HOT: Á hậu Miss Universe Vietnam được cầu hôn, nhẫn kim cương "to vật vã" chứng minh vị hôn phu "không phải dạng vừa"!
HOT: Á hậu Miss Universe Vietnam được cầu hôn, nhẫn kim cương "to vật vã" chứng minh vị hôn phu "không phải dạng vừa"!
 Vợ đẹp của Lâm Tây gây tranh cãi khi tập gym chỉ sau 10 ngày sinh con, lên tiếng cảnh báo: Đừng như Xuân!
Vợ đẹp của Lâm Tây gây tranh cãi khi tập gym chỉ sau 10 ngày sinh con, lên tiếng cảnh báo: Đừng như Xuân! Gia đình xây dựng vườn tưởng niệm cho nữ diễn viên Từ Hy Viên
Gia đình xây dựng vườn tưởng niệm cho nữ diễn viên Từ Hy Viên Sao Hoa ngữ 1/3: Trương Quân Ninh tiết lộ cảnh tình tứ với Liên Bỉnh Phát
Sao Hoa ngữ 1/3: Trương Quân Ninh tiết lộ cảnh tình tứ với Liên Bỉnh Phát Selena Gomez và hành trình giảm cân, lấy lại phong độ nhan sắc
Selena Gomez và hành trình giảm cân, lấy lại phong độ nhan sắc Cô giáo gửi ảnh học sinh ngủ trưa và xóa trong 30 giây nhưng đã quá muộn: Phụ huynh quyết định chuyển trường
Cô giáo gửi ảnh học sinh ngủ trưa và xóa trong 30 giây nhưng đã quá muộn: Phụ huynh quyết định chuyển trường Vợ chồng Huyền thoại Hollywood Gene Hackman đã chết 9 ngày trước khi được phát hiện
Vợ chồng Huyền thoại Hollywood Gene Hackman đã chết 9 ngày trước khi được phát hiện Người mẹ bật điều hòa giữ xác con gái trong căn chung cư suốt 6 năm
Người mẹ bật điều hòa giữ xác con gái trong căn chung cư suốt 6 năm Người mẹ nguy kịch vì bị con trai tạt xăng dã man: "Tôi không bao giờ giận con..."
Người mẹ nguy kịch vì bị con trai tạt xăng dã man: "Tôi không bao giờ giận con..." Thêm 1 sao Việt tung tin nhắn, "bóc trần" mẹ bé Bắp nói chuyện trước sau bất nhất?
Thêm 1 sao Việt tung tin nhắn, "bóc trần" mẹ bé Bắp nói chuyện trước sau bất nhất? Mẹ Bắp lên tiếng về chiến dịch gây quỹ trên Give.Asia và mối quan hệ với gia đình chồng cũ
Mẹ Bắp lên tiếng về chiến dịch gây quỹ trên Give.Asia và mối quan hệ với gia đình chồng cũ Nóng: Huy Khánh và Mạc Anh Thư ly hôn sau 12 năm chung sống
Nóng: Huy Khánh và Mạc Anh Thư ly hôn sau 12 năm chung sống Nóng: Báo Hàn "bắt gọn" Lee Jong Suk hẹn hò Moon Ga Young, chuyện tình với IU đã toang?
Nóng: Báo Hàn "bắt gọn" Lee Jong Suk hẹn hò Moon Ga Young, chuyện tình với IU đã toang? Nóng: Mẹ Từ Hy Viên tuyên bố cho con rể cũ tất cả, nghi từ bỏ quyền nuôi cả 2 cháu
Nóng: Mẹ Từ Hy Viên tuyên bố cho con rể cũ tất cả, nghi từ bỏ quyền nuôi cả 2 cháu Mỹ nhân Việt đổi đời chỉ nhờ 1 cái bĩu môi, cả body lẫn nhan sắc đều thăng hạng đỉnh cao sau 8 năm
Mỹ nhân Việt đổi đời chỉ nhờ 1 cái bĩu môi, cả body lẫn nhan sắc đều thăng hạng đỉnh cao sau 8 năm Lộ nhan sắc thật của vợ mẫu tây Bùi Tiến Dũng qua cam thường video thân mật với chồng, có khác ảnh tự đăng?
Lộ nhan sắc thật của vợ mẫu tây Bùi Tiến Dũng qua cam thường video thân mật với chồng, có khác ảnh tự đăng? Kỳ thú hiện tượng "Thất tinh liên châu" - 7 hành tinh hội tụ hiếm gặp, ở Việt Nam quan sát được không?
Kỳ thú hiện tượng "Thất tinh liên châu" - 7 hành tinh hội tụ hiếm gặp, ở Việt Nam quan sát được không?