EU và AstraZeneca đạt thỏa thuận về phân phối vaccine COVID-19
Ủy ban châu Âu (EC) và hãng dược AstraZeneca ngày 3/9 cho biết đã đạt thỏa thuận về việc phân phối lượng vaccine ngừa COVID-19 còn lại trong hợp đồng, kết thúc vụ kiện tại Brussels về vấn đề này.
Vaccine ngừa COVID-19 của hãng dược AstraZeneca. Ảnh: AFP/TTXVN
Theo thỏa thuận này, AstraZeneca cam kết bàn giao cho Liên minh châu Âu (EU) 60 triệu liều vaccine trước cuối Quý III/2021, 75 triệu liều vào cuối Quý IV/2021 và 65 triệu liều trước cuối Quý I/2022.
Cơ quan điều hành EU cho biết, theo thỏa thuận mới, các nước thành viên EU sẽ được cung cấp lịch trình bàn giao định kỳ, và có thể giảm giá mua trong trường hợp AstraZence chậm bàn giao. Cao ủy EU về An toàn thực phẩm và sức khỏe Stella Kyriakides nhấn mạnh giữa các nước thành viên EU có khác biệt đáng kể về tỷ lệ tiêm chủng vaccine ngừa COVID-19 và mức độ sẵn có của các vaccine, trong đó có AstraZeneca, vẫn giữ vai trò vô cùng quan trọng.
AstraZeneca ban đầu dự kiến cung cấp 300 triệu liều vaccine cho EU trong 6 tháng đầu năm nay, song kế hoạch này đã bị cắt giảm xuống chỉ còn 100 triệu liều do gặp khó khăn về sản xuất. Điều này đã làm trì hoãn chương trình tiêm chủng quy mô lớn của EU khi khối này đặt cược vào vaccine của AstraZeneca để tiêm vaccine cho người dân trong khối. EC đã triển khai hành động pháp lý nhằm vào AstraZeneca hồi tháng 4/2021 với lý do hãng dược không tuân thủ hợp đồng đã ký về việc cung cấp vaccine ngừa COVID-19 của hãng cũng như không có kế hoạch “đáng tin cậy” để đảm bảo giao hàng đúng hạn. Khối liên minh này yêu cầu hãng dược phải cung cấp 120 triệu liều vaccine vào trước ngày 30/6 và hoàn tất hợp đồng 300 triệu liều vào tháng 9.
Video đang HOT
Hồi giữa tháng 6, một tòa án Bỉ đã ra phán quyết có lợi cho hãng dược AstraZeneca trong vụ kiện của EU, theo AstraZeneca chỉ phải chuyển giao thêm 50 triệu liều vaccine phòng COVID-19 cho các nước EU đến ngày 27/9 tới. Tuy nhiên, phán quyết khẳng định AstraZeneca vẫn có nghĩa vụ hoàn tất hợp đồng giao 300 triệu liều nhưng không nói rõ thời hạn chót.
Pháp kêu gọi Anh hợp tác về phân phối vaccine của AstraZeneca
Ngày 26/3, Ngoại trưởng Pháp Jean-Yves Le Drian cho rằng Anh đang gây sức ép với Liên minh châu Âu (EU) do nước này bị thiếu vaccine ngừa COVID-19 để tiêm phòng cho người dân.
Vaccine ngừa COVID-19 của AstraZeneca. Ảnh: AFP/TTXVN
Phát biểu trên đài France Info, Ngoại trưởng Le Drian cho rằng sau khi đẩy nhanh việc tiêm phòng mũi đầu cho người dân, Anh đang bị thiếu vaccine để tiêm mũi thứ 2. Trước tình hình này, Pháp kêu gọi Anh thỏa thuận hợp tác về phân phối vaccine của AstraZeneca, thay vì gây sức ép như hiện nay.
Tuyên bố trên được đưa ra trong bối cảnh chương trình tiêm chủng vaccine ngừa COVID-19 tại Anh và EU đều chậm trễ do thiếu nguồn cung vaccine. Hai bên đang tranh cãi để giành quyền tiếp cận số vaccine của hãng AstraZeneca sản xuất tại một nhà máy ở Hà Lan.
Để đảm bảo nguồn cung cho khối, EU ngày 25/3 đã cảnh báo sẽ cấm xuất khẩu vaccine ngừa COVID-19 với lượng nhất định.
Về phần mình, Thủ tướng Hà Lan Mark Rutt tuyên bố Anh và EU có thể đạt được thỏa thuận về chia sẻ vaccine vào cuối tuần này hoặc sớm hơn để tránh việc EU áp đặt lệnh cấm xuất khẩu. Tuy nhiên, nhà lãnh đạo Hà Lan cho biết nước này sẽ phải tuân thủ trong trường hợp EU quyết định cấm xuất khẩu vaccine được sản xuất tại nhà máy Halix của Hà Lan sang Anh.
Cũng liên quan đến vaccine ngừa COVID-19, Ngoại trưởng Le Drian cho rằng Nga đang sử dụng vaccine Sputnik V để gia tăng sức ảnh hưởng và Trung Quốc cũng sử dụng vaccine do nước này sản xuất với mục đích tương tự. Tuyên bố này được đưa ra sau khi Nga thông báo sẽ bàn giao 30.000 liều vaccine cho Tunisia.
Trả lời phỏng vấn, người phát ngôn của Điện Kremlin Dmitry Peskov đã lập tức lên tiếng bác bỏ nhận định này.
Cơ quan dược phẩm của Liên minh châu Âu (EMA) đang phân tích dữ liệu hiện có về tính an toàn và hiệu quả của vaccine Sputnik V. Trong khi đó, các nhà phát triển vaccine Nga thông báo họ đã đạt được thỏa thuận sản xuất tại các quốc gia quan trọng của EU, gồm Đức, Pháp, Italy và Tây Ban Nha.
Việc EU phê duyệt Sputnik V sẽ đánh dấu bước ngoặt thay đổi quan điểm đối với loại vaccine của Nga. Vaccine Sputnik V của Nga đang được sử dụng tại trên 20 nước... Một nghiên cứu được công bố vào tháng trước đã đánh giá hiệu quả của Sputnik V là 91,6%. Các thành viên EU là Hungary và Slovakia đã mua Sputnik V trong thời gian chờ đợi quyết định cấp phép sử dụng vaccine này từ EU.
Trong tuyên bố mới nhất, người phát ngôn của Thủ tướng Đức Angela Merkel, Steffen Seibert cũng khẳng định sẽ dụng vaccine Sputnik V của Nga nếu sản phẩm này được EMA phê duyệt.
Cùng ngày, kênh truyền hình TV2 đưa tin Na Uy sẽ hoãn việc đưa ra quyết định xem có tiếp tục sử dụng vaccine ngừa COVID-19 của hãng AstraZeneca hay không. Trong khi đó, Viện Y tế công Na Uy tuyên bố sẽ thông báo quyết định trong ngày 26/3.
Cách đây 2 tuần, Chính phủ Na Uy đã đình chỉ việc sử dụng vaccine của AstraZeneca sau khi một số người trẻ tuổi được tiêm chủng phải nhập viện với các triệu chứng đông máu, chảy máu và giảm tiểu cầu. Na Uy nằm trong số nhiều nước châu Âu đã tạm dừng việc tiêm phòng bằng vaccine của AstraZeneca do lo ngại mức độ an toàn. Hiện phần lớn các nước đều đã nối lại việc tiêm phòng sau khi EMA khẳng định vaccine an toàn và nhìn chung không liên quan hiện tượng đông máu, đồng thời cho rằng chỉ cần thêm thông tin cảnh báo về các nguy cơ trên nhãn mác của vaccine.
Tổ chức Y tế Thế giới (WHO) cũng ủng hộ việc tiêm vaccine ngừa COVID-19 của hãng AstraZeneca và kêu gọi các quốc gia duy trì việc triển khai tiêm chủng sau khi xem xét các báo cáo về hiện tượng đông máu ghi nhận ở một số trường hợp được tiêm vaccine
Hôm 24/3 vừa qua, hãng dược phẩm liên doanh Anh - Thụy Điển AstraZeneca công bố báo cáo cập nhật về vaccine phòng COVID-19 do hãng này phối hợp với đại học Oxford (Anh) phát triển, khẳng định vaccine có hiệu quả 100% ngăn ngừa nguy cơ bệnh nặng và 76% ngăn ngừa nguy cơ mắc bệnh có triệu chứng.
Vaccine AstraZeneca tại Mỹ hiệu quả 79%  Kết quả thử nghiệm tại Mỹ, vaccine Covid-19 của AstraZeneca, tên gọi AZD1222, hiệu quả 79% và không gây ra nguy cơ đông máu. Kết quả phân tích độ an toàn và hiệu quả được Mỹ công bố ngày 22/3. Thử nghiệm giai đoạn 3 tiến hành trên hơn 32.000 người. Trong số các tình nguyện viên, khoảng 20% từ 65 tuổi trở...
Kết quả thử nghiệm tại Mỹ, vaccine Covid-19 của AstraZeneca, tên gọi AZD1222, hiệu quả 79% và không gây ra nguy cơ đông máu. Kết quả phân tích độ an toàn và hiệu quả được Mỹ công bố ngày 22/3. Thử nghiệm giai đoạn 3 tiến hành trên hơn 32.000 người. Trong số các tình nguyện viên, khoảng 20% từ 65 tuổi trở...
 Mỹ cảnh báo Nga, khẳng định cam kết với NATO09:42
Mỹ cảnh báo Nga, khẳng định cam kết với NATO09:42 Hamas kêu gọi ngừng bắn08:16
Hamas kêu gọi ngừng bắn08:16 Vị thế nước Đức cho an ninh châu Âu08:52
Vị thế nước Đức cho an ninh châu Âu08:52 Tổng thống Putin ca ngợi tỉ phú Musk08:48
Tổng thống Putin ca ngợi tỉ phú Musk08:48 Trung Quốc gửi thông điệp mới tới Mỹ08:43
Trung Quốc gửi thông điệp mới tới Mỹ08:43 Mỹ điều oanh tạc cơ B-2, Iran phải tự đoán thông điệp09:02
Mỹ điều oanh tạc cơ B-2, Iran phải tự đoán thông điệp09:02 Yêu sách mới của Israel tại Gaza08:11
Yêu sách mới của Israel tại Gaza08:11 Houthi lại bắn hạ MQ-9, Mỹ tập kích Yemen dồn dập08:25
Houthi lại bắn hạ MQ-9, Mỹ tập kích Yemen dồn dập08:25 Chính quyền Mỹ nêu lý do ông Trump hoãn áp thuế đối ứng08:54
Chính quyền Mỹ nêu lý do ông Trump hoãn áp thuế đối ứng08:54 Mỹ muốn mở lại loạt căn cứ quân sự ở Panama08:45
Mỹ muốn mở lại loạt căn cứ quân sự ở Panama08:45 Trực thăng lao xuống sông ở New York, 6 người thiệt mạng00:42
Trực thăng lao xuống sông ở New York, 6 người thiệt mạng00:42Tiêu điểm
Tin đang nóng
Tin mới nhất

Italy hoài nghi khả năng đạt mục tiêu chi tiêu quốc phòng 2% GDP của NATO

Tiền kỹ thuật số $TRUMP tăng vọt sau tin mời ăn tối cùng Tổng thống

Ông Trump tuyên bố sẽ giảm mạnh thuế với Trung Quốc

Iran 'bật đèn xanh' cho IAEA khôi phục giám sát hạt nhân

Boeing xác nhận Trung Quốc từ chối tiếp nhận 50 máy bay

Số người bị thương trong động đất ở Thổ Nhĩ Kỳ tăng lên 236 người

Ukraine đối mặt 'ngã rẽ sống còn' dưới sức ép đàm phán của Tổng thống Trump

Thuế quan của Mỹ: Liên minh gồm 12 bang kiện chính quyền của Tổng thống Donald Trump

Thụy Sỹ thể hiện cam kết rõ ràng với Mỹ

Tổng thống Trump cảnh báo 'chảy máu triệu phú' khi đảng Cộng hòa đề xuất tăng thuế

UAV và tên lửa Nga dội xuống thủ đô của Ukraine, 56 người thương vong

Trung Quốc sắp khánh thành cây cầu cao nhất hành tinh
Có thể bạn quan tâm

Đoạn trích xuất camera 1,5 triệu người xem phơi bày hôn nhân kỳ lạ của đôi vợ chồng Á hậu - diễn viên hot Vbiz
Sao việt
14:51:50 24/04/2025
Vụ sao nam lộ ảnh thân mật giữa đêm với ngọc nữ kém 15 tuổi: Thêm 2 người mẫu bikini bị réo tên!
Sao châu á
14:47:18 24/04/2025
Diễn viên Thanh Thúy khoe vẻ đẹp không tuổi với đầm chất liệu lụa
Phong cách sao
14:46:49 24/04/2025
Người đàn ông tử vong khi đang chơi pickleball
Tin nổi bật
14:33:42 24/04/2025
Xem độ mỏng đáng kinh ngạc của iPhone 17 Air trong video mới
Đồ 2-tek
14:30:13 24/04/2025
Đối thủ lớn nhất của iPhone có lợi thế trong cuộc chiến thuế quan của ông Trump?
Thế giới số
14:03:24 24/04/2025
San phẳng hơn 1000 ngọn núi để xây dựng kỳ quan chỉ bằng dụng cụ thô sơ
Lạ vui
14:00:37 24/04/2025
Cựu Thứ trưởng Bộ Tài nguyên và Môi trường chuẩn bị hầu tòa vụ đất hiếm
Pháp luật
13:37:08 24/04/2025
Sự cố của Jennie suýt gây ra "thảm họa" tại Coachella
Nhạc quốc tế
12:59:18 24/04/2025
NSND Mỹ Uyên từng tủi thân vì bị đạo diễn Victor Vũ 'giấu' khi quảng bá phim
Hậu trường phim
12:55:10 24/04/2025
 Campuchia thí điểm cho phép bệnh nhân triệu chứng nhẹ điều trị tại khách sạn
Campuchia thí điểm cho phép bệnh nhân triệu chứng nhẹ điều trị tại khách sạn Chuyển khỏi Cairo, Ai Cập đầu tư công nghệ nhảy vọt cho thủ đô mới
Chuyển khỏi Cairo, Ai Cập đầu tư công nghệ nhảy vọt cho thủ đô mới Thêm nhiều nước quay lại dùng vaccine AstraZeneca phòng COVID-19
Thêm nhiều nước quay lại dùng vaccine AstraZeneca phòng COVID-19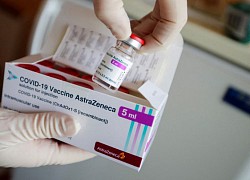 Lãnh đạo châu Âu lục đục vì vaccine AstraZeneca
Lãnh đạo châu Âu lục đục vì vaccine AstraZeneca Đức, Italy hỗn loạn sau đình chỉ vaccine AstraZeneca
Đức, Italy hỗn loạn sau đình chỉ vaccine AstraZeneca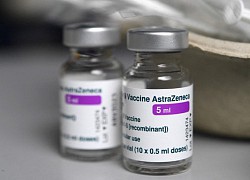 Australia, Canada trấn an về vaccine AstraZeneca
Australia, Canada trấn an về vaccine AstraZeneca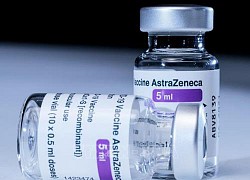 Đại học Oxford khẳng định vaccine AstraZeneca không liên quan với bệnh huyết khối
Đại học Oxford khẳng định vaccine AstraZeneca không liên quan với bệnh huyết khối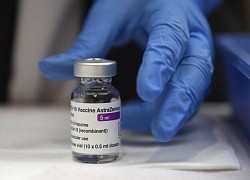 Người từng tiêm vaccine AstraZeneca ở Na Uy bị đông máu
Người từng tiêm vaccine AstraZeneca ở Na Uy bị đông máu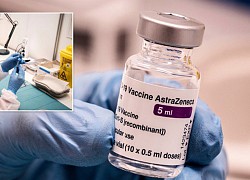 Đan Mạch dừng tiêm vaccine COVID-19 AstraZeneca sau ca tử vong vì máu đông
Đan Mạch dừng tiêm vaccine COVID-19 AstraZeneca sau ca tử vong vì máu đông Vaccine AstraZeneca 'chống biển chủng nCoV Brazil hiệu quả'
Vaccine AstraZeneca 'chống biển chủng nCoV Brazil hiệu quả' COVID-19 tại ASEAN hết 21/2: Thêm 12.620 ca mắc; Campuchia có 17 ca mắc mới trong làn sóng thứ 3
COVID-19 tại ASEAN hết 21/2: Thêm 12.620 ca mắc; Campuchia có 17 ca mắc mới trong làn sóng thứ 3 Thái Lan chuẩn bị nhận thêm 61 triệu liều vaccinengừa COVID-19
Thái Lan chuẩn bị nhận thêm 61 triệu liều vaccinengừa COVID-19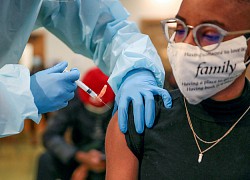 Cuộc đua vaccine 'trị được mọi biến thể nCoV'
Cuộc đua vaccine 'trị được mọi biến thể nCoV'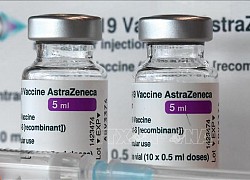 AstraZeneca công bố kết quả thử nghiệm thuốc phòng ngừa và điều trị COVID-19
AstraZeneca công bố kết quả thử nghiệm thuốc phòng ngừa và điều trị COVID-19 Tổng thống Trump hé lộ khả năng 'giảm đáng kể' thuế với Trung Quốc
Tổng thống Trump hé lộ khả năng 'giảm đáng kể' thuế với Trung Quốc Tỷ phú Elon Musk sẽ giảm thời gian làm việc cho Chính phủ Mỹ
Tỷ phú Elon Musk sẽ giảm thời gian làm việc cho Chính phủ Mỹ Fed phát tín hiệu giữ nguyên lãi suất bất chấp áp lực từ Tổng thống Trump
Fed phát tín hiệu giữ nguyên lãi suất bất chấp áp lực từ Tổng thống Trump Chiến đấu cơ Mỹ chặn máy bay ném bom chiến lược có thể mang vũ khí hạt nhân của Nga
Chiến đấu cơ Mỹ chặn máy bay ném bom chiến lược có thể mang vũ khí hạt nhân của Nga Linh cữu Giáo hoàng Francis được đưa đến Vương cung thánh đường Thánh Peter
Linh cữu Giáo hoàng Francis được đưa đến Vương cung thánh đường Thánh Peter Điều gì xảy ra khi Mỹ rút khỏi tiến trình hòa bình giữa Nga và Ukraine?
Điều gì xảy ra khi Mỹ rút khỏi tiến trình hòa bình giữa Nga và Ukraine? Tổng thống Zelensky tuyên bố sẵn sàng đàm phán với Nga 'dưới mọi hình thức'
Tổng thống Zelensky tuyên bố sẵn sàng đàm phán với Nga 'dưới mọi hình thức' Kho vũ khí lớn hàng đầu của Nga phát nổ dữ dội
Kho vũ khí lớn hàng đầu của Nga phát nổ dữ dội Cặp sinh đôi nhà Phương Oanh - shark Bình hóa thân thành chiến sĩ nhí, hành động ngộ nghĩnh khiến ai cũng bật cười
Cặp sinh đôi nhà Phương Oanh - shark Bình hóa thân thành chiến sĩ nhí, hành động ngộ nghĩnh khiến ai cũng bật cười Vợ Hồ Tấn Tài từng lên mạng tố HLV ĐT Việt Nam để bảo vệ chồng, sau ồn ào cuộc sống gia đình gây chú ý
Vợ Hồ Tấn Tài từng lên mạng tố HLV ĐT Việt Nam để bảo vệ chồng, sau ồn ào cuộc sống gia đình gây chú ý Đạo diễn Quang Dũng bị nhồi máu cơ tim
Đạo diễn Quang Dũng bị nhồi máu cơ tim "Ngọc nữ" từ chối Lâm Chí Dĩnh gặp bi kịch vì kết hôn với đại gia rởm
"Ngọc nữ" từ chối Lâm Chí Dĩnh gặp bi kịch vì kết hôn với đại gia rởm
 Cặp đôi trong mơ của làng thể thao đối mặt với khủng hoảng hôn nhân: Chồng đi suốt ngày, để vợ ở nhà chăm con
Cặp đôi trong mơ của làng thể thao đối mặt với khủng hoảng hôn nhân: Chồng đi suốt ngày, để vợ ở nhà chăm con Kẻ "ngáo đá" đến Công an phường khai nhận dùng ma túy có 3 khẩu súng và 39 viên đạn
Kẻ "ngáo đá" đến Công an phường khai nhận dùng ma túy có 3 khẩu súng và 39 viên đạn Toàn cảnh vụ sữa giả: Lợi dụng kẽ hở, thu lợi bất chính hàng trăm tỷ
Toàn cảnh vụ sữa giả: Lợi dụng kẽ hở, thu lợi bất chính hàng trăm tỷ Dùng dao đâm bạn gái tử vong rồi lên ô tô phóng hỏa tự sát
Dùng dao đâm bạn gái tử vong rồi lên ô tô phóng hỏa tự sát Giấu kín bấy lâu, 1 mỹ nhân Việt công khai có con trai với vị bác sĩ thẩm mỹ nổi tiếng?
Giấu kín bấy lâu, 1 mỹ nhân Việt công khai có con trai với vị bác sĩ thẩm mỹ nổi tiếng? Á hậu Quỳnh Châu xin lỗi về bài đăng kẹt xe ngay dịp Đại lễ 30/4
Á hậu Quỳnh Châu xin lỗi về bài đăng kẹt xe ngay dịp Đại lễ 30/4 Hot: Vợ Bùi Tiến Dũng hạ sinh quý tử, "nam thần" lấy vợ sớm nhất dàn U23 Việt Nam nay đã là bố 3 con
Hot: Vợ Bùi Tiến Dũng hạ sinh quý tử, "nam thần" lấy vợ sớm nhất dàn U23 Việt Nam nay đã là bố 3 con
 Phiên tòa xử vụ kiện cháy xe 5 tỷ đồng của ca sĩ Duy Mạnh: Tình tiết sự việc nghe mà "sốc"
Phiên tòa xử vụ kiện cháy xe 5 tỷ đồng của ca sĩ Duy Mạnh: Tình tiết sự việc nghe mà "sốc"
 Cô gái Bắc Giang nhan sắc gây sốt trong 'khối hoa hậu' diễu binh 30/4
Cô gái Bắc Giang nhan sắc gây sốt trong 'khối hoa hậu' diễu binh 30/4 Thông tin đặc biệt về lễ thuỷ táng của Quý Bình
Thông tin đặc biệt về lễ thuỷ táng của Quý Bình Người phụ nữ đi đường bất ngờ bị kéo lên ô tô, 'tra tấn' bằng axit và máy xăm
Người phụ nữ đi đường bất ngờ bị kéo lên ô tô, 'tra tấn' bằng axit và máy xăm