Chỉ với công nghệ này, các tế bào ung thư sẽ “tự sát” và “huynh đệ tương tàn”
Phương pháp sử dụng công nghệ chỉnh sửa gene này không chỉ khiến tế bào ung thư tự sát mà còn tiêu diệt tế bào ung thư huynh đệ của mình.
Mới đây một nhóm nhà nghiên cứu đến từ Đại học Y Harvard (Mỹ) đã thử nghiệm việc tái lập trình các tế bào ung thư nhằm “đánh lừa” chúng quay sang tấn công nhau và giết chết chính tế bào anh em của mình.
Phương pháp “đánh lừa” các tế bào ung thư tự tiêu diệt lẫn nhau
Các tế bào ung thư thường có hành vi “tự tìm đường về nhà” – tức là các tế bào đã di căn trở lại khối u gốc nơi chúng được sản sinh ra. Nhóm nghiên cứu đã tận dụng đặc tính này của các tế bào di động, biến điểm mạnh của chúng trở thành điểm yếu.
Các tế bào ung thư thường có hành vi “tự quay về nhà”
Về ý tưởng, nhóm nghiên cứu sử dụng CRISPR để đưa S-TRAIL vào tế bào ung thư, đây là một loại protein có khả năng tiêu diệt các tế bào ung thư mà không gây hại cho các tế bào khỏe mạnh.
Ý tưởng của nhóm là đưa “công tắc tiêu diệt” vào tế bào, khiến chúng thủ tiêu bất cứ tế bào ung thư nào gặp phải trên đường. Đồng thời “công tắc tự tử” – bắt chúng tự hủy trước khi lây lan sang các bộ phận khác hoặc tự hình thành khối u cũng hoạt động.
Video đang HOT
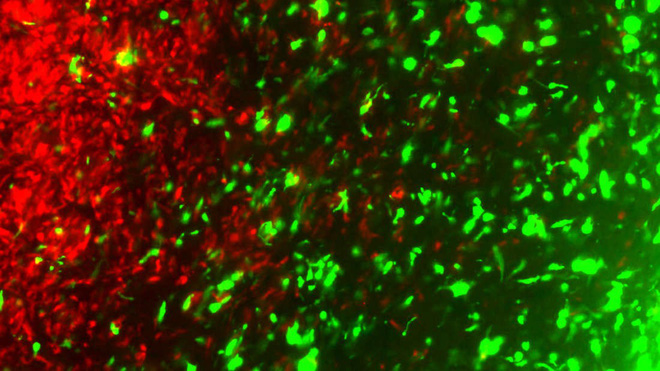
Tế bào ung thư điều chỉnh gen (xanh) tấn công các tế bào ung thư (đỏ)
Các nhà nghiên cứu sử dụng hai phương pháp kết hợp để thử nghiệm lý thuyết của họ. Thí nghiệm được tiến hành trên các mẫu chuột bị u não nguyên phát, u não tái phát và ung thư vú đã di căn lên não.
Đúng như dự định, cả hai phương pháp sử dụng các “tế bào sát thủ” không những thu nhỏ kích thước khối u một cách đáng kể mà còn làm tăng khả năng sống của chuột.
Kết quả được công bố trên tạp chí Science Translational Medicine ngày 11/07/2018, đây không phải là nỗ lực đầu tiên nhằm khiến các tế bào ung tự tiêu diệt lẫn nhau.
Tiến sĩ Khalid Shah đến từ trường Đại học Y Harvard và Viện nghiên cứu tế bào gốc, trưởng nhóm nghiên cứu nói trong một bài phát biểu: “Đây mới chỉ là bề nổi. Các phương pháp trị bệnh dựa trên tế bào có tiềm năng to lớn trong việc đưa nhân tố có khả năng chữa trị đến khối u. Điều này sẽ cho chúng ta thêm lựa chọn khi mà phương pháp thông thường đều thất bại”.
“Với công nghệ này, chúng tôi muốn chứng minh việc tái cấu trúc tế bào ung thư và dùng chính chúng để chữa trị ung thư là điều có thể. Chúng tôi nghĩ việc này sẽ có nhiều tác động và có thể áp dụng trên tất cả các loại tế bào ung thư.”
Phương pháp mới được kỳ vọng sẽ có tác dụng trên tất cả các loại ung thư
Hiện tại vẫn chưa thể đảm bảo rằng phương pháp này sẽ có tác dụng ở người tương tự như ở chuột, tuy nhiên đây vẫn là một tín hiệu đáng mừng.
Công trình nghiên cứu đang ở giai đoạn đầu và sẽ còn nhiều thử nghiệm trong thời gian tới, nếu thành công, công nghệ này hứa hẹn mang lại một phương pháp nhanh chóng, chính xác và hiệu quả trong việc điều trị ung thư.
Tham khảo: iflscience, techtimes, firstpost
Theo Helino
Thuốc mới có thể ngăn ngừa ung thư di căn
Các nhà khoa học đã phát hiện ra hợp chất có thể "đóng băng" các tế bào ung thư trên đường đi và ngăn chúng di căn, có thể khiến chúng dễ bị tiêu diệt hơn, theo nghiên cứu được công bố trên tạp chí Nature Communications.
Ngăn ngừa ung thư lan rộng là điều thiết yếu để cứu tính mạng.
Trong khi việc điều trị bệnh cần tiêu diệt các tế bào ung thư, song ngăn chặn sự lan tràn của chúng ra khắp cơ thể - một quá trình được gọi là di căn - cũng quan trọng không kém. Tuy nhiên, phần lớn các liệu pháp ung thư hiên nay được thiết kế đơn giản để tiêu diệt các tế bào, theo Raymond Bergan, giảng viên y tại Đại học Khoa học & Sức khỏe Oregon (OHSU), người đứng đầu nghiên cứu.
Việc thiếu các phương pháp điều trị được thiết kế để ngăn chặn sự di chuyển của ung thư là vấn đề mà các nhà nghiên cứu tại OHSU - hợp tác với các đồng nghiệp từ Đại học Northwestern, Đại học Chicago, Đại học Washington và Đại học Hạ Môn, Trung Quốc đang cố gắng giải quyết.
"Đối với đại đa số các ung thư - vú, tuyến tiền liệt, phổi, đại tràng và các loại khác - nếu được phát hiện sớm khi còn là một khối u nhỏ trong cơ quan đó và không lan rộng, bạn sẽ sống", Bergan nói trong. Còn nói chung, nếu phát hiện muộn, sau khi bệnh đã lan rộng khắp cơ thể, thì bệnh nhân sẽ không qua khỏi".
"Sự di chuyển là điểm mấu chốt: sự khác biệt là đen và trắng, đêm và ngày. Nếu các tế bào ung thư lan ra khắp cơ thể, chúng sẽ lấy đi mạng sống của bạn. Chúng ta có thể điều trị chúng, nhưng chúng sẽ lấy mạng sống của bạn."
Từ năm 2011, các nhà nghiên cứu đã cố gắng phát triển một loại thuốc kiểm soát sự di căn của ung thư. Trong các thí nghiệm, họ đã xác định được một hợp chất đặc biệt - được gọi là KBU2046 - ức chế sự di chuyển của tế bào của 4 loại ung thư khác nhau (vú, đại tràng, phổi, tuyến tiền liệt).
Hợp chất này hoạt động bằng cách liên kết với các protein cụ thể để làm sạch các tế bào. Bằng cách gắn với các protein này, chất ức chế tính di động của chúng mà không gây bất kỳ tác dụng phụ nào - một cơ chế khác thường mà các nhà khoa học đã dành nhiều năm để cố tìm hiểu.
Cuối cùng mục tiêu của nghiên cứu là phát triển một liệu pháp có thể áp dụng cho bệnh nhân trong giai đoạn sớm của bệnh để ngăn ngừa ung thư di căn, khi nó trở nên khó điều trị hơn nhiều.
"Mục tiêu cuối cùng của chúng tôi là có thể nói với một người phụ nữ bị ung thư vú rằng: đây, hãy uống viên thuốc này và ung thư sẽ không lan ra khắp cơ thể của bạn", Bergan nói. "Điều tương tự cho bệnh nhân ung thư tuyến tiền liệt, phổi và đại tràng."
Cho đến nay, hợp chất mới chỉ được thử nghiệm trên tế bào người nuôi cấy và do đó một loại thuốc được chấp thuận dựa trên hợp chất này vẫn còn là một chặng đường dài. Nhóm nghiên cứu hiện đang gây quỹ để tài trợ cho các nghiên cứu sâu hơn và đã thành lập một công ty, Third Coast Therapeutics, để giúp thực hiện tầm nhìn của họ.
Cẩm Tú
Theo Dân trí
Tại sao có bao nhiêu loại ung thư, chẳng bao giờ chúng ta nghe thấy "ung thư tim"? 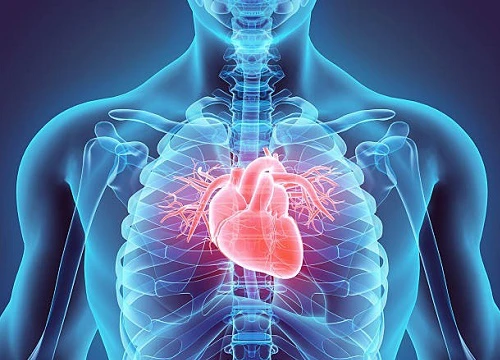 Đã bao nhiêu lần bạn nghe thấy ai đó nhắc tới cụm từ "ung thư tim"? Có người tin rằng tim là cơ quan duy nhất không bao giờ mắc phải căn bệnh quái ác này. Liệu điều đó có đúng không? Bạn đã bao giờ nghe về cụm từ "ung thư tim"? Cần làm rõ rằng đây là một căn bệnh hoàn...
Đã bao nhiêu lần bạn nghe thấy ai đó nhắc tới cụm từ "ung thư tim"? Có người tin rằng tim là cơ quan duy nhất không bao giờ mắc phải căn bệnh quái ác này. Liệu điều đó có đúng không? Bạn đã bao giờ nghe về cụm từ "ung thư tim"? Cần làm rõ rằng đây là một căn bệnh hoàn...
 Sự cố chấn động điền kinh: VĐV bị đối thủ vụt gậy vào đầu, nghi vỡ hộp sọ02:05
Sự cố chấn động điền kinh: VĐV bị đối thủ vụt gậy vào đầu, nghi vỡ hộp sọ02:05 Báo Mỹ: Ông Trump "khó chịu" vì trang phục của ông Zelensky01:28
Báo Mỹ: Ông Trump "khó chịu" vì trang phục của ông Zelensky01:28 TP.HCM: Xôn xao clip nhóm người ngang nhiên chặn xe kiểm tra giấy tờ06:11
TP.HCM: Xôn xao clip nhóm người ngang nhiên chặn xe kiểm tra giấy tờ06:11 Nhân viên y tế bị đánh hội đồng ngay tại nơi làm việc00:17
Nhân viên y tế bị đánh hội đồng ngay tại nơi làm việc00:17 Kế hoạch bắt cóc người đàn ông Trung Quốc, tống tiền 10 tỷ đồng ở TPHCM13:48
Kế hoạch bắt cóc người đàn ông Trung Quốc, tống tiền 10 tỷ đồng ở TPHCM13:48 Ông Tập Cận Bình nói kinh tế Trung Quốc đang đối mặt nhiều thách thức08:09
Ông Tập Cận Bình nói kinh tế Trung Quốc đang đối mặt nhiều thách thức08:09 Israel vận động Mỹ giữ căn cứ Nga ở Syria?08:52
Israel vận động Mỹ giữ căn cứ Nga ở Syria?08:52 Ông Trump gợi ý ông Zelensky có thể ra đi vì từ chối thỏa thuận08:44
Ông Trump gợi ý ông Zelensky có thể ra đi vì từ chối thỏa thuận08:44 Ông Zelensky nói gì về chuyện tổ chức bầu cử ở Ukraine?10:13
Ông Zelensky nói gì về chuyện tổ chức bầu cử ở Ukraine?10:13 Ông Trump phát biểu tại quốc hội, một nghị sĩ bị mời ra ngoài09:32
Ông Trump phát biểu tại quốc hội, một nghị sĩ bị mời ra ngoài09:32 Trung Quốc tuyên bố cứng về cuộc tập trận gần Úc09:44
Trung Quốc tuyên bố cứng về cuộc tập trận gần Úc09:44Tiêu điểm
Tin đang nóng
Tin mới nhất

Tập luyện khi bụng đói có giúp đốt cháy nhiều mỡ hơn?

Dấu hiệu trên da cảnh báo bệnh truyền nhiễm nguy hiểm

6 loại thực phẩm giúp thanh lọc gan tốt nhất

Bạn chống đẩy được bao nhiêu lần liên tiếp?

Sau cú ngã mạnh, người đàn ông đi tiểu ra máu, suýt phải cắt thận

Sốt cao 2 tuần không đến bệnh viện, một học sinh tử vong

Vì sao ngâm chân tốt cho giấc ngủ?

Khi nào nên uống nước để phòng đột quỵ?

Dự phòng đợt cấp cho bệnh nhân COPD

Gia Lai: Bệnh sởi sẽ còn diễn biến phức tạp đến mùa hè

Người bệnh hẹp thanh quản tập luyện như thế nào?

Những người nên uống Omega-3 và liều dùng cho từng nhóm
Có thể bạn quan tâm

Loài hoa rừng mỗi năm chỉ nở một lần, du khách tò mò vượt 80km để check-in
Du lịch
09:18:12 10/03/2025
Quảng Nam: Thêm một học sinh huyện miền núi tử vong chưa rõ nguyên nhân
Tin nổi bật
09:07:49 10/03/2025
Triệu Vy còn gì sau cú "gãy cánh" bí ẩn nhất lịch sử showbiz Hoa ngữ?
Sao châu á
08:37:54 10/03/2025
Một huyền thoại FPS 12 năm tuổi đời chuẩn bị "sống dậy" - từng là "đối chọi" với Đột Kích?
Mọt game
08:33:01 10/03/2025
Hôm nay xét xử 8 bị cáo vụ cháy chung cư mini làm 56 người chết
Pháp luật
08:31:31 10/03/2025
Sao Việt 10/3: Vợ chồng Salim Hải Long hạnh phúc trong đám cưới
Sao việt
08:24:25 10/03/2025
Ông Elon Musk bị Nhà Trắng hạn chế quyền hành?
Thế giới
08:17:18 10/03/2025
'Cha tôi người ở lại' tập 10: Bố đẻ của Việt dàn cảnh tai nạn để tiếp cận con trai
Phim việt
07:29:21 10/03/2025
Hai bộ phim đình đám tái hiện cuộc đời những thiên tài công nghệ cự phách
Phim âu mỹ
07:22:21 10/03/2025
Mỹ nhân Việt đóng chính phim nào thất bại phim đó, tiếc cho nhan sắc cực phẩm đẹp không tả nổi
Hậu trường phim
07:10:48 10/03/2025
 Liệu pháp ánh sáng chữa được vết loét lâu liền
Liệu pháp ánh sáng chữa được vết loét lâu liền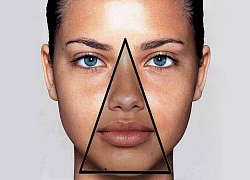 Vùng tam giác tử thần trên mặt: Nặn mụn, nhổ lông mũi có thể gây liệt cơ, thậm chí tử vong
Vùng tam giác tử thần trên mặt: Nặn mụn, nhổ lông mũi có thể gây liệt cơ, thậm chí tử vong
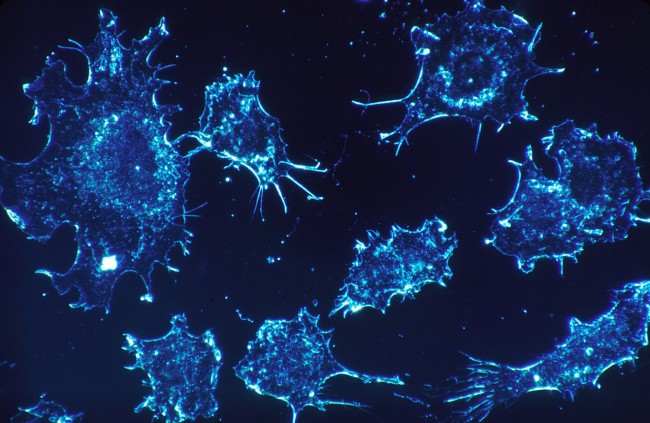

 Ai cũng có tế bào ung thư trong người: 3 nguyên tắc vàng chặn đứng sự hình thành khối u
Ai cũng có tế bào ung thư trong người: 3 nguyên tắc vàng chặn đứng sự hình thành khối u Ức chế khối u ung thư bằng a xít béo omega-3
Ức chế khối u ung thư bằng a xít béo omega-3 Chụp X-quang màu 3D đầu tiên giúp chẩn đoán bệnh hiệu quả hơn
Chụp X-quang màu 3D đầu tiên giúp chẩn đoán bệnh hiệu quả hơn Cơ thể được cung cấp đủ loại vitamin này sẽ giảm nguy cơ ung thư đại trực tràng đến 31%
Cơ thể được cung cấp đủ loại vitamin này sẽ giảm nguy cơ ung thư đại trực tràng đến 31% 5 lợi ích tuyệt vời của khám sức khỏe định kỳ cá nhân
5 lợi ích tuyệt vời của khám sức khỏe định kỳ cá nhân Uống baking soda có thể giúp chữa ung thư
Uống baking soda có thể giúp chữa ung thư Giải độc gan bằng thực phẩm lành mạnh tại nhà
Giải độc gan bằng thực phẩm lành mạnh tại nhà Tai biến lần 2 vì thói quen dùng thuốc lại và không chịu tái khám
Tai biến lần 2 vì thói quen dùng thuốc lại và không chịu tái khám Bé gái "đen kịt" khi vào viện, cha mẹ cũng bỏng nặng trong vụ cháy ở TPHCM
Bé gái "đen kịt" khi vào viện, cha mẹ cũng bỏng nặng trong vụ cháy ở TPHCM Khoa học cảnh báo: Mất ngủ, dễ mắc 3 bệnh phổ biến này
Khoa học cảnh báo: Mất ngủ, dễ mắc 3 bệnh phổ biến này Nữ sinh 15 tuổi thủng tá tràng sau cơn đau dữ dội vùng thượng vị
Nữ sinh 15 tuổi thủng tá tràng sau cơn đau dữ dội vùng thượng vị Loại rau được đánh giá 'tốt nhất thế giới', ở nước ta mọc um tùm như cỏ
Loại rau được đánh giá 'tốt nhất thế giới', ở nước ta mọc um tùm như cỏ Sai lầm khi chạy bộ làm tăng nguy cơ đau tim
Sai lầm khi chạy bộ làm tăng nguy cơ đau tim Người lớn bị thủy đậu có được tắm không?
Người lớn bị thủy đậu có được tắm không? Nguyễn Đình Như Vân đăng quang Miss Global, BTC xin lỗi vì ồn ào 'đường lưỡi bò'
Nguyễn Đình Như Vân đăng quang Miss Global, BTC xin lỗi vì ồn ào 'đường lưỡi bò'
 Nữ ca sĩ 23 tuổi bị tấn công bằng dao đến mù mắt và hủy dung nhan, bản án cho kẻ ác gây phẫn nộ
Nữ ca sĩ 23 tuổi bị tấn công bằng dao đến mù mắt và hủy dung nhan, bản án cho kẻ ác gây phẫn nộ Đi nhà nghỉ với đồng nghiệp, đã được chồng tha thứ nhưng tôi luôn cảm thấy tội lỗi
Đi nhà nghỉ với đồng nghiệp, đã được chồng tha thứ nhưng tôi luôn cảm thấy tội lỗi Em chồng ngồi lướt điện thoại trong phòng để chị dâu bầu bì 8 tháng rửa 5 mâm bát, phản ứng của bố chồng khiến cả nhà náo loạn
Em chồng ngồi lướt điện thoại trong phòng để chị dâu bầu bì 8 tháng rửa 5 mâm bát, phản ứng của bố chồng khiến cả nhà náo loạn Xem phim "Sex Education" cùng chồng, tôi đỏ mặt NGƯỢNG NGÙNG vì một câu nói và đúc rút BÀI HỌC ĐẮT GIÁ trong hôn nhân
Xem phim "Sex Education" cùng chồng, tôi đỏ mặt NGƯỢNG NGÙNG vì một câu nói và đúc rút BÀI HỌC ĐẮT GIÁ trong hôn nhân Lòng vị tha của cha mẹ bị hại trong vụ án 'chồng giết vợ' do ghen tuông
Lòng vị tha của cha mẹ bị hại trong vụ án 'chồng giết vợ' do ghen tuông Nữ nghệ sĩ Việt gây phẫn nộ khi lan truyền hình ảnh thi hài cố diễn viên Quý Bình
Nữ nghệ sĩ Việt gây phẫn nộ khi lan truyền hình ảnh thi hài cố diễn viên Quý Bình Nói về Hòa Minzy mà bị chê "nhạt", NSND Tự Long đáp trả
Nói về Hòa Minzy mà bị chê "nhạt", NSND Tự Long đáp trả
 Nuôi đứa con bại não của cô gái quán bia suốt 25 năm, bà bán vé số đau đáu: "Phương ơi, con có còn sống không?"
Nuôi đứa con bại não của cô gái quán bia suốt 25 năm, bà bán vé số đau đáu: "Phương ơi, con có còn sống không?" "Cháy" nhất cõi mạng: Tập thể nam giảng viên một trường ĐH mặc váy múa ba lê mừng 8/3, còn bonus cú ngã của Jennifer Lawrence
"Cháy" nhất cõi mạng: Tập thể nam giảng viên một trường ĐH mặc váy múa ba lê mừng 8/3, còn bonus cú ngã của Jennifer Lawrence Lê Phương đăng ảnh nắm chặt tay Quý Bình, nghẹn ngào nói 6 chữ vĩnh biệt cố nghệ sĩ
Lê Phương đăng ảnh nắm chặt tay Quý Bình, nghẹn ngào nói 6 chữ vĩnh biệt cố nghệ sĩ "Vợ Quý Bình đẫm nước mắt, chỉ xuống đứa bé đứng dưới chân nói: Nè chị, con trai ảnh nè, ôm nó đi chị"
"Vợ Quý Bình đẫm nước mắt, chỉ xuống đứa bé đứng dưới chân nói: Nè chị, con trai ảnh nè, ôm nó đi chị"
 Lễ an táng diễn viên Quý Bình: Vợ tựa đầu ôm chặt di ảnh, Vân Trang và các nghệ sĩ bật khóc, nhiều người dân đội nắng tiễn đưa
Lễ an táng diễn viên Quý Bình: Vợ tựa đầu ôm chặt di ảnh, Vân Trang và các nghệ sĩ bật khóc, nhiều người dân đội nắng tiễn đưa Tang lễ diễn viên Quý Bình: Lặng lẽ không kèn trống, nghệ sĩ khóc nấc trước di ảnh
Tang lễ diễn viên Quý Bình: Lặng lẽ không kèn trống, nghệ sĩ khóc nấc trước di ảnh