Những lo ngại khi vaccine Oxford tạm dừng thử nghiệm
Vaccine Oxford tạm dừng thử nghiệm do có người bất ngờ nhiễm bệnh dấy lên nhiều lo ngại về tính an toàn của những “ứng viên” khác.
Mới đây, một trong những “ứng viên” tiềm năng nhất thời điểm hiện tại, vaccine Oxford, bất ngờ tạm dừng toàn bộ thử nghiệm lâm sàng khiến nhiều người lo lắng. Điều đó cho thấy việc kiểm chứng thực tế về khả năng phát triển lâm sàng và rủi ro về tính an toàn của một loại vaccine mới là rất quan trọng.
Việc một đơn vị nghiên cứu vaccine phải tạm dừng các thử nghiệm lâm sàng do có người nhiễm bệnh không mới, thậm chí khá quen thuộc trong ngành dược phẩm thế giới. Song nếu xét trong cuộc đua vaccine nCoV toàn cầu, các đơn vị nghiên cứu có thể sẽ nhìn nhận nghiêm túc về vấn đề này.
Giữa thời điểm cả thế giới đang chịu sự ảnh hưởng nặng nề do Covid-19, cú “vấp ngã” này của AstraZeneca như một lời nhắc nhở rằng vaccine mới có thể thất bại. Hoặc tệ hơn, một “ứng viên” kém an toàn có thể hại nhiều hơn lợi. Đồng thời đây cũng được xem như lời cảnh báo về các nguy cơ liên quan đến tính an toàn, đối với các hãng dược muốn đẩy nhanh tiến độ thử nghiệm hoặc mong muốn “ứng viên” của mình được chấp thuận sớm.
Sam Fazeli, một nhà phân tích của Bloomberg Intelligence, cho biết việc dừng thử nghiệm “ứng viên” của AstraZeneca “cho thấy nguy cơ của việc gấp rút đưa vaccine mới ra thị trường”.
“Không có bất cứ ‘ứng viên’ nào có thể bảo đảm 100% không mắc phải những rủi ro tương tự. Nhất là trong thời điểm hiện nay, các sản phẩm vaccine nCoV đang ở giai đoạn cuối của thử nghiệm lâm sàng, được tiêm cho hàng chục nghìn tình nguyện viên”, Sam Fazeli nói.
Mặt khác, Financial Times cho biết các cuộc thử nghiệm lâm sàng của AstraZeneca có thể được tiếp tục thực hiện vào đầu tuần tới. Quyết định tạm dừng thử nghiệm cho thấy tính kỷ luật, tôn trọng nguyên tắc an toàn các giai đoạn phát triển vaccine của hãng dược này. Song diễn biến này lại khiến những người đặt nhiều kỳ vọng vào sự tiến triển của một loại vaccine giúp chấm dứt Covid-19 cảm thấy hụt hẫng.
Theo AstraZeneca, các nhà nghiên cứu độc lập đang xem xét triệu chứng bệnh xuất hiện không rõ nguyên nhân của tình nguyện viên. Họ cần xác định rõ xem người đó nhiễm bệnh do tình cờ hay bắt nguồn từ việc thử vaccine.
Video đang HOT
Ugur Sahin, Giám đốc điều hành BioNTech cho biết nhóm bác sĩ điều hành thử nghiệm và các chuyên gia khác sẽ đánh giá trường hợp này. Nếu không tìm thấy mối liên hệ chặt chẽ nào giữa căn bệnh với vaccine Oxford, cuộc nghiên cứu có thể sẽ tiếp tục với các biện pháp đặc biệt, theo dõi sát sao để phát hiện kịp thời những trường hợp tương tự.
Các “đối thủ” của AstraZeneca lại không mấy lo lắng trước tin tức tạm dừng nghiên cứu của hãng dược này. Đơn cử như bộ đôi Pfizer – BioNTech, vẫn tự tin công bố rằng “ứng viên” của họ có thể cho kết quả thử nghiệm lâm sàng diện rộng vào tháng 10. Ngoài ra còn có Moderna, Sanofi và SinoVac cũng không bị lung lay bởi “cú vấp” này của AstraZeneca.
Vaccine của Moderna được thử nghiệm tại Viện Y tế Quốc gia. Ảnh: NY Times.
“Bất kỳ cuộc thử nghiệm vaccine trên người nào cũng phải thông qua phê duyệt nghiêm ngặt về mặt đạo đức. Thất bại lần này của AstraZeneca sẽ không ảnh hưởng đến kế hoạch hay tiến độ của SinoVac”, Liu Peicheng, phát ngôn viên của SinoVac cho biết.
Hai công ty Mỹ - Đức tuyên bố sắp có vaccine Covid-19
Hai công ty Pfizer và BioNTech tự tin tuyên bố sẽ có loại vaccine ngừa Covid-19 được phê duyệt vào giữa tháng 10 hoặc đầu tháng 11 tới.
"Nó có hồ sơ xuất sắc và tôi xem loại vaccine này gần như hoàn hảo", Ugur Sahin, giám đốc điều hành và đồng sáng lập công ty công nghệ sinh học BioNTech của Đức hôm nay nói về BNT162, loại vaccine ngừa Covid-19 đang hợp tác phát triển cùng công ty dược phẩm Mỹ Pfizer.
Hai công ty này cho biết họ dự định cung cấp 100 triệu liều BNT162 cho tới cuối năm nay và khoảng 1,3 tỷ liều vào năm sau.
Hồi tháng 7, Bộ Y tế và Dịch vụ Nhân sinh và Bộ Quốc phòng Mỹ thông báo thỏa thuận trị giá 1,95 tỷ USD với Pfizer để sản xuất 100 triệu liều vaccine Covid-19. Thỏa thuận này cũng cho phép chính phủ Mỹ mua thêm 500 triệu liều.
Sahin chi sẻ ông tin rằng việc cấp phép sử dụng khẩn cấp đối với ứng viên vaccine này sẽ nhanh chóng được cơ quan chức năng thông qua, thêm rằng "sự hiểu biết về phương thức hoạt động cùng với dữ liệu an toàn từ quá trình thử nghiệm" khiến họ có rất nhiều niềm tin với BNT162.
"Chúng tôi tin rằng mình sẽ có sản phẩm an toàn và cũng tin rằng có thể chứng minh nó hiệu quả", ông nói.
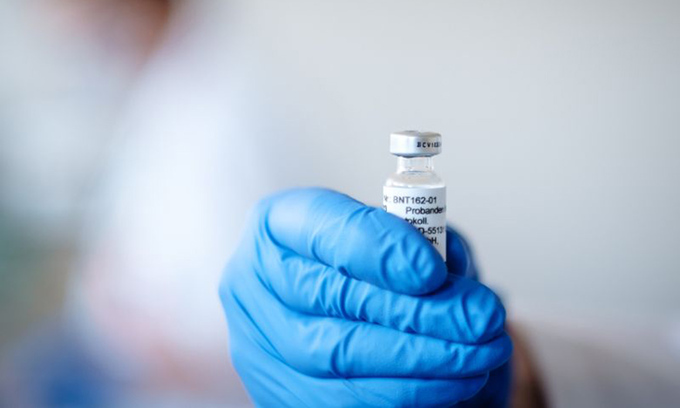
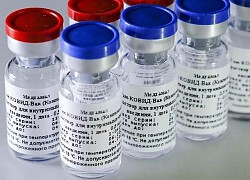
Một mẫu thử của loại vaccine BNT162 do Pfizer và BioNTech phát triển. Ảnh: BioNTech SE.
CEO của BioNTech cho biết thử nghiệm lâm sàng trên người già và người trưởng thành còn trẻ cho thấy phản ứng của kháng thể rất mạnh mẽ, với rất tác dụng phụ tối thiểu.
"Chỉ có một bộ phận nhỏ tham gia thử nghiệm bị sốt", Sahin nói. "Chúng tôi cũng thấy rất ít xuất hiện triệu chứng đau đầu và mệt mỏi. Các triệu chứng này xuất hiện ở người tiêm vaccine chỉ là tạm thời và thường biến mất sau một, hai ngày".
Dù BioNTech và Pfizer tin rằng loại vaccine của họ sẽ có thể được phê duyệt vào giữa tháng 10, nhiều quan chức liên bang lại cho rằng đây là mốc thời gian "quá lạc quan".
"Tôi chưa thấy bất kỳ nhà khoa học nào liên quan tới nỗ lực phát triển vaccine cho rằng chúng ta sẽ có các mũi tiêm trước ngày bầu cử 3/11", một quan chức nắm rõ dự án phát triển vaccine thần tốc của chính phủ Mỹ Operation Warp Speed, nói.
Song Moncef Slaoui, cố vấn trưởng của Operation Warp Speed, tuần trước nói với NPR rằng "cực kỳ khó xảy ra nhưng không phải là không thể" để một loại vaccine Covid-19 được Cục Quản lý Thực phẩm và Dược phẩm Mỹ (FDA) cấp phép sử dụng khẩn cấp trước cuối tháng 10.
Tổng thống Mỹ Donald Trump cũng nhiều lần nói rằng ông "lạc quan" về một loại vaccine được phê duyệt sử dụng trước ngày 3/11. "Chúng ta sẽ sớm có vaccine, có thể là trước ngày đặc biệt. Các bạn biết tôi muốn nói đến ngày nào rồi đó", Trump nói tại họp báo hôm 7/9.
BioNTech và Pfizer là hai trong số 9 công ty dược phẩm đã ký cam kết duy trì "tiêu chuẩn đạo đức cao", trong đó nêu rõ họ không được xin chính phủ cấp phép sớm cho vaccine.
Tuy nhiên, Sahin nói rằng hai công ty sẽ nhanh chóng nộp đơn xin cấp phép cho ứng viên BNT162 bởi tin rằng đã hoàn thiện quy trình đầy đủ.
"Tôi tin rằng với việc chúng tôi đã hoàn tất quy trình đầy đủ theo yêu cầu phát triển vaccine gồm nghiên cứu khoa học, nghiên cứu tiền lâm sàng, thử nghiệm khả năng tiếp nhận an toàn và thử nghiệm tính hiệu quả, không cần thêm quá nhiều thời gian giữa việc cấp phép sử dụng khẩn cấp và cấp phép hoàn toàn nữa", Sahin nói.
BNT162 của BioNTech và Pfizer là một trong số 34 loại vaccine đang được thử nghiệm lâm sàng trên toàn cầu, theo Tổ chức Y tế Thế giới.
Trung Quốc tiêm thử vaccine Covid-19 cho hàng trăm nghìn người  Hàng trăm nghìn người Trung Quốc đã tiêm vaccine Covid-19 thử nghiệm theo chương trình khẩn cấp của chính phủ. Hai loại vaccine thử nghiệm được phát triển bởi Công ty Công nghệ Sinh học Quốc gia Trung Quốc (CNBG). Zhou Song, thư ký ủy ban kiểm tra kỷ luật của CNBG, cho biết thời gian duy trì bảo vệ đối với người...
Hàng trăm nghìn người Trung Quốc đã tiêm vaccine Covid-19 thử nghiệm theo chương trình khẩn cấp của chính phủ. Hai loại vaccine thử nghiệm được phát triển bởi Công ty Công nghệ Sinh học Quốc gia Trung Quốc (CNBG). Zhou Song, thư ký ủy ban kiểm tra kỷ luật của CNBG, cho biết thời gian duy trì bảo vệ đối với người...
 Trung Quốc tung chatbot đấu ChatGPT, cổ phiếu Phố Wall chao đảo bốc hơi 1.000 tỉ14:53
Trung Quốc tung chatbot đấu ChatGPT, cổ phiếu Phố Wall chao đảo bốc hơi 1.000 tỉ14:53 Ông Trump dọa trừng phạt Nga nếu ông Putin từ chối đàm phán chấm dứt chiến sự Ukraine09:59
Ông Trump dọa trừng phạt Nga nếu ông Putin từ chối đàm phán chấm dứt chiến sự Ukraine09:59 Tình báo Israel cài thuốc nổ trong máy ly tâm hạt nhân Iran09:17
Tình báo Israel cài thuốc nổ trong máy ly tâm hạt nhân Iran09:17 Trung Quốc, Đức phản ứng sau khi ông Trump ký sắc lệnh rút khỏi WHO01:49
Trung Quốc, Đức phản ứng sau khi ông Trump ký sắc lệnh rút khỏi WHO01:49 Ông Trump nói muốn gặp ông Putin ngay lập tức08:46
Ông Trump nói muốn gặp ông Putin ngay lập tức08:46 Tàu vận tải Nga cập cảng Syria, chuẩn bị cho cuộc rút quân09:12
Tàu vận tải Nga cập cảng Syria, chuẩn bị cho cuộc rút quân09:12 Ông Trump và ông Biden đều nhận công về thỏa thuận ngừng bắn ở Gaza09:00
Ông Trump và ông Biden đều nhận công về thỏa thuận ngừng bắn ở Gaza09:00 Căn cứ hải quân ngầm ở độ sâu 500 m của Iran08:37
Căn cứ hải quân ngầm ở độ sâu 500 m của Iran08:37 "Hỏa thần nhiệt áp" Nga ra đòn, nhằm thẳng cứ điểm Ukraine ở Kursk08:59
"Hỏa thần nhiệt áp" Nga ra đòn, nhằm thẳng cứ điểm Ukraine ở Kursk08:59 Phe ông Yoon cáo buộc lãnh đạo cơ quan điều tra 'vi phạm bí mật quân sự'09:51
Phe ông Yoon cáo buộc lãnh đạo cơ quan điều tra 'vi phạm bí mật quân sự'09:51 Trung Quốc thông báo điện đàm ông Tập-ông Trump, TikTok không qua ải Tòa Tối cao Mỹ09:17
Trung Quốc thông báo điện đàm ông Tập-ông Trump, TikTok không qua ải Tòa Tối cao Mỹ09:17Tiêu điểm
Tin đang nóng
Tin mới nhất

Tổng thống Trump có những đòn bẩy gì với Nga trong đàm phán hòa bình về Ukraine?

Israel hoãn trả tự do cho các tù nhân Palestine

Đến thăm thị trấn Tân Hội ở Trung Quốc, nơi 'vàng' mọc trên cây

Thời báo Tài chính Anh: EU cân nhắc nối lại nhập khẩu khí đốt từ Liên bang Nga

Va chạm máy bay tại Mỹ: Thợ lặn tìm thấy một hộp đen dưới sông Potomac

Đối tượng nhiều lần đốt kinh Koran tại Thụy Điển bị sát hại

Tranh cãi về lớp học đầu tiên không có giáo viên tại Anh

Vụ va chạm máy bay trên không ở Washington DC: không có người sống sót

Tổng thống Trump lên tiếng về 'thảm kịch' hàng không ở thủ đô Washington DC

Hamas thả 3 con tin Israel đổi lấy 110 tù nhân Palestine

Nhật yêu cầu 1,2 triệu người hạn chế tắm để cứu tài xế khỏi 'hố tử thần'

Hàn Quốc sắp nhận trực thăng mới từ Mỹ để đối phó tàu ngầm Triều Tiên
Có thể bạn quan tâm

Tuổi 27 nổi tiếng, giàu có, Hoàng Đức tiết lộ hình mẫu lý tưởng muốn cưới làm vợ, một yếu tố gây bất ngờ
Sao thể thao
14:04:29 31/01/2025
5 Gen Z tuổi rắn hội tụ đủ combo xinh - giàu - giỏi
Netizen
13:43:17 31/01/2025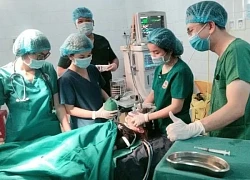
Bác sĩ cảnh báo nguy cơ dị vật đường thở ở trẻ dịp tết
Sức khỏe
13:32:33 31/01/2025
Đôi lời nhắn gửi tuổi Tỵ khi bước sang NĂM TUỔI Ất Tỵ 2025: Cung nghênh Thái Tuế, rước lộc trừ tà
Trắc nghiệm
12:12:11 31/01/2025
Gợi ý áo dài màu pastel cho nàng yêu sự nhẹ nhàng
Thời trang
12:06:20 31/01/2025
Lịch thi đấu LCK Cup 2025 mới nhất: Chờ đội hình T1
Mọt game
11:11:23 31/01/2025
Tôi chân thành nhắc bạn: Lau sạch 5 nơi này vào ngày đầu năm để "khai thông tài vận", giũ sạch tà khí
Sáng tạo
10:47:53 31/01/2025
Thấy chị gái mặc cái váy nhàu nhĩ, tôi kéo vào phòng hỏi thì sững người khi chị tiết lộ bí mật động trời
Góc tâm tình
09:50:39 31/01/2025
Phim Hàn gây bão toàn cầu nhất định phải xem dịp Tết, 1 mỹ nam đẹp ăn đứt truyện tranh gây sốt MXH
Phim châu á
09:25:04 31/01/2025
Khoảnh khắc đốt mắt khiến dân tình không nhận ra nữ thần đẹp nhất nhóm đại mỹ nhân
Nhạc quốc tế
09:21:29 31/01/2025
 Một thời ‘ăn chanh phòng dịch’
Một thời ‘ăn chanh phòng dịch’ Thủ đô Indonesia tái áp đặt lệnh hạn chế do Covid-19
Thủ đô Indonesia tái áp đặt lệnh hạn chế do Covid-19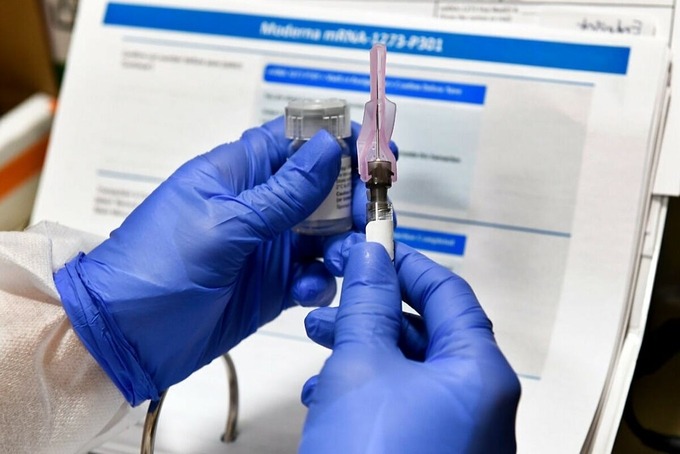
 Chủ nghĩa dân tộc phủ bóng cuộc đua vaccine Covid-19
Chủ nghĩa dân tộc phủ bóng cuộc đua vaccine Covid-19
 Nga ký thỏa thuận với Ấn Độ để sản xuất vaccine Sputnik V
Nga ký thỏa thuận với Ấn Độ để sản xuất vaccine Sputnik V Trump thúc cấp phép vaccine Covid-19 trước ngày bầu cử
Trump thúc cấp phép vaccine Covid-19 trước ngày bầu cử Kịch bản Mỹ thất thế trong cuộc đua vaccine với Trung Quốc
Kịch bản Mỹ thất thế trong cuộc đua vaccine với Trung Quốc Nga nói phương Tây học theo cách tiếp cận về vaccine Covid-19
Nga nói phương Tây học theo cách tiếp cận về vaccine Covid-19 Mỹ công bố ảnh chân dung mới của Đệ nhất phu nhân Melania Trump
Mỹ công bố ảnh chân dung mới của Đệ nhất phu nhân Melania Trump Vụ va chạm máy bay tại Mỹ: Tìm thấy 19 thi thể tại hiện trường
Vụ va chạm máy bay tại Mỹ: Tìm thấy 19 thi thể tại hiện trường Lời nguyện ước cuối cùng của chàng trai chết não hiến tạng cứu 5 người
Lời nguyện ước cuối cùng của chàng trai chết não hiến tạng cứu 5 người Nhật Bản gặp khó khi xử lý 'hố tử thần'
Nhật Bản gặp khó khi xử lý 'hố tử thần' Sai lầm khiến loạt lữ đoàn Ukraine "chưa đánh đã tan" ở chảo lửa Donetsk
Sai lầm khiến loạt lữ đoàn Ukraine "chưa đánh đã tan" ở chảo lửa Donetsk Mỹ dừng nhận người tị nạn Ukraine, xe đâm vào Đại sứ quán Nga ở Thụy Điển
Mỹ dừng nhận người tị nạn Ukraine, xe đâm vào Đại sứ quán Nga ở Thụy Điển Thẩm phán Mỹ chặn sắc lệnh của ông Trump
Thẩm phán Mỹ chặn sắc lệnh của ông Trump Pháp có thể triển khai quân đến Greenland
Pháp có thể triển khai quân đến Greenland Bát bún riêu 400k ngày Tết khiến dân mạng "dậy sóng", chủ quán lên tiếng khiến nhiều người bất ngờ khi biết lý do
Bát bún riêu 400k ngày Tết khiến dân mạng "dậy sóng", chủ quán lên tiếng khiến nhiều người bất ngờ khi biết lý do Đắng cay nhạc Việt: Thời của nhan sắc?
Đắng cay nhạc Việt: Thời của nhan sắc? Nhìn anh nhân viên của chị dâu mặc tạp dề chặt thịt gà thoăn thoắt, tôi nói một câu làm anh ấy kinh ngạc
Nhìn anh nhân viên của chị dâu mặc tạp dề chặt thịt gà thoăn thoắt, tôi nói một câu làm anh ấy kinh ngạc Cô gái nhiều năm không đi chúc Tết họ hàng, lý do khiến bố mẹ bức xúc
Cô gái nhiều năm không đi chúc Tết họ hàng, lý do khiến bố mẹ bức xúc Cạnh tranh làm ăn, ném mắm tôm vào cửa hàng đối thủ sáng mùng 1 Tết
Cạnh tranh làm ăn, ném mắm tôm vào cửa hàng đối thủ sáng mùng 1 Tết Về nhà vợ chúc Tết thì bất ngờ khi ông bà chia tài sản, vợ con tôi được thừa kế những thứ khiến tôi kinh ngạc khó tin
Về nhà vợ chúc Tết thì bất ngờ khi ông bà chia tài sản, vợ con tôi được thừa kế những thứ khiến tôi kinh ngạc khó tin Phá trường gà ngày mùng 2 Tết, tóm 72 con bạc, thu giữ gần nửa tỷ đồng
Phá trường gà ngày mùng 2 Tết, tóm 72 con bạc, thu giữ gần nửa tỷ đồng 3 con giáp "tiền vào như nước" nếu đầu tư vào vàng bạc, trang sức trong năm Ất Tỵ 2025!
3 con giáp "tiền vào như nước" nếu đầu tư vào vàng bạc, trang sức trong năm Ất Tỵ 2025! Điều tra vụ án sát hại mẹ và anh trai vào sáng mùng 2 Tết
Điều tra vụ án sát hại mẹ và anh trai vào sáng mùng 2 Tết HOT: Đúng mùng 1 Tết, phu nhân hào môn Vbiz và chồng đại gia thông báo đã đón con đầu lòng!
HOT: Đúng mùng 1 Tết, phu nhân hào môn Vbiz và chồng đại gia thông báo đã đón con đầu lòng!
 Ô tô mất lái lao xuống sông ở Nam Định, 7 người tử vong
Ô tô mất lái lao xuống sông ở Nam Định, 7 người tử vong BVĐK Vĩnh Long thông tin về vụ bé gái 3 tuổi tử vong đêm giao thừa
BVĐK Vĩnh Long thông tin về vụ bé gái 3 tuổi tử vong đêm giao thừa Nguyên nhân khiến em trai xuống tay sát hại mẹ và anh vào sáng mùng 2 Tết
Nguyên nhân khiến em trai xuống tay sát hại mẹ và anh vào sáng mùng 2 Tết
 Ảnh hiếm: Xuân Trường ôm vợ giám đốc đi chúc tết, nhan sắc Nhuệ Giang thế nào 4 năm sau đám hỏi bí mật?
Ảnh hiếm: Xuân Trường ôm vợ giám đốc đi chúc tết, nhan sắc Nhuệ Giang thế nào 4 năm sau đám hỏi bí mật? Quang Hải khoe ảnh cùng con trai mặc áo dài đi chơi tết, HLV Park Hang-seo liền có phản ứng này
Quang Hải khoe ảnh cùng con trai mặc áo dài đi chơi tết, HLV Park Hang-seo liền có phản ứng này Vũ trụ mỹ nhân Việt nhập đường đua mùng 1 Tết: Thùy Tiên - Thanh Thủy đọ sắc bất phân thắng bại
Vũ trụ mỹ nhân Việt nhập đường đua mùng 1 Tết: Thùy Tiên - Thanh Thủy đọ sắc bất phân thắng bại