Nhà khoa học đứng sau đột phá vaccine Moderna
Giám đốc Y tế hãng dược Moderna Tal Zaks, cùng với Melissa Moore, Giám đốc Khoa học, là hai bộ óc tạo nên “phép màu” của vaccine mRNA-1273.
Vaccine mRNA-1273 đạt hiệu quả 94,5% ngăn ngừa Covid-19, giúp Moderna trở thành nhà sản xuất dược phẩm thứ hai Mỹ gặt hái thành công trong cuộc đua vaccine thế giới. Cùng với vaccine của Pfizer, hiệu quả hơn 90%, Mỹ có thể có hai loại vaccine được phép sử dụng khẩn cấp vào tháng 12 với khoảng 60 triệu liều.
Vào tháng 3, khi cuộc khủng hoảng Covid-19 toàn cầu trở nên rõ ràng, Tổng thống Mỹ Donald Trump đã mời một nhóm lãnh đạo các công ty dược phẩm lớn đến Nhà Trắng. Tại cuộc họp đó, Stéphane Bancel, CEO của công ty công nghệ sinh học Moderna, đã báo cáo về khả năng công ty của ông có thể nghiên cứu thành công vaccine trong vòng vài tháng. Ngày 16/11, Moderna công bố vaccine thử nghiệm của công ty có hiệu quả 94,5% trong việc ngăn ngừa Covid -19.
Melissa Moore, Giám đốc Khoa học của Moderna phụ trách công nghệ mRNA . Ảnh: Umass
Nhà nghiên cứu đứng sau thành công
Đứng sau thành công bước đầu rất quan trọng này của Moderna là nhóm các nhà khoa học của Moderna. Dẫn đầu là Giám đốc Y tế Tal Zaks, cùng với Melissa Moore, Giám đốc Khoa học của Moderna phụ trách công nghệ mRNA.
Video đang HOT
Tal Zaks, nhà khoa học từng là cựu trưởng khoa ung thư toàn cầu tại Sanofi (một công ty dược của Pháp), vui mừng trước việc công bố hiệu quả tích cực của vaccine: “Đây là một trong những khoảnh khắc tuyệt vời trong cuộc đời và sự nghiệp của tôi”.
Ngoài sự dẫn dắt của Tal Zaks, Melissa Moore, giám đốc khoa học của Moderna phụ trách công nghệ mRNA, chính là nhân vật quan trọng hàng đầu cho nỗ lực này.
Moore là nhà nghiên cứu lĩnh vực sinh hóa, chuyên nghiên cứu về phân tích cấu trúc protein. Từ khi còn là một nhà nghiên cứu trẻ tại Học viện Công nghệ Massachusetts (MIT) vào đầu những năm 1990, cô đã chuyên tâm nghiên cứu về mRNA, một công nghệ mới. Năm 2013, cô quyết định chuyển sang làm việc cho Moderna.
Trong một email gửi Tiến sĩ Tony de Fougerolles, lúc đó là giám đốc khoa học của Moderna, Moore tự tin về khả năng của mình trong lĩnh vực mRNA. Tiến sĩ De Fougerolles mời cô tham gia ban cố vấn khoa học của mình. Năm 2016, Moore thôi giữ chức vụ giáo sư có thời hạn tại Trường Y Đại học Massachusetts ở Worcester để tiếp nhận vai trò của De Fougerolles tại công ty Moderna.
Trao đổi với tạp chí Science năm 2017, Moore nói: “Tôi có thể dành 15 năm tiếp theo để tiếp tục công việc giáo sư, viết nhiều bài báo hơn, đào tạo nhiều sinh viên hơn. Nhưng khi tôi già đi và nhìn lại cuộc đời mình, tôi có thể sẽ cảm thấy hối tiếc nếu quyết định như vậy”.
Kể từ khi Moore gia nhập, các nghiên cứu của cô đã giúp Moderna phát triển thành một công ty công nghệ sinh học lớn, đã sản xuất 23 loại thuốc mRNA và vaccine trong danh mục của công ty, chẳng hạn như vaccine cho virus Zika, một số loại vaccine cúm gia cầm, với 14 loại đang được nghiên cứu lâm sàng. Tuy vậy, những thành quả này chưa đủ để làm nên thành công cho công ty. Với việc bùng phát dịch bệnh Covid – 19, công ty đã được chính phủ Mỹ tài trợ để phát triển vaccine một cách nhanh chóng.
Sau các thông tin về thành công bước đầu trong việc thử nghiệm vaccine Covid-19, cổ phiếu của công ty đã tăng vọt. Từ dao động quanh mức 20 USD trong hai năm qua, sau tin tức đưa ra ngày 16/11, cổ phiếu của công ty đã lên mức hơn 95 USD, định giá công ty khoảng 38 tỷ USD.
Moderna thành lập năm 2010 với ý tưởng rằng công nghệ mRNA – phân tử gửi các hướng dẫn di truyền từ gene đến bộ máy tạo protein của tế bào – có thể được tái thiết kế để phát triển thuốc và vaccine.
Moderna hoàn tất thử nghiệm vaccine Covid-19 giai đoạn 3
Hãng dược Moderna cho biết đã hoàn thành thử nghiệm vaccine giai đoạn 3 cho 30.000 tình nguyện viên tham gia.
Quá trình nghiên cứu được theo dõi chặt chẽ để đảm bảo sự đa dạng tình nguyện viên. Theo dữ liệu của công ty, 1/5 tình nguyện viên đến từ Tây Ban Nha và 10% là người da đen. Tình nguyện viên trên 65 tuổi, đối tượng có nguy cơ cao nhiễm nCoV, chiếm 25%.
"Tôi nghĩ rằng chúng tôi đang làm khá tốt, yếu tố nhân khẩu của thử nghiệm vaccine Moderna khá đa dạng", Larry Corey, chuyên gia virus tại Trung tâm Nghiên cứu Ung thư Fred Hutchinson, nhận định. Ông Corey đang tiến hành các thử nghiệm lâm sàng trong Chiến dịch Thần tốc - nỗ lực liên bang nhằm đẩy nhanh tiến độ phát triển vaccine.
"Chúng tôi hy vọng sẽ tiếp tục cải thiện điều này. Đây mới là thử nghiệm đầu tiên hoàn thành, chúng ta còn hai loại khác nữa. Chặng đường đến với vaccine Covid-19 chỉ mới bắt đầu", ông Corey nói, đề cập đến hai loại vaccine khác của hai nhà nghiên cứu Pfizer và Johnson & Johnson.
Hơn một nửa số tình nguyện viên của Moderna đều là người khỏe mạnh, không dễ nhiễm nCoV. 25% khác là người cao tuổi, 17% trẻ hơn, song mắc các bệnh nền như tiểu đường hoặc béo phì, khiến họ nằm trong nhóm rủi ro cao.
Dữ liệu đánh giá thử nghiệm vaccine của Moderna được lưu tại Trung tâm nghiên cứu Mỹ ở Hollywood, Florida. Ảnh: AFP
Tiến sĩ Stephen Hoge, chủ tịch của Moderna, cho biết chủng ngừa cho 30.000 tình nguyện viên "chỉ là cột mốc quan trọng, không phải thành tựu". 50% trong đó đã nhận vaccine, số còn lại tiêm giả dược là nước muối sinh lý. Hai mũi tiêm cách nhau 4 tuần.
Moderna dự kiến công bố dữ liệu sơ bộ của thử nghiệm giai đoạn 3 trong tháng 11. Sau hai tháng theo dõi, công ty sẽ xác định liệu sản phẩm có đủ tiêu chuẩn đệ trình lên cơ quan quản lý để xin cấp phép hay không. Họ kỳ vọng hoàn thành toàn bộ quá trình trước Lễ Tạ ơn, ngày 26/11 năm nay.
Hiện Moderna, Pfizer và Johnson & Johnson là ba hãng dược dẫn đầu cuộc đua phát triển vaccine tại Mỹ. Moderna khởi động thử nghiệm giai đoạn 3 ngày 27/2, cùng ngày với Pfizer. Vaccine do Johnson & Johnson sản xuất bắt đầu tiêm thử ngày 23/9, song phải ngừng sau chưa đầy ba tuần vì một tình nguyện viên bị ốm. AstraZeneca, hãng dược của Anh, gặp tình trạng tương tự.
Thử nghiệm lâm sàng các loại vaccine bao gồm ba giai đoạn. Ở giai đoạn một, các nhà khoa học tiêm vaccine cho số tình nguyện viên hạn chế để kiểm tra độ an toàn và xác định liều lượng. Giai đoạn hai, thử nghiệm diễn ra trên hàng trăm người, chia thành các nhóm, chẳng hạn trẻ em, người già, để xem liệu liều tiêm có tạo ra phản ứng khác nhau ở từng đối tượng hay không. Trong thử nghiệm giai đoạn ba, các nhà nghiên cứu tiêm vaccine hoặc giả dược trên hàng chục nghìn người, chia làm hai nhóm. Tình nguyện sau đó trở về vùng dịch sinh sống nhằm so sánh tỷ lệ lây nhiễm.
Sau thử nghiệm giai đoạn ba, đơn vị nghiên cứu sẽ đệ trình dữ liệu lên cơ quan quản lý để xin cấp phép. Trong thời kỳ đại dịch, một số loại vaccine được phê duyệt khẩn cấp khi đang trong nghiên cứu giai đoạn 3.
Khi đã được cơ quan quản lý chấp thuận, các nhà nghiên cứu tiếp tục theo dõi phản ứng của nhóm tình nguyện viên nhằm tìm ra các tác dụng phụ tiềm ẩn. Đây gọi là quá trình đánh giá sau phê duyệt. Nếu vaccine được chứng minh là an toàn và hiệu quả, nhà sản xuất sẽ tiến hành phân phối hàng loạt đến các cơ sở y tế, phục vụ cho chương trình tiêm chủng.
Thông thường toàn bộ quy trình từ nghiên cứu đến cấp phép, phân phối ra thị trường của một loại vaccine mới mất ít nhất hai năm. Trong bối cảnh Covid-19 lan rộng, một số chính phủ thúc đẩy quá trình nghiên cứu cấp phép vaccine này nhanh hơn bình thường. Thậm chí Nga đã cấp phép cho hai loại vaccine Covid-19 trước khi tiến hành các giai đoạn thử nghiệm lâm sàng, dẫn đến nhiều hoài nghi của các nhà khoa học về chất lượng sản phẩm.
Đến nay 6 loại vaccine Covid-19 được phê duyệt khẩn cấp, đều thuộc về Trung Quốc và Nga. Hai "ứng viên" của Nga là Sputnik V và EpiVacCorona. Bốn loại vaccine của Trung Quốc do hãng dược nhà nước và các Viện Sinh phẩm điều chế, chủ yếu dựa trên virus bất hoạt.
5 người gặp phản ứng phụ khi tham gia thử nghiệm 2 loại vaccine Covid-19 hàng đầu tại Mỹ  Cả 5 người tham gia thử nghiệm cho biết họ bị sốt cao, đau nhức cơ thể, đau đầu, kiệt sức suốt cả ngày và các triệu chứng khác sau khi tiêm. 5 trong số những tình nguyện viên người Mỹ tham gia thử nghiệm giai đoạn cuối loại vaccine ngừa Covid-19 tiềm năng của hai hãng Moderna và Pfizer đã bắt gặp...
Cả 5 người tham gia thử nghiệm cho biết họ bị sốt cao, đau nhức cơ thể, đau đầu, kiệt sức suốt cả ngày và các triệu chứng khác sau khi tiêm. 5 trong số những tình nguyện viên người Mỹ tham gia thử nghiệm giai đoạn cuối loại vaccine ngừa Covid-19 tiềm năng của hai hãng Moderna và Pfizer đã bắt gặp...
 Nội bộ Mỹ mâu thuẫn về Ukraine?08:24
Nội bộ Mỹ mâu thuẫn về Ukraine?08:24 Nga liên lạc với 'lực lượng mạnh nhất' ở Syria14:18
Nga liên lạc với 'lực lượng mạnh nhất' ở Syria14:18 Trăn khổng lồ xuất hiện trên đường ngập nước sau trận mưa lớn08:31
Trăn khổng lồ xuất hiện trên đường ngập nước sau trận mưa lớn08:31 Triều Tiên lần đầu lên tiếng về vụ thiết quân luật Hàn Quốc09:01
Triều Tiên lần đầu lên tiếng về vụ thiết quân luật Hàn Quốc09:01 Nga phóng gần 300 tên lửa và UAV, Ukraine điều F-16 ứng phó?08:24
Nga phóng gần 300 tên lửa và UAV, Ukraine điều F-16 ứng phó?08:24 Mỹ tấn công mục tiêu ở Syria, Iran cân nhắc triển khai quân08:28
Mỹ tấn công mục tiêu ở Syria, Iran cân nhắc triển khai quân08:28 Nga tuyên bố chưa thể đàm phán với Ukraine08:20
Nga tuyên bố chưa thể đàm phán với Ukraine08:20 2024 sẽ trở thành năm nóng nhất lịch sử00:53
2024 sẽ trở thành năm nóng nhất lịch sử00:53 Trung Quốc triển khai gần 90 tàu, Đài Loan nâng mức báo động?19:25
Trung Quốc triển khai gần 90 tàu, Đài Loan nâng mức báo động?19:25 Ông Trump nói Canada, Mexico nên thành tiểu bang Mỹ vì đang nhận 'trợ cấp'08:37
Ông Trump nói Canada, Mexico nên thành tiểu bang Mỹ vì đang nhận 'trợ cấp'08:37 Xuồng không người lái Ukraine 'gây thảm họa' cho hạm đội Nga?09:18
Xuồng không người lái Ukraine 'gây thảm họa' cho hạm đội Nga?09:18Tiêu điểm
Tin đang nóng
Tin mới nhất

Tổng thống Hàn Quốc không trình diện để cung cấp lời khai

Chính phủ mới Syria muốn Nga 'xem xét lại' hiện diện quân sự

CEO TikTok gặp riêng ông Trump, tìm cách ngăn lệnh cấm ở Mỹ

Thẩm phán ra phán quyết mới bất lợi cho ông Trump về vụ chi tiền bịt miệng

Nga phải sẵn sàng chiến đấu với NATO trong thập niên tới

Người đàn ông phát hiện u phổi ác tính từ dấu hiệu không ngờ

Tổng thống Hàn Quốc đối mặt bê bối mới liên quan đến nhà ngoại cảm

Nga sẽ đưa vụ Ukraine ám sát tướng cấp cao ra cuộc họp của Liên hợp quốc

Boeing nối lại tất cả các chương trình sản xuất máy bay

Hà Lan phạt Netflix gần 5 triệu USD vì cách xử lý dữ liệu người dùng

IEA dự báo lượng than đá sử dụng tăng cao kỷ lục lên 8,7 tỷ tấn

Israel ra điều kiện rút quân khỏi vùng đệm với Syria
Có thể bạn quan tâm

Hoa hậu Việt ồ ạt đi thi quốc tế, mấy người giành vương miện?
Sao việt
08:10:29 19/12/2024
Đưa dì út mỗi tháng 10 triệu chăm mẹ già bị liệt, mẹ tôi bật khóc tức giận khi lật chiếc chăn của bà ngoại lên
Góc tâm tình
08:07:58 19/12/2024
Choáng ngợp trước khoảnh khắc 'nhật chiếu kim sơn" trên đỉnh núi tuyết 7.500 m
Du lịch
07:47:52 19/12/2024
Lý do quán 'Hát cho nhau nghe' bị phóng hỏa khiến 11 người tử vong ở Hà Nội
Pháp luật
07:27:43 19/12/2024
Không thời gian - Tập 14: Đại gặp rắc rối
Phim việt
07:13:25 19/12/2024
Quả trứng 'siêu quý hiếm' được bán với giá 6 triệu đồng
Lạ vui
06:52:00 19/12/2024
Phim Hàn kịch tính tột độ được khán giả Việt khen nức nở: Dàn cast đỉnh cao, xem mà tim đập thình thịch "7749" hướng
Phim châu á
06:08:06 19/12/2024
Điện ảnh Việt năm 2024: Phim kinh dị lên ngôi
Hậu trường phim
06:07:32 19/12/2024
Nhân chứng và camera ghi hình ảnh kẻ đổ xăng phóng hỏa quán ở Phạm Văn Đồng
Tin nổi bật
06:05:34 19/12/2024
Cách làm món bò hầm trứng cút lạ miệng, hấp dẫn
Ẩm thực
06:00:54 19/12/2024
 Moderna bán vaccine Covid-19 giá đắt đỏ
Moderna bán vaccine Covid-19 giá đắt đỏ Nghìn ô tô xếp hàng trước điểm cứu trợ thực phẩm
Nghìn ô tô xếp hàng trước điểm cứu trợ thực phẩm

 Vaccine Oxford 'hẹn' ra mắt cuối năm nay
Vaccine Oxford 'hẹn' ra mắt cuối năm nay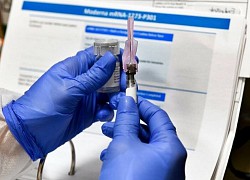 Những lo ngại khi vaccine Oxford tạm dừng thử nghiệm
Những lo ngại khi vaccine Oxford tạm dừng thử nghiệm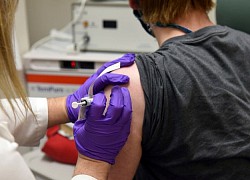 Mỹ thử nghiệm vaccine Covid-19 quy mô lớn
Mỹ thử nghiệm vaccine Covid-19 quy mô lớn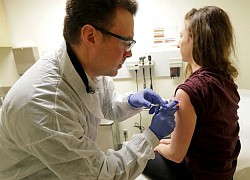 Vaccine Covid-19 Mỹ đầu tiên được bình duyệt
Vaccine Covid-19 Mỹ đầu tiên được bình duyệt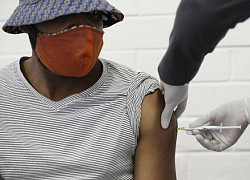 Tháng 7 quyết định cuộc đua vaccine
Tháng 7 quyết định cuộc đua vaccine Vaccine tiến đến giai đoạn thử nghiệm cuối cùng
Vaccine tiến đến giai đoạn thử nghiệm cuối cùng Ông Trump: Xung đột Nga - Ukraine phải chấm dứt
Ông Trump: Xung đột Nga - Ukraine phải chấm dứt Khai "lố" tuổi để lấy vợ, 28 năm sau người chồng ra tòa yêu cầu hủy hôn
Khai "lố" tuổi để lấy vợ, 28 năm sau người chồng ra tòa yêu cầu hủy hôn Mỹ sắp trừng phạt mạnh tay đội tàu "dầu bóng tối" của Nga
Mỹ sắp trừng phạt mạnh tay đội tàu "dầu bóng tối" của Nga Dùng xe tải 5 tấn và 20 người hỗ trợ chôn cất người đàn ông nặng 420kg
Dùng xe tải 5 tấn và 20 người hỗ trợ chôn cất người đàn ông nặng 420kg Bitcoin tiến sát kỷ lục 108.000 USD sau phát biểu của Tổng thống Trump
Bitcoin tiến sát kỷ lục 108.000 USD sau phát biểu của Tổng thống Trump Trung Quốc tăng thời gian quá cảnh miễn thị thực cho công dân từ 54 nước
Trung Quốc tăng thời gian quá cảnh miễn thị thực cho công dân từ 54 nước Nữ sinh 15 tuổi nổ súng sát hại 2 người tại trường học Mỹ
Nữ sinh 15 tuổi nổ súng sát hại 2 người tại trường học Mỹ Ông Trump xem xét đề xuất ngừng bắn giữa Nga, Ukraine vào Giáng sinh
Ông Trump xem xét đề xuất ngừng bắn giữa Nga, Ukraine vào Giáng sinh Cháy quán cà phê 11 người tử vong: Lời khai của nghi phạm
Cháy quán cà phê 11 người tử vong: Lời khai của nghi phạm Ngọc Trinh nói gì về thái độ của đồng nghiệp khi thấy mình?
Ngọc Trinh nói gì về thái độ của đồng nghiệp khi thấy mình? NÓNG: Nghi vấn Lưu Thi Thi - Ngô Kỳ Long ly hôn?
NÓNG: Nghi vấn Lưu Thi Thi - Ngô Kỳ Long ly hôn? "Vũ trụ mỹ nhân" hot tối nay: Thùy Tiên lạ lẫm chưa từng thấy, Thanh Thủy - Ý Nhi đọ visual căng nhưng spotlight thuộc về Midu!
"Vũ trụ mỹ nhân" hot tối nay: Thùy Tiên lạ lẫm chưa từng thấy, Thanh Thủy - Ý Nhi đọ visual căng nhưng spotlight thuộc về Midu!
 Cặp sao Việt lệch 10 tuổi vẫn đẹp đôi xuất sắc, nhà gái khoe mặt mộc xinh hút hồn khiến netizen nô nức "xin vía"
Cặp sao Việt lệch 10 tuổi vẫn đẹp đôi xuất sắc, nhà gái khoe mặt mộc xinh hút hồn khiến netizen nô nức "xin vía"
 Diễn viên Hoàng Yến tiết lộ chồng thứ 5, là sinh viên theo đuổi từ 20 năm trước
Diễn viên Hoàng Yến tiết lộ chồng thứ 5, là sinh viên theo đuổi từ 20 năm trước Tranh cãi việc học sinh cởi áo khoác, ngồi ngoài trời lạnh 19 độ C
Tranh cãi việc học sinh cởi áo khoác, ngồi ngoài trời lạnh 19 độ C Vợ cũ 1 sao Vbiz nhận "bão" chỉ trích khi tiếp tục đăng ảnh Hoa hậu Khánh Vân kèm lời lẽ thô thiển
Vợ cũ 1 sao Vbiz nhận "bão" chỉ trích khi tiếp tục đăng ảnh Hoa hậu Khánh Vân kèm lời lẽ thô thiển 4 người sống "phông bạt" ồn ào nhất Việt Nam năm 2024, top 1 đang cố tẩy trắng
4 người sống "phông bạt" ồn ào nhất Việt Nam năm 2024, top 1 đang cố tẩy trắng Lộ thời điểm nghi Nhật Kim Anh được bạn trai mới cầu hôn
Lộ thời điểm nghi Nhật Kim Anh được bạn trai mới cầu hôn Làm rõ nguyên nhân nữ sinh lớp 12 bị bố đẻ và chú ruột bạo lực
Làm rõ nguyên nhân nữ sinh lớp 12 bị bố đẻ và chú ruột bạo lực Dịch lạ tại Công-gô phức tạp, Hà Nội tăng cường kiểm dịch sân bay
Dịch lạ tại Công-gô phức tạp, Hà Nội tăng cường kiểm dịch sân bay Drama căng đét: Dương Mịch - Lưu Thi Thi giành giật vị trí nảy lửa kế Lưu Diệc Phi, tạo nên 30 phút im lặng đáng sợ trên thảm đỏ?
Drama căng đét: Dương Mịch - Lưu Thi Thi giành giật vị trí nảy lửa kế Lưu Diệc Phi, tạo nên 30 phút im lặng đáng sợ trên thảm đỏ? Diễn biến mới nhất vụ ca sĩ Đàm Vĩnh Hưng kiện tỉ phú Mỹ
Diễn biến mới nhất vụ ca sĩ Đàm Vĩnh Hưng kiện tỉ phú Mỹ Bạn trai mới của Nhật Kim Anh là ai?
Bạn trai mới của Nhật Kim Anh là ai? Nhật Kim Anh lên tiếng trả lời "bố đứa bé là ai?" sau khi công bố mang bầu gần 9 tháng
Nhật Kim Anh lên tiếng trả lời "bố đứa bé là ai?" sau khi công bố mang bầu gần 9 tháng