Cơ quan y tế châu Âu không cấp phép sử dụng thuốc Lecanemab trong điều trị Alzheimer
Cơ quan Giám sát dược phẩm châu Âu (EMA) ngày 26/7 đã từ chối yêu cầu tiếp thị Leqembi – một loại thuốc mới được sử dụng trong điều trị bệnh Alzheimer, do lo ngại rằng những nguy cơ từ tác dụng phụ của thuốc này có thể còn lớn hơn lợi ích.
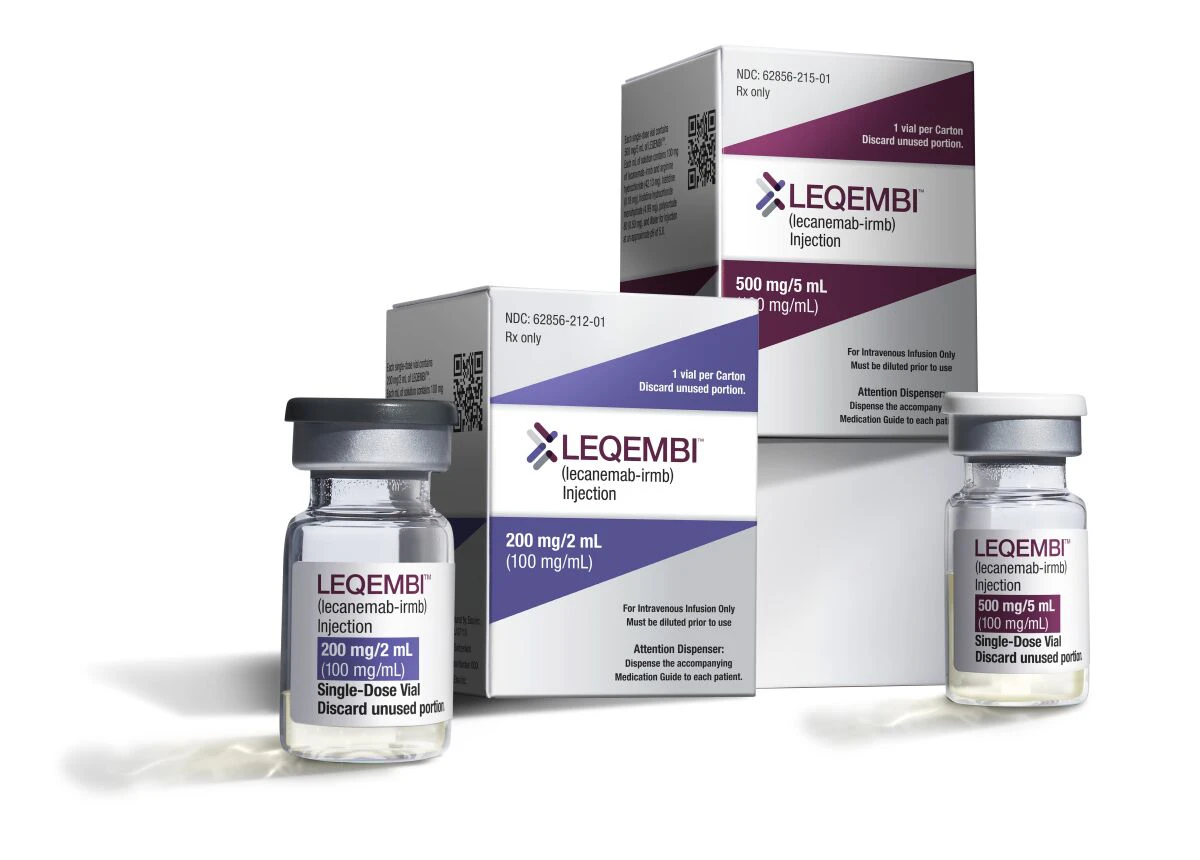
Thuốc Leqembi đặc trị cho người mắc bệnh Alzheimer. Ảnh: AP
Thông báo của EMA nêu rõ: “Ủy ban về dược phẩm sử dụng cho con người (CHMP thuộc EMA) khuyến cáo không cấp phép tiếp thị đối với Leqembi – một loại thuốc dùng để điều trị bệnh Alzheimer”.
Leqembi sử dụng một hoạt chất có tên là lecanemab để điều trị cho người trưởng thành gặp các vấn đề nhẹ về trí nhớ và nhận thức trong giai đoạn đầu của chứng mất trí nhớ thông thường. Tuy nhiên, CHMP cho biết “những hiệu quả có thể quan sát được của Leqembi trong việc trì hoãn suy giảm nhận thức là không cân bằng so với nguy cơ xảy ra các tác dụng phụ nghiêm trọng liên quan đến thuốc. Mối quan ngại lớn nhất về mức độ an toàn của Leqembi là tình trạng thường xuyên xảy ra các bất thường về hình ảnh liên quan đến amyloid (ARIA) – một tác dụng phụ có thể quan sát trong các hình ảnh về não, liên quan đến tình trạng sưng và nguy cơ xuất huyết não”.
Leqembi là một kháng thể đơn dòng, một loại protein có thể kết hợp với một chất có trong não và theo đó giúp làm chậm sự tiến triển của bệnh Alzheimer.
Leqembi, cùng một loại thuốc điều trị bệnh Alzheimer tên là Aduhelm, đã được Cơ quan Quản lý Thực phẩm và Dược phẩm Mỹ (FDA) phê duyệt sử dụng đầu năm ngoái. FDA thông qua 2 loại thuốc này trong một quy trình thúc đẩy đưa vào sử dụng những loại thuốc điều trị các tình trạng nghiêm trọng khi nguồn cung y tế chưa thể đáp ứng nhu cầu điều trị.
Theo số liệu của trang web Alzheimer Europe, Liên minh châu Âu (EU) hiện có khoảng 8 triệu người mắc chứng mất trí nhớ, trong đó bệnh Alzheimer chiếm hơn 50% trong số những trường hợp này.
Nhật Bản cấp phép sử dụng thuốc Lecanemab chữa Alzheimer
Ngày 25/9, Bộ Y tế Nhật Bản cấp phép sản xuất và bán thuốc điều trị bệnh Alzheimer do công ty dược phẩm nội địa Eisai Co. và công ty Biogen Inc. của Mỹ phối hợp phát triển.
Thuốc Lecanemab, nhãn hiệu Leqembi, là thuốc đầu tiên được cấp phép ở Nhật Bản vừa để điều trị các nguyên nhân tiềm ẩn gây bệnh Alzheimer vừa có tác dụng làm chậm quá trình phát triển các triệu chứng của bệnh. Thuốc dùng điều trị bệnh trong giai đoạn đầu và suy giảm nhận thức nhẹ, dự kiến sẽ được đưa vào sử dụng sớm nhất là cuối năm nay.
Quyết định trên được đưa ra sau khi các nhà quản lý Mỹ chính thức cấp phép sử dụng Lecanemab hồi tháng 7 vừa qua, sau 6 tháng cấp phép sử dụng khẩn cấp trong một số điều kiện. Tại Nhật Bản, một ban chuyên gia của Bộ Y tế đã đồng ý cấp phép chính thức với thuốc này vào cuối tháng 8 vừa qua. Giá của thuốc ở Mỹ là 26.500 USD/năm. Giá thuốc tại Nhật Bản cũng được cho là sẽ ở mức cao.
Eisai cho biết các thử nghiệm lâm sàng cho thấy thuốc có tác dụng kiềm chế sự phát triển của các triệu chứng như ngày càng suy giảm trí nhớ và suy giảm nhận thức, hiệu quả hơn khoảng 27% so với nhóm dùng giả dược.
Dù vậy, một số bệnh nhân sau khi tiêm thuốc xuất hiện một số tác dụng phụ như phù não và chảy máu.
Australia thu hồi 55 sản phẩm thuốc ho  Theo phóng viên TTXVN tại Sydney, Cục Quản lý dược phẩm (TGA) của Australia đã hủy đăng ký và yêu cầu thu hồi 55 sản phẩm thuốc ho có chứa chất pholcodine do lo ngại nguy cơ gây dị ứng nghiêm trọng, đe dọa đến tính mạng của người sử dụng. Australia thu hồi 55 sản phẩm thuốc ho. Ảnh minh họa: theconversation.com...
Theo phóng viên TTXVN tại Sydney, Cục Quản lý dược phẩm (TGA) của Australia đã hủy đăng ký và yêu cầu thu hồi 55 sản phẩm thuốc ho có chứa chất pholcodine do lo ngại nguy cơ gây dị ứng nghiêm trọng, đe dọa đến tính mạng của người sử dụng. Australia thu hồi 55 sản phẩm thuốc ho. Ảnh minh họa: theconversation.com...
 Trung Quốc triển khai hơn 80 máy bay, tàu chiến sát Đài Loan?08:57
Trung Quốc triển khai hơn 80 máy bay, tàu chiến sát Đài Loan?08:57 Philippines nói khó tránh liên quan nếu Đài Loan bị tấn công08:25
Philippines nói khó tránh liên quan nếu Đài Loan bị tấn công08:25 "Con đường tử thần" tại Kursk khi Nga đánh bật Ukraine khỏi chiến tuyến08:18
"Con đường tử thần" tại Kursk khi Nga đánh bật Ukraine khỏi chiến tuyến08:18 Động đất Myanmar: Cứu sống một người sau gần 4 ngày, số người chết gần vượt 3.00001:58
Động đất Myanmar: Cứu sống một người sau gần 4 ngày, số người chết gần vượt 3.00001:58 Washington cấp tập chuyển vũ khí đến Trung Đông08:52
Washington cấp tập chuyển vũ khí đến Trung Đông08:52 Ông Trump chính thức ký lệnh đánh thuế lên toàn cầu06:21
Ông Trump chính thức ký lệnh đánh thuế lên toàn cầu06:21 Mỹ cảnh báo Nga, khẳng định cam kết với NATO09:42
Mỹ cảnh báo Nga, khẳng định cam kết với NATO09:42 Iran tuyên bố rắn sau khi ông Trump dọa ném bom08:09
Iran tuyên bố rắn sau khi ông Trump dọa ném bom08:09 Phe đối lập Myanmar ngừng bắn sau động đất, Thái Lan điều tra vụ cao ốc sập10:07
Phe đối lập Myanmar ngừng bắn sau động đất, Thái Lan điều tra vụ cao ốc sập10:07 Nhiều nước lên tiếng về giải pháp cho khủng hoảng Ukraine21:26
Nhiều nước lên tiếng về giải pháp cho khủng hoảng Ukraine21:26 23 bang kiện chính quyền Tổng thống Trump09:04
23 bang kiện chính quyền Tổng thống Trump09:04Tiêu điểm
Tin đang nóng
Tin mới nhất

Mỹ và Nga lên tiếng về kết quả đàm phán hạt nhân Washington-Tehran

Ngành đồ chơi Mỹ 'khóc ròng' vì thuế nhập khẩu 145%

Chuyên gia đánh giá về chiến lược linh hoạt của ASEAN với chính sách thuế quan của Mỹ

Iran thông báo về kết quả cuộc đàm phán mới nhất với Mỹ tại Oman

Bí ẩn về người phụ nữ mang thai và giáo phái Nga ở Argentina

Apple hưởng lợi lớn từ thông báo miễn thuế đối ứng mới của Tổng thống Trump

Khai mạc EXPO 2025: Chung tay kiến tạo tương lai bền vững

Bất ngờ vì láng giềng của Dải Ngân hà đang bị xé toạc

Trung Quốc sẽ dùng đất mặt trăng để in gạch xây căn cứ tại đây

Nga phát động cuộc tấn công mùa xuân mới khi Ukraine tái xâm nhập vùng Belgorod

Ngoại trưởng Nga, Thổ Nhĩ Kỳ thảo luận nỗ lực thúc đẩy ngừng bắn tại Ukraine

Chiến tranh thương mại Mỹ - Trung: Ngành dược phẩm đứng trước sóng gió hay cơ hội?
Có thể bạn quan tâm

Tạm giữ 3 đối tượng khai thác gỗ thông trong rừng phòng hộ
Pháp luật
06:40:17 13/04/2025
Để làm món trứng hấp ngon hơn nhà hàng ngoài tỷ lệ nước và trứng, còn một thao tác nhỏ nữa không thể bỏ qua
Ẩm thực
06:21:42 13/04/2025
Chị Đẹp Concert "hài nhạt" từ đầu đến cuối: Giao lưu tới đâu khán giả "cảm lạnh" tới đó, cuối cùng "phải cười" vì.... lỗi từ BTC
Sao việt
06:20:04 13/04/2025
Báo Hàn gay gắt: "Lời xin lỗi của Kim Soo Hyun nên nhờ ngôi sao này viết hộ"
Sao âu mỹ
06:05:31 13/04/2025
Bố chồng chia thừa kế nhưng lại ép tôi ký giấy khước từ tài sản, tôi đưa ra 2 thứ khiến nhà họ tái mặt, run rẩy
Góc tâm tình
05:27:25 13/04/2025
Từ đối đầu sang đối thoại với Mỹ: Vì sao Lãnh tụ Tối cao Iran đổi ý?

 Cựu Tổng thống Trump lên kế hoạch trở lại nơi mình từng bị ám sát hụt
Cựu Tổng thống Trump lên kế hoạch trở lại nơi mình từng bị ám sát hụt Liên quân Mỹ – Anh tiếp tục không kích các mục tiêu quân sự của Houthi
Liên quân Mỹ – Anh tiếp tục không kích các mục tiêu quân sự của Houthi
 Mỹ cấp phép lưu hành thuốc mới chữa bệnh Alzheimer
Mỹ cấp phép lưu hành thuốc mới chữa bệnh Alzheimer EU và Ukraine chia rẽ về cấm vận dược phẩm liên quan đến Nga
EU và Ukraine chia rẽ về cấm vận dược phẩm liên quan đến Nga Toàn cảnh vụ tai nạn trực thăng khiến cả gia đình giám đốc Siemens tử nạn
Toàn cảnh vụ tai nạn trực thăng khiến cả gia đình giám đốc Siemens tử nạn Chính quyền Tổng thống Trump liệt hàng nghìn người nhập cư là đã chết
Chính quyền Tổng thống Trump liệt hàng nghìn người nhập cư là đã chết Sập đường hầm tàu điện ngầm ở Hàn Quốc, hơn 2.300 người sơ tán khẩn
Sập đường hầm tàu điện ngầm ở Hàn Quốc, hơn 2.300 người sơ tán khẩn Ông Trump nói về việc Mỹ áp thuế 145% với Trung Quốc
Ông Trump nói về việc Mỹ áp thuế 145% với Trung Quốc Nhà Trắng: Mức thuế áp lên Trung Quốc hiện là 145%, không phải 125%
Nhà Trắng: Mức thuế áp lên Trung Quốc hiện là 145%, không phải 125% Tổng thống Donald Trump để ngỏ việc miễn trừ đối với một số quốc gia
Tổng thống Donald Trump để ngỏ việc miễn trừ đối với một số quốc gia Cơ trưởng tử vong vì ngừng tim ngay sau khi đáp xuống sân bay Ấn Độ
Cơ trưởng tử vong vì ngừng tim ngay sau khi đáp xuống sân bay Ấn Độ Trung Quốc công bố mức thuế cuối cùng lên hàng hoá Mỹ
Trung Quốc công bố mức thuế cuối cùng lên hàng hoá Mỹ Xem lại Tây Du Ký 50 lần tôi mới nhận ra sự thật không ngờ đằng sau: Tôn Ngộ Không bị oan suốt 39 năm
Xem lại Tây Du Ký 50 lần tôi mới nhận ra sự thật không ngờ đằng sau: Tôn Ngộ Không bị oan suốt 39 năm
 HOT: Hoa hậu H'Hen Niê lộ rõ mồn một dấu hiệu bầu bí giữa lúc đang diễn concert Chị đẹp!
HOT: Hoa hậu H'Hen Niê lộ rõ mồn một dấu hiệu bầu bí giữa lúc đang diễn concert Chị đẹp!
 Trúc Anh (Mắt Biếc) có tình mới sau 1 tháng lộ chuyện chia tay bạn trai đạo diễn?
Trúc Anh (Mắt Biếc) có tình mới sau 1 tháng lộ chuyện chia tay bạn trai đạo diễn? Em gái của nàng công chúa đẹp nhất Châu Âu chọn lối đi riêng, không theo con đường của chị gái
Em gái của nàng công chúa đẹp nhất Châu Âu chọn lối đi riêng, không theo con đường của chị gái Nam MC đình đám VTV bị mạo danh trục lợi: Về hưu ngày nào cũng làm 2 việc này
Nam MC đình đám VTV bị mạo danh trục lợi: Về hưu ngày nào cũng làm 2 việc này 573 nhãn hiệu sữa giả, 11 công ty và doanh thu gần 500 tỷ đồng
573 nhãn hiệu sữa giả, 11 công ty và doanh thu gần 500 tỷ đồng Trùm Điền Quân Color Man đi xin việc, nói về việc phá sản
Trùm Điền Quân Color Man đi xin việc, nói về việc phá sản Nam thanh niên lao xuống dòng nước sâu để cứu cô gái nhảy cầu
Nam thanh niên lao xuống dòng nước sâu để cứu cô gái nhảy cầu Hai nữ bệnh nhân trẻ đột quỵ, từng sử dụng thuốc tránh thai kéo dài
Hai nữ bệnh nhân trẻ đột quỵ, từng sử dụng thuốc tránh thai kéo dài
 Kinh hoàng clip giáo viên xách ngược chân trẻ 20 tháng tuổi, đánh đập dã man
Kinh hoàng clip giáo viên xách ngược chân trẻ 20 tháng tuổi, đánh đập dã man Lâm Đồng thông tin vụ 7 chú tiểu bị xâm hại tình dục
Lâm Đồng thông tin vụ 7 chú tiểu bị xâm hại tình dục Vụ cháy nhà 4 người tử vong: Nỗi đau của thanh niên mất cùng lúc mẹ và em gái
Vụ cháy nhà 4 người tử vong: Nỗi đau của thanh niên mất cùng lúc mẹ và em gái Nữ MC 24 tuổi ra tay đầu độc đồng nghiệp, nạn nhân hiện đang tê liệt toàn thân
Nữ MC 24 tuổi ra tay đầu độc đồng nghiệp, nạn nhân hiện đang tê liệt toàn thân Vụ kẹo rau Kera: Hé lộ thêm sản phẩm công ty Quang Linh Vlogs thuê gia công
Vụ kẹo rau Kera: Hé lộ thêm sản phẩm công ty Quang Linh Vlogs thuê gia công Kinh hoàng cảnh bác sĩ lôi con rắn dài 1,2m ra khỏi miệng một phụ nữ ở Nga
Kinh hoàng cảnh bác sĩ lôi con rắn dài 1,2m ra khỏi miệng một phụ nữ ở Nga