Chuyên gia nêu điều kiện Việt Nam mua vaccine Covid-19
Việt Nam cần có thông tin về quy trình, căn cứ phê duyệt vaccine ngừa nCoV, để đi đến quyết định mua sản phẩm này, theo các chuyên gia.
Ngày 14/8, Bộ Y tế Việt Nam cho biết đã đề xuất đặt mua vaccine Covid-19 từ Nga, Anh và nỗ lực phối hợp với các nhà cung cấp vaccine trên thế giới để mua và sản xuất vaccine, ví dụ Mỹ.
Trước đó, Tổng thống Nga Putin tuyên bố nước này đã phát triển loại vaccine cung cấp khả năng “miễn dịch vững vàng” chống Covid-19. Đây là vaccine đầu tiên chống Covid-19 trên thế giới được cấp phép, sau chưa đầy hai tháng thử nghiệm trên người. Vaccine Sputnik V được đặt tên theo vệ tinh đầu tiên trên thế giới “Sputnik 1″ mà Liên Xô phóng lên vũ trụ năm 1957.
Gợi ý về các điều kiện cần thiết trước khi xúc tiến kế hoạch, Tiến sĩ Natalie Dean, Khoa Thống kê sinh học, Trường cao đẳng Y khoa, Đại học Florida, cho rằng Việt Nam nên xem xét các dữ liệu có sẵn về độ an toàn và hiệu quả của vaccine do nước bán sản xuất.
Thứ nhất, Việt Nam nên có thông tin nhà sản xuất như Nga đã tiến hành những gì trong quy trình nghiên cứu vaccine, để đảm bảo hiệu quả của sản phẩm khi “vượt quá” quỹ đạo chung. Dean cho hay quỹ đạo chung mà các nước đang phát triển vaccine chống Covid-19 là qua các giai đoạn khác nhau, một số vaccine đang được thử nghiệm lâm sàng trên quy mô lớn, người tham gia được chọn ngẫu nhiên. Thử nghiệm Giai đoạn ba là bước thử nghiệm quan trọng trên quy mô hàng nghìn người. Quá trình này đòi hỏi một tỷ lệ người tham gia nhất định tiếp xúc với virus để theo dõi hiệu quả của vaccine, thường được coi là tiền đề cần thiết giúp vaccine được cơ quan quản lý chấp thuận.
Theo Dean, các thử nghiệm lâm sàng trên quy mô với hàng nghìn người tham gia sẽ giúp phát hiện các tác dụng phụ hiếm gặp. Bên cạnh đó, dữ liệu về phản ứng miễn dịch, có được từ những thử nghiệm ban đầu, không có nghĩa là sản phẩm giúp bảo vệ con người khỏi bị nhiễm bệnh.
Thứ hai, Việt Nam nên có các dữ liệu khoa học cơ bản đã được nhà sản xuất sử dụng để phê duyệt vaccine mới. Bà cho rằng bất kể chính phủ nào cũng cần phải tự tin vào độ an toàn và hiệu quả của sản phẩm y tế.
“Có thể vaccine đáp ứng được các tiêu chuẩn an toàn và hiệu quả, nhưng chúng ta chưa biết chắc vì thiếu thông tin”, Dean nói đến vaccine của Nga.

Vaccine ngừa nCoV do Nga sản xuất, được công bố hôm 6/8. Ảnh: AP.
Giáo sư Danny Altmann, Khoa Miễn dịch và các bệnh viêm, Đại học Hoàng gia, Anh, cũng cho rằng Việt Nam nên có dữ liệu rõ ràng về hiệu quả của vaccine định mua. Bởi việc xác định tính lâu bền của vaccine trong bảo vệ người dân khỏi Covid-19 và giám sát nó là điều rất quan trọng. Nếu vaccine chỉ có hiệu quả trong vòng một năm hoặc ít hơn, một quốc gia sẽ cần phải tái tiêm chủng toàn dân.
Video đang HOT
Altmann cũng nhấn mạnh tầm quan trọng của thử nghiệm Giai đoạn ba, là bước cơ bản xác định sản phẩm được cấp phép và sản xuất. Quy trình tiến hành Giai đoạn ba có thể mất vài tháng. Ông cho hay trên toàn cầu hiện 160 loại vaccine chống Covid-19 đang được nghiên cứu, trong đó 6 vaccine đang ở Giai đoạn ba.
Giáo sư người Anh lưu ý các nước cần đưa ra quyết định chọn vaccine dựa trên các dữ liệu khoa học vững chắc, vì Covid-19 khiến con người khó có thể được tình trạng “miễn dịch tiệt trùng”, là khi vaccine ngăn được bệnh nhiễm vào phổi, từ đó giúp “quét sạch virus”. Tuy nhiên, những vaccine tạo ra phản ứng miễn dịch mạnh mẽ nhất sẽ giúp hạn chế sự vận chuyển của virus tồn đọng. Khi đó các quốc gia có thể không phải đối diện với các làn sóng mới của dịch trong tương lai.
Giáo sư John Moore, chuyên về miễn dịch và vi trùng học, Trường Y khoa Weill Cornell, Mỹ, khuyến cáo Việt Nam nên chờ đến khi có dữ liệu cho thấy vaccine Covid-19 an toàn và có tác dụng.
Hiện nhiều nhà khoa học của phương Tây bày tỏ lo ngại về vaccine do Nga sản xuất, nghi ngờ giới nghiên cứu nước này có thể đã “đốt cháy giai đoạn” dưới áp lực từ chính quyền. Tiến sĩ Dean đề xuất các nước nên sử dụng tiêu chuẩn chung về vaccine, trong đó có tiêu chuẩn của Tổ chức Y tế thế giới (WHO).
Theo tiến sĩ Dean, Việt Nam là một trong những nước cơ bản xử lý thành công Covid-19. Tại Mỹ, với diễn biến hiện nay, nước này cần có vaccine ngừa nCoV nhưng cũng chưa sử dụng, do chưa có sản phẩm đáng tin cậy.
“Tôi cho rằng Việt Nam nêu dựa vào các tiêu chuẩn chung về vaccine như của Mỹ, châu Âu và Tổ chức Y tế thế giới”, Dean nói.
Cuộc đua gian khó điều chế vaccine ngừa nCoV
Điều chế loại vaccine phù hợp ngừa nCoV chỉ là bước đầu, việc chứng minh được độ an toàn, hiệu quả và tăng cường quy mô sản xuất có thể mất tới nhiều năm hoặc hàng thập kỷ.
Ian Haydon, một nam thanh niên khỏe mạnh, 29 tuổi, đăng ký lấy máu tại một trung tâm y tế thành phố Seattle vào tuần trước.
"Ồ, máu của anh ấy quý như vàng đấy", y tá nói.
Haydon là một trong những tình nguyện viên đầu tiên tham gia thử nghiệm vaccine tại Mỹ. Với hy vọng góp phần vào nỗ lực chấm dứt đại dịch, anh đăng ký chương trình tiêm chủng dù biết về những rủi ro có thể gặp phải.
Các nhà khoa học tại Viện Y tế Quốc gia Mỹ (NIH) sẽ nghiên cứu mẫu máu của Haydon và những người khác, xem xét liệu vaccine có thể kích hoạt phản ứng miễn dịch, chống lại mầm bệnh cơ thể chưa từng gặp phải hay không. Đây sẽ là manh mối đầu tiên để đánh giá độ hiệu quả.
Ian Haydon, tình nguyện viên thử nghiệm vaccine ngừa nCoV tại Mỹ. Ảnh: Ian Haydon
Khi đại dịch có xu hướng suy yếu, vaccine dần trở thành "ánh sáng cuối đường hầm", diệt trừ hoàn toàn mầm bệnh và ngăn chặn các làn sóng tái bùng phát trong tương lai.
Theo tiến sĩ Anthony Fauci, Viện trưởng Viện Dị ứng và Bệnh truyền nhiễm Quốc gia, Mỹ đặt mục tiêu đưa vaccine vào sử dụng trong khoảng 12 đến 18 tháng tới. Nhà Trắng thậm chí khởi động một chiến dịch mang tên "Operation Warp Speed" nhằm đẩy nhanh quá trình điều chế, tiến hành thử nghiệm 14 "ứng cử viên" tiềm năng, tham vọng phân phối đại trà trong tháng 1 năm sau.
Với ít nhất 115 dự án phát triển vaccine tại nhiều công ty và phòng thí nghiệm, các nhà khoa học đang ráo riết chạy đua, bẻ cong rất nhiều quy trình vốn có. Ngay cả chuyên gia kỳ cựu nhất cũng không thể dự đoán điều gì sẽ xảy đến tiếp theo.
Nhiều năm liền, nghiên cứu khoa học được tiến hành theo từng bước tuần tự: thử nghiệm trên động vật, nghiên cứu độc lực học, nghiên cứu trong phòng thí nghệm, thử nghiệm trên người và cuối cùng là lên kế hoạch sản xuất. Giờ đây, các giai đoạn được thực hiện song song và đẩy nhanh hết mức có thể. Các nhà khoa học gọi đây là điều "chưa từng có tiền lệ".
Giới chức nước Mỹ mạnh mẽ cam kết họ sẽ không đặt tốc độ lên trên yếu tố an toàn, song nhiều chuyên gia y đức lo ngại về khái niệm "ngoại lệ nghiên cứu trong đại dịch", tức là tăng tốc phát triển và phân phối vaccine ra thị trường, bỏ qua một số tiêu chuẩn sẵn có. Nếu đi chệch hướng, thế giới có thể phải trả giá bằng làn sóng phản đối từ những người ủng hộ phong trào anti-vaccine, vốn là nỗi đau đầu từ trước khi Covid-19 bùng phát.
"Chúng ta mất đến 26 năm để phát triển vaccine ngừa rotavirus (gây bệnh tiêu chảy cấp ở trẻ em). Nếu muốn thành công trong vòng 12 đến 18 tháng, bạn sẽ phải bỏ qua nhiều giai đoạn. Như vậy có hơi mạo hiểm không? Có, nhưng việc nhiễm virus cũng vậy", Paul Offit, nhà nghiên cứu đã điều chế vaccine rotavirus, khẳng định.
Kể từ đầu tháng 1, khi Covid-19 thậm chí chưa được đặt tên, các nhà khoa học tại công ty công nghệ sinh học Inovio đã bắt đầu tìm cách phát triển vaccine. Giống với nhiều nhóm nghiên cứu trên toàn thế giới, họ sử dụng bộ mã gene của nCoV được các đồng nghiệp Trung Quốc chia sẻ trước đó.
Joseph Kim, giám đốc điều hành công ty, cho biết chỉ mất ba giờ để điều chế loại vaccine phù hợp.
Trong khi đó, các chuyên gia tại NIH cũng hợp tác với công ty công nghệ sinh học Moderna, cho ra đời loại vaccine khác. Quá trình sản xuất bắt đầu vào cuối tháng 1 tại một nhà máy ở thành phố Boston.
Ian Haydon được lấy máu để nghiên cứu liệu vaccine có kích hoạt phản ứng miễn dịch của cơ thể hay không. Ảnh: Ian Haydon
Tuy nhiên, việc điều chế một "ứng cử viên" tiềm năng mới chỉ là bước đầu của cuộc hành trình gian nan. Chứng minh sản phẩm an toàn, hiệu quả và tăng cường quy mô sản xuất có thể mất tới nhiều năm, thậm chí hàng thập kỷ.
Bên cạnh khoa học công nghệ, quá trình phát triển còn phụ thuộc vào diễn biến của dịch bệnh, sự linh hoạt của cơ quan quản lý và những điều giới chuyên gia tìm hiểu được trong khi nghiên cứu.
Thử nghiệm lâm sàng cũng gặp phải nhiều vấn đề phức tạp.
Thông thường, quá trình này diễn ra sau thử nghiệm trên động vật. Giai đoạn 1 được thực hiện trên số lượng nhỏ tình nguyện viên để xác định độ an toàn và liều dùng phù hợp. Các nhà chuyên gia sẽ theo dõi tác dụng phụ cũng như dấu hiệu sơ bộ cho thấy vaccine có hiệu quả.
Sau khi phân tích dữ liệu, hãng dược quyết định xem có tiến hành thử nghiệm giai đoạn 2 trên hàng trăm người hay không. Ở giai đoạn 3, các tình nguyện viên sẽ được phân nhóm, tiêm vaccine hoặc sử dụng giả dược để đối chứng. Toàn bộ công đoạn mất tới vài năm.
Một cách để đẩy nhanh quá trình sản xuất vaccine là chủ động nhiễm nCoV sau khi đã được tiêm chủng để đánh giá độ hiệu quả. Dù nhiều nhà khoa học ủng hộ cách làm này, số khác đặc biệt cân nhắc vấn đề đạo đức.
Song số lượng tình nguyện viên đăng ký các thử nghiệm đầy rủi ro như vậy vẫn tiếp tục tăng lên. Nhiều người sẵn sàng trở thành đối tượng nghiên cứu cho một loại vaccine có thể chưa được kiểm chứng trên động vật.
Ian Haydon sẽ tiêm mũi vaccine thử nghiệm thứ hai vào tuần tới, cho biết anh chưa từng làm điều này trước đây, nhưng rất sẵn lòng góp sức vào nỗ lực tìm ra vaccine an toàn và hiệu quả.
Công ty Mỹ bỏ thử nghiệm vaccine nCoV trên động vật 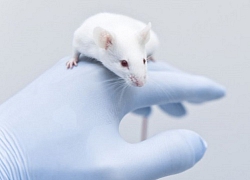 Với việc thử nghiệm lâm sàng ở người ngay sau khi sản xuất vaccine nCoV, công ty Moderna đã phá vỡ quy tắc thông thường trong phát triển dược phẩm. Moderna bỏ qua bước thử nghiệm vaccine trên mô hình động vật. Ảnh: Live Science. Thử nghiệm lâm sàng cho vaccine ngừa nCoV của công ty Moderna đã bắt đầu tuyển tình nguyện...
Với việc thử nghiệm lâm sàng ở người ngay sau khi sản xuất vaccine nCoV, công ty Moderna đã phá vỡ quy tắc thông thường trong phát triển dược phẩm. Moderna bỏ qua bước thử nghiệm vaccine trên mô hình động vật. Ảnh: Live Science. Thử nghiệm lâm sàng cho vaccine ngừa nCoV của công ty Moderna đã bắt đầu tuyển tình nguyện...
 Trung Quốc tung chatbot đấu ChatGPT, cổ phiếu Phố Wall chao đảo bốc hơi 1.000 tỉ14:53
Trung Quốc tung chatbot đấu ChatGPT, cổ phiếu Phố Wall chao đảo bốc hơi 1.000 tỉ14:53 Ông Trump dọa trừng phạt Nga nếu ông Putin từ chối đàm phán chấm dứt chiến sự Ukraine09:59
Ông Trump dọa trừng phạt Nga nếu ông Putin từ chối đàm phán chấm dứt chiến sự Ukraine09:59 Trung Quốc, Đức phản ứng sau khi ông Trump ký sắc lệnh rút khỏi WHO01:49
Trung Quốc, Đức phản ứng sau khi ông Trump ký sắc lệnh rút khỏi WHO01:49 Tàu vận tải Nga cập cảng Syria, chuẩn bị cho cuộc rút quân09:12
Tàu vận tải Nga cập cảng Syria, chuẩn bị cho cuộc rút quân09:12 Hé lộ kế hoạch mới của ông Trump về xung đột Nga-Ukraine08:31
Hé lộ kế hoạch mới của ông Trump về xung đột Nga-Ukraine08:31 Ông Trump nói muốn gặp ông Putin ngay lập tức08:46
Ông Trump nói muốn gặp ông Putin ngay lập tức08:46 Căn cứ hải quân ngầm ở độ sâu 500 m của Iran08:37
Căn cứ hải quân ngầm ở độ sâu 500 m của Iran08:37 "Hỏa thần nhiệt áp" Nga ra đòn, nhằm thẳng cứ điểm Ukraine ở Kursk08:59
"Hỏa thần nhiệt áp" Nga ra đòn, nhằm thẳng cứ điểm Ukraine ở Kursk08:59 Tổng thống Trump lên tiếng về 'thảm kịch' hàng không ở thủ đô Washington DC10:41
Tổng thống Trump lên tiếng về 'thảm kịch' hàng không ở thủ đô Washington DC10:41 Bức điện tín hé lộ nỗi lo của Đức về ông Trump08:02
Bức điện tín hé lộ nỗi lo của Đức về ông Trump08:02 Tỉ phú Musk gây tranh cãi với cử chỉ 'chào Hitler' trong lễ nhậm chức của Tổng thống Trump10:12
Tỉ phú Musk gây tranh cãi với cử chỉ 'chào Hitler' trong lễ nhậm chức của Tổng thống Trump10:12Tiêu điểm
Tin đang nóng
Tin mới nhất

Học giả Trung Quốc đề xuất nhiều giải pháp thúc đẩy hợp tác thực chất Việt - Trung

Hàn Quốc xét xử các lãnh đạo quân đội và cảnh sát liên quan đến lệnh thiết quân luật

Chiến sự tại Gaza và những giới hạn của hệ thống phòng thủ tên lửa

Thủ tướng Israel công du Mỹ: Thỏa thuận ngừng bắn tại Gaza đứng trước ngã rẽ?

Thủ tướng Israel Benjamin Netanyahu lên đường thăm Mỹ

Lý do nhiều người dân Anh trả tiền để sống trong các công trình bỏ hoang

Kỷ nguyên mới của chủ nghĩa bảo hộ của Mỹ

Tổng thống Nga bình luận về định hướng chính sách của tân chính quyền Mỹ

Cộng đồng doanh nghiệp Mexico bày tỏ quan ngại trước lệnh áp thuế của Mỹ

Ukraine lên tiếng về đề xuất giải quyết xung đột của Mỹ

Tổng thống Litva đề nghị NATO 'thể hiện sức mạnh' trước mối đe dọa từ phía Đông

Lý do bất ngờ khiến tên lửa 'không có đối thủ' của Nga vẫn chưa thể đưa vào hoạt động
Có thể bạn quan tâm

Súp sủi cảo - món ăn ấm nóng mùa giá lạnh
Ẩm thực
06:20:54 04/02/2025
Mở miệng hỏi xin chồng 50 triệu để khám bệnh cho mẹ, anh đưa 200 triệu nhưng kèm điều kiện khiến tôi muốn ly hôn
Góc tâm tình
05:59:15 04/02/2025
Khám phá sắc xuân trên cao nguyên Lâm Viên
Du lịch
05:35:59 04/02/2025
Hình ảnh mới của diva Hồng Nhung sau điều trị ung thư
Sao việt
23:57:50 03/02/2025
Bộ Tứ Báo Thủ bị chê dở nhất: Trấn Thành đăng đàn đáp trả gây xôn xao
Hậu trường phim
23:55:19 03/02/2025
Nhìn lại loạt khoảnh khắc visual xuất sắc của Từ Hy Viên trước khi mãi mãi ra đi ở tuổi 48 vì bệnh cúm
Sao châu á
23:32:33 03/02/2025
Phim Việt hay đến mức được tăng 166% suất chiếu, cặp chính gây bão mạng vì ngọt từ phim đến đời
Phim việt
23:24:35 03/02/2025
Tổng kết Grammy 2025: Taylor Swift trắng tay, Beyoncé hoàn thành giấc mơ kèn vàng, một siêu sao "thắng đậm"
Nhạc quốc tế
23:18:28 03/02/2025
Bảo Anh gọi 1 Anh Trai là "thợ đụng", từng cùng tham gia band nhạc giao lưu Việt - Ấn rồi tan rã ngay lập tức
Nhạc việt
23:11:33 03/02/2025
Cách chăm sóc, bảo vệ da trong mùa Xuân
Làm đẹp
22:17:45 03/02/2025
 Tân sinh viên Mỹ lúng túng học online thời Covid-19
Tân sinh viên Mỹ lúng túng học online thời Covid-19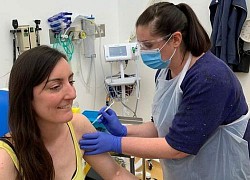 100.000 người Anh đăng ký tiêm thử vaccine Covid-19
100.000 người Anh đăng ký tiêm thử vaccine Covid-19

 Jack Ma chi hơn 14 triệu USD chống virus Corona Vũ Hán
Jack Ma chi hơn 14 triệu USD chống virus Corona Vũ Hán Ban hiệu suất chính phủ "khoe" giúp Mỹ tiết kiệm được 1 tỷ USD mỗi ngày
Ban hiệu suất chính phủ "khoe" giúp Mỹ tiết kiệm được 1 tỷ USD mỗi ngày Trung Quốc tuyên bố kiện Mỹ lên WTO sau lệnh áp thuế
Trung Quốc tuyên bố kiện Mỹ lên WTO sau lệnh áp thuế Ukraine báo động đỏ trên cả nước: Hàng loạt máy bay Tu-95 Nga cất cánh
Ukraine báo động đỏ trên cả nước: Hàng loạt máy bay Tu-95 Nga cất cánh Nga cảnh báo Tổng thống Trump khơi lại "Chiến tranh giữa các vì sao"
Nga cảnh báo Tổng thống Trump khơi lại "Chiến tranh giữa các vì sao" Tổng thống Ukraine sẵn sàng bắt đầu đàm phán chấm dứt xung đột
Tổng thống Ukraine sẵn sàng bắt đầu đàm phán chấm dứt xung đột
 Ấn Độ công bố ngân sách quốc phòng kỷ lục
Ấn Độ công bố ngân sách quốc phòng kỷ lục Hé lộ đề xuất của Mỹ với Ukraine sau lệnh ngừng bắn
Hé lộ đề xuất của Mỹ với Ukraine sau lệnh ngừng bắn Từ Hy Viên vừa qua đời: Chồng mới - chồng cũ lao vào cuộc chiến tranh chấp tài sản?
Từ Hy Viên vừa qua đời: Chồng mới - chồng cũ lao vào cuộc chiến tranh chấp tài sản? Nóng: Không tìm thấy chồng Từ Hy Viên
Nóng: Không tìm thấy chồng Từ Hy Viên Chồng cũ Từ Hy Viên về đến sân bay: Mắt sưng húp, còn làm 1 hành động gây bất ngờ
Chồng cũ Từ Hy Viên về đến sân bay: Mắt sưng húp, còn làm 1 hành động gây bất ngờ Rò rỉ thỏa thuận tiền hôn nhân "3 không" của Từ Hy Viên, chồng ca sĩ Hàn sẽ mất quyền thừa kế?
Rò rỉ thỏa thuận tiền hôn nhân "3 không" của Từ Hy Viên, chồng ca sĩ Hàn sẽ mất quyền thừa kế? Mẹ khóc nghẹn bên thi thể Từ Hy Viên, cầu xin truyền thông và khán giả cùng làm 1 điều vì tâm nguyện của con
Mẹ khóc nghẹn bên thi thể Từ Hy Viên, cầu xin truyền thông và khán giả cùng làm 1 điều vì tâm nguyện của con Văn Hậu khoe ảnh chụp cùng nhà vợ toàn cực phẩm, mẹ Doãn Hải My gây chú ý với nhan sắc trẻ đẹp tuổi U50
Văn Hậu khoe ảnh chụp cùng nhà vợ toàn cực phẩm, mẹ Doãn Hải My gây chú ý với nhan sắc trẻ đẹp tuổi U50 'Sự ra đi của Từ Hy Viên là nỗi đau khắc sâu trong lòng chị'
'Sự ra đi của Từ Hy Viên là nỗi đau khắc sâu trong lòng chị' Nhan sắc Doãn Hải My sau 10 ngày thẩm mỹ, khoe ảnh ở quê Đoàn Văn Hậu mà dân tình tấm tắc khen: Quá đẹp!
Nhan sắc Doãn Hải My sau 10 ngày thẩm mỹ, khoe ảnh ở quê Đoàn Văn Hậu mà dân tình tấm tắc khen: Quá đẹp! Thi hài Từ Hy Viên được hỏa táng ở Nhật, di ngôn hé lộ tâm nguyện sau lần thập tử nhất sinh 9 năm trước
Thi hài Từ Hy Viên được hỏa táng ở Nhật, di ngôn hé lộ tâm nguyện sau lần thập tử nhất sinh 9 năm trước SỐC: Từ Hy Viên 3 lần cấp cứu vì nguy kịch ở Nhật, tử vong chỉ sau 5 ngày phát bệnh
SỐC: Từ Hy Viên 3 lần cấp cứu vì nguy kịch ở Nhật, tử vong chỉ sau 5 ngày phát bệnh Chấn động: Từ Hy Viên qua đời
Chấn động: Từ Hy Viên qua đời Đạo diễn Nguyễn Ngọc Quyền đột ngột qua đời ở tuổi 36, đồng nghiệp tiết lộ nguyên nhân
Đạo diễn Nguyễn Ngọc Quyền đột ngột qua đời ở tuổi 36, đồng nghiệp tiết lộ nguyên nhân Thêm 1 sao nam lên tiếng về drama chê phim Trấn Thành, đứng ra giảng hoà nhưng bị Lê Giang đáp trả đến câm nín
Thêm 1 sao nam lên tiếng về drama chê phim Trấn Thành, đứng ra giảng hoà nhưng bị Lê Giang đáp trả đến câm nín
 Chấn động vụ đánh ghen ngay tại rạp Việt dịp Tết, tình tiết y hệt phim Trấn Thành khiến 3,6 triệu người quá sốc
Chấn động vụ đánh ghen ngay tại rạp Việt dịp Tết, tình tiết y hệt phim Trấn Thành khiến 3,6 triệu người quá sốc Dòng tâm sự cuối cùng trên mạng xã hội của Từ Hy Viên trước khi qua đời
Dòng tâm sự cuối cùng trên mạng xã hội của Từ Hy Viên trước khi qua đời Vụ tai nạn 7 người tử vong ở Nam Định: Nữ tài xế đột ngột đánh lái sang phải
Vụ tai nạn 7 người tử vong ở Nam Định: Nữ tài xế đột ngột đánh lái sang phải