Bộ Y tế lần đầu tiên nói về vụ ‘test kit Việt Á’: Bộ thực hiện đúng quy định, địa phương tự mua sắm
Ba ngày kể từ khi tổng giám đốc Công ty Việt Á bị bắt vì nâng giá xét nghiệm, Bộ Y tế gửi đến truyền thông một thông báo dài về vụ việc này.
Bộ Y tế nói gì?
KIT xét nghiệm COVID-19 của Việt Nam được WHO chấp thuận – Ảnh: Bộ KH&CN
Tuổi Trẻ Online tóm tắt nội dung:
Thực hiện đúng quy định cấp phép lưu hành sinh phẩm của Việt Á
Thực hiện quyết định 489 ngày 2-3-2020 của bộ trưởng Bộ Khoa học và công nghệ, ngày 3-3-2020, Hội đồng đánh giá, nghiệm thu kết quả giai đoạn 1 đề tài cấp quốc gia “Nghiên cứu chế tạo bộ sinh phẩm RT-PCR và realtime RT-PCR phát hiện chủng virus corona mới 2019 (2019-nCoV)” đã họp, đề nghị Bộ Y tế cấp phép sử dụng cho 2 bộ sinh phẩm realtime PCR chẩn đoán SARS-CoV-2 (LightPoweriVA SARS-CoV-2 1st RT-PCR Kit, LightPoweriVA SARS-CoV-2 1st RT-rPCR Kit).
Đây là kết quả của nhiệm vụ khoa học và công nghệ cấp quốc gia do Bộ Khoa học và công nghệ phê duyệt, được thực hiện giữa Học viện Quân y và Công ty cổ phần công nghệ Việt Á.
Căn cứ vào ý kiến của hội đồng nói trên, kết quả đánh giá đáp ứng về độ nhạy và độ đặc hiệu của Viện Vệ sinh dịch tễ trung ương, kết quả xác nhận cơ sở sản xuất của công ty đã đạt tiêu chuẩn ISO 13485:2016 của Tổ chức Bureau Veritas (tổ chức đã được Bộ Khoa học và công nghệ công nhận), theo các quy định tại nghị định 36/2016, nghị định 169/2018, Bộ Y tế đã cấp phép sử dụng tạm thời cho 2 bộ sinh phẩm nói trên trong thời hạn 6 tháng vào ngày 4-3-2020 để sử dụng trong xét nghiệm sàng lọc.
Bộ Y tế cho rằng việc cấp phép đã đáp ứng nhu cầu xét nghiệm “tại thời điểm khó khăn khi tiếp cận với nguồn cung ứng sinh phẩm trên thế giới”.
Đến ngày 4-12-2020, Bộ Y tế có quyết định số 5071 cấp phép lưu hành 5 năm đối với bộ sinh phẩm xét nghiệm SARS-CoV-2 chủng loại LightPoweriVA SARS-CoV-2 1st RT-rPCR Kit của Công ty cổ phần công nghệ Việt Á.
Cũng tại quyết định trên, Bộ Y tế cấp phép lưu hành cho sinh phẩm xét nghiệm SARS-CoV-2 chủng loại One-Step RT- PCR COVID-19 Kit Thai Duong Multiplex-3 target genes Version 1.0 của Công ty cổ phần Sao Thái Dương.
Tính đến ngày 20-12-2021, Bộ Y tế đã cấp phép 146 sinh phẩm xét nghiệm SARS-CoV-2, trong đó có 46 sinh phẩm xét nghiệm vật liệu di truyền (PCR, LAMP) tương tự như sản phẩm của Công ty cổ phần công nghệ Việt Á và Công ty cổ phần Sao Thái Dương với 7 sinh phẩm sản xuất trong nước và 39 sinh phẩm nhập khẩu, Bộ Y tế xác định việc cấp phép cho nhiều sản phẩm là để tăng cường nội địa hóa, chủ động nguồn cung và tạo sự cạnh tranh về giá sinh phẩm xét nghiệm.
Tất cả các sản phẩm cấp phép đều được đánh giá đạt yêu cầu, đáp ứng tiêu chuẩn, chất lượng của Việt Nam và đảm bảo đúng theo các quy định hiện hành. Các sản phẩm sau khi được cấp phép đều được theo dõi chất lượng và tính ổn định.
Về danh mục các sinh phẩm do Tổ chức Y tế thế giới (WHO) công bố và đưa vào danh sách sử dụng khẩn cấp (EUL), Bộ Y tế cho rằng các công ty mong muốn sản phẩm của mình được đưa vào danh sách của WHO thì nộp hồ sơ đề nghị WHO xem xét.
Video đang HOT
Mỗi quốc gia, tổ chức đều xây dựng tiêu chí và yêu cầu về hồ sơ, sản phẩm khác nhau về việc chấp thuận lưu hành sinh phẩm. Các công ty có nhu cầu lưu hành, sử dụng tại quốc gia và tổ chức nào sẽ nộp hồ sơ theo quy định của từng tổ chức, quốc gia, việc cấp phép của Bộ Y tế đối với sản phẩm của Việt Á và các nhà sản xuất khác không phụ thuộc vào danh sách WHO công bố.
Bộ Y tế thông tin
“Giá sinh phẩm xét nghiệm phải thông qua đấu thầu công khai”
Theo Bộ Y tế, quy định của Luật giá cho biết trang thiết bị y tế và sinh phẩm xét nghiệm không thuộc trong danh mục mặt hàng phải quản lý giá. Giá trang thiết bị y tế và sinh phẩm xét nghiệm được xác định thông qua đấu thầu và giá các sản phẩm khác nhau theo từng thời điểm và số lượng mua sắm, khả năng cung ứng.
“Cùng thời điểm Công ty Việt Á niêm yết giá trên Cổng công khai giá là 470.000 đồng/sản phẩm, thì Công ty cổ phần Sao Thái Dương niêm yết giá loại xét nghiệm PCR là 300.000 đồng/sản phẩm và xét nghiệm LAMP có giá 385.000 đồng/sản phẩm, Công ty Ampharco U.S.A có giá 179.800 đồng/sản phẩm…
Có 15 sản phẩm PCR nhập khẩu đã được cấp phép đăng ký và niêm yết giá từ 280.000 đồng đến 600.000 đồng/sản phẩm.
Thông tin này đã được công khai trên Cổng công khai giá để các địa phương, cơ sở y tế nắm bắt, tham khảo khi xây dựng kế hoạch và thực hiện mua sắm, đấu thầu, sử dụng sản phẩm phục vụ nhu cầu phòng, chống dịch, không phải là giá bắt buộc áp dụng.
Bộ Y tế cho rằng các địa phương, đơn vị thực hiện mua sắm, đấu thầu theo đúng quy định và chịu trách nhiệm về kết quả thực hiện. “Bộ Y tế đã có các văn bản đề nghị các đơn vị sản xuất và kinh doanh xem xét giảm giá bán sinh phẩm xét nghiệm để hỗ trợ cho các đơn vị chống dịch. Đến nay, cơ bản hầu hết các sản phẩm đã được giảm giá” – Bộ Y tế nêu ý kiến.
Bộ Y tế cũng cho biết đã trình Chính phủ nghị định 98/2021 (có hiệu lực thi hành từ ngày 1-1-2022), trong đó quy định giá sinh phẩm xét nghiệm thuộc mặt hàng quản lý giá. Chính phủ cũng đã trình Ủy ban Thường vụ Quốc hội đưa trang thiết bị, sinh phẩm y tế phòng chống dịch COVID-19 vào mặt hàng bình ổn giá.
“Các địa phương, đơn vị chủ động mua sắm, đấu thầu sinh phẩm theo quy định. Công tác phòng, chống dịch ở Việt Nam được thực hiện theo phương châm “4 tại chỗ”" – Bộ Y tế viết trong thông cáo. Việc thực hiện mua sắm vật tư, trang thiết bị, sinh phẩm y tế cứ theo các quy định của pháp luật về đấu thầu.
Tin sáng 18-12: Bộ Y tế rút ngắn lịch tiêm mũi vắc xin bổ sung, tiêm sau mũi hai 3 tháng
Ngày 17-12, Bộ Y tế đã có văn bản gửi sở y tế các tỉnh, thành phố; Viện Vệ sinh dịch tễ, Viện Pasteur; Cục Y tế, Bộ Công an, Cục Quân y, Tổng cục Hậu cần, Bộ Quốc phòng về việc tiêm vắc xin COVID-19 liều bảo vệ và nhắc lại.
Nhân viên y tế chăm sóc cho các trường hợp F0 đang điều trị tại Bệnh viện hồi sức COVID-19 (TP Thủ Đức) - Ảnh: DUYÊN PHAN
Liều bổ sung dành cho đối tượng là người có tình trạng suy giảm miễn dịch vừa và nặng như người cấy ghép tạng, ung thư, nhiễm HIV, đang điều trị thuốc ức chế miễn dịch hoặc đã điều trị trong vòng 6 tháng...
Người đã tiêm đủ liều cơ bản bằng vắc xin của Hãng Sinopharm hoặc vắc xin Sputnik V thì tiêm liều bổ sung bằng vắc xin cùng loại với liều cơ bản hoặc vắc xin mRNA. Khoảng cách tiêm 1 mũi bổ sung sau mũi cuối cùng của liều cơ bản từ 28 ngày đến 3 tháng.
Đối với những người có chỉ định tiêm liều bổ sung, sau khi đã tiêm liều bổ sung thì được coi là hoàn thành liều cơ bản.
Đồ họa: NGỌC THÀNH
Tiêm liều nhắc lại vắc xin COVID-19 cho người từ 18 tuổi trở lên đã tiêm đủ liều cơ bản hoặc liều bổ sung, bảo đảm bao phủ cho toàn bộ người có bệnh nền, người cần được chăm sóc dài hạn tại các cơ sở y tế, người từ 50 tuổi trở lên, người trực tiếp xét nghiệm, chăm sóc, điều trị bệnh nhân COVID-19, nhân viên y tế.
Về loại vắc xin, nếu các mũi tiêm cơ bản hoặc bổ sung cùng loại vắc xin thì tiêm mũi nhắc lại cùng loại đó hoặc vắc xin mRNA. Nếu trước đó đã tiêm các loại vắc xin khác nhau thì tiêm mũi nhắc lại bằng vắc xin mRNA.
Nếu tiêm liều cơ bản hoặc bổ sung là vắc xin của Hãng Sinopharm thì có thể tiêm mũi nhắc lại cùng loại đó hoặc vắc xin mRNA hoặc vắc xin véctơ virus (vắc xin AstraZeneca).
Khoảng cách tiêm 1 mũi nhắc lại ít nhất 3 tháng sau mũi cuối cùng của liều cơ bản. So với hướng dẫn do Bộ Y tế ban hành đầu tháng 12, thời gian tiêm mũi bổ sung đã rút ngắn xuống còn 3 tháng, thay vì 6 tháng như trước đây.
Bộ Y tế nêu rõ vắc xin sử dụng để tiêm bổ sung và liều nhắc lại là vắc xin đã được Bộ Y tế phê duyệt. Liều lượng vắc xin để tiêm bổ sung và nhắc lại tuân thủ theo hướng dẫn sử dụng của nhà sản xuất đã được Bộ Y tế cho phép.
Đối với những người đã mắc COVID-19 thì tiêm ngay sau khi hồi phục và hoàn thành việc cách ly y tế theo quy định.
Tiêm vắc xin mũi 2 Pfizer cho học sinh khối lớp 10 Trường THPT Trưng Vương, quận 1, TP.HCM sáng 23-11 - Ảnh: QUANG ĐỊNH
Việt Nam đã nhận 172 triệu liều vắc xin, đã tiêm gần 137 triệu mũi
Bộ Y tế cho biết vừa tiếp nhận thêm lô vắc xin mới, nâng tổng số vắc xin đã tiếp nhận cho đến nay là 172 triệu liều. Đến ngày 18-12 đã tiêm chủng gần 137 triệu mũi.
Tính đến ngày 14-12, tỉ lệ người từ 18 tuổi trở lên tiêm ít nhất 1 mũi vắc xin là 97%, tiêm đủ 2 mũi đạt xấp xỉ 81%, tỉ lệ bao phủ ít nhất 1 liều vắc xin/dân số đạt trên 60%, xếp thứ 4 tại khu vực ASEAN (sau Singapore, Campuchia và Brunei).
Lực lượng chức năng P.Phố Huế phong tỏa y tế nhiều khu vực thuộc tập thể Nguyễn Công Trứ (Hà Nội) khi phát hiện hàng loạt ca nhiễm COVID-19 - Ảnh: NAM TRẦN
Số ca COVID-19 nặng và tử vong vẫn tăng
Số liệu của Tiểu ban điều trị, Bộ Y tế cho biết số mắc mới trong ngày 17-12 là 15.206 ca, nâng tổng số ca mắc ghi nhận tại Việt Nam từ đầu vụ dịch lên xấp xỉ 1,5 triệu ca. Trong số này có gần 1,1 triệu ca đã khỏi bệnh (73,6%), số tử vong là 29.125 ca (2%).
Hiện còn 283.522 bệnh nhân theo dõi, điều trị, trong đó có 243.472 ca theo dõi, điều trị tại nhà; 9.732 ca theo dõi, điều trị tại khu cách ly và 110.257 ca điều trị tại 916 bệnh viện. Trong số đang điều trị tại bệnh viện có 7.841 ca nặng, bao gồm 1.109 ca phải thở máy.
So với trung bình 7 ngày trước, số ca bệnh mới giảm 10,4%, số ca tử vong tăng 2,9%, số ca nặng tăng 6,1%.
So với tuần trước, số mắc mới tăng 5,1%, số tử vong tăng 9%, số ca nặng, nguy kịch tăng 2,2%, trong đó số thở máy xâm lấn tăng 23,1%. So sánh với tháng trước, số ca nặng, nguy kịch tăng 91,5%, số ca tử vong tăng 167%.
Hiện các địa phương đang có số bệnh nhân điều trị cao gồm TP.HCM (70.361), Bình Dương 60.942, Tây Ninh 16.953, Cần Thơ 16.088, Bà Rịa - Vũng Tàu 11.873, Cà Mau 11.335, Khánh Hòa 9.731, Trà Vinh 9.396. Hiện TP.HCM, Đồng Nai, Bình Dương, Long An, Cần Thơ, An Giang, Tiền Giang, Bến Tre, Tây Ninh, Vĩnh Long là có nhiều ca diễn biến nặng nhất.
Nhân viên y tế phường 7, quận Phú Nhuận thăm khám và phát thuốc cho các trường hợp F0 cách ly tại nhà - Ảnh: DUYÊN PHAN
- Ngày 17-12, Hà Nội cho biết trong 24 giờ qua ghi nhận 1.440 ca COVID-19 mới, trong đó có 557 ca cộng đồng, chiếm gần 40%, 634 ca trong khu cách ly và 249 ca trong khu phong tỏa. Đây là ngày thứ 3 liên tiếp Hà Nội phát hiện trên 1.300 ca COVID-19/ngày.
Cộng dồn số ca tại Hà Nội trong đợt dịch 4 là 24.237 ca, trong đó số ca cộng đồng 9.354 ca, số ca đã được cách ly 14.883 ca. Quận Đống Đa - quận vùng cam nguy cơ cao duy nhất ở Hà Nội - đã đưa vào vận hành cơ sở thu dung, điều trị F0 thể nhẹ với quy mô 600 giường tại khu ký túc xá Trường đại học Thủy lợi. Số bệnh nhân đang được tiếp nhận điều trị là 98 người.
- Chiều tối 17-12, Hà Nam công bố thêm 25 ca dương tính. Hà Nam yêu cầu chủ các nhà máy, xí nghiệp, công ty chủ động xét nghiệm tầm soát đối với những trường hợp có nguy cơ cao. Sau gần 3 tháng bùng phát đợt dịch mới, toàn tỉnh ghi nhận 1.567 ca COVID-19.
- Quảng Bình từ 6h ngày 16-12 đến 6h ngày 17-12 ghi nhận thêm 50 ca COVID-19 mới, trong đó có 44 ca cộng đồng. Có 31 ca liên quan đến chùm ca bệnh chợ Tréo-Kiến Giang (Lệ Thủy).
- Vĩnh Long, số ca COVID-19 mới chưa có dấu hiệu giảm, trong đó phát hiện qua khám sàng lọc cộng đồng và tại cơ sở y tế chiếm hơn 70% số ca mắc mới. Trong 14 ngày gần đây, tỉnh ghi nhận 7.898 ca COVID-19, trung bình 566 ca/ngày. So với 14 ngày trước đó, tăng 1.553 ca, trong đó có trên 5.500 ca mắc phát hiện qua khám sàng lọc cộng đồng.
- Bến Tre từ 6h đến 11h ngày 17-12 có 726 ca COVID-19, tính đến 11h có 1.128 ca, nâng tổng số ca mắc toàn tỉnh là 19.738 ca. Trong đó, có 8.699 ca được điều trị khỏi, 101 ca tử vong.
- Cà Mau cho biết trong 24 giờ qua, tỉnh này ghi nhận 1.339 ca COVID-19 mới, trong đó có 1.029 ca cộng đồng, cao nhất từ trước đến nay, nâng số ca mắc của tỉnh lên 20.640 ca. Cà Mau đã quyết định điều chỉnh cấp độ dịch: có 74 đơn vị cấp xã thuộc cấp độ 3 (vùng cam) về dịch COVID-19, tăng 12 đơn vị cấp xã.
Người dân không đồng ý tiêm, Quảng Trị xin trả lại lô vắc xin trong diện gia hạn 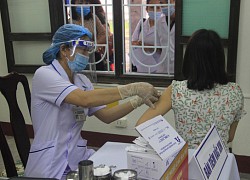 Sau khi thực hiện khảo sát, có đến 94% số người trong nhóm tuổi 12-17 không đồng ý tiêm lô vắc xin được gia hạn, Sở Y tế Quảng Trị đã có văn bản xin trả lại lô vắc xin nói trên cho Bộ Y tế. Hầu hết người trong lứa tuổi 12-17 đều từ chối tiêm nên Quảng Trị đã trả lại...
Sau khi thực hiện khảo sát, có đến 94% số người trong nhóm tuổi 12-17 không đồng ý tiêm lô vắc xin được gia hạn, Sở Y tế Quảng Trị đã có văn bản xin trả lại lô vắc xin nói trên cho Bộ Y tế. Hầu hết người trong lứa tuổi 12-17 đều từ chối tiêm nên Quảng Trị đã trả lại...
 Sự thật ngỡ ngàng người đàn ông chui qua cửa kính taxi kêu cứu trên cao tốc00:46
Sự thật ngỡ ngàng người đàn ông chui qua cửa kính taxi kêu cứu trên cao tốc00:46 Quán bún Hà Nội xin lỗi vụ bán 1,2 triệu đồng 3 bát bún riêu ngày Tết, nói chỉ là 'hiểu lầm'09:39
Quán bún Hà Nội xin lỗi vụ bán 1,2 triệu đồng 3 bát bún riêu ngày Tết, nói chỉ là 'hiểu lầm'09:39 Vụ xe ôtô lao xuống mương 7 người tử vong: Công an công bố nguyên nhân ban đầu14:39
Vụ xe ôtô lao xuống mương 7 người tử vong: Công an công bố nguyên nhân ban đầu14:39 11 'quái xế' chạy vào cao tốc Nghi Sơn - Diễn Châu bị phạt 78 triệu đồng501:27
11 'quái xế' chạy vào cao tốc Nghi Sơn - Diễn Châu bị phạt 78 triệu đồng501:27 Tiết lộ về nữ doanh nhân ở Hải Dương nhảy xuống hồ cứu 3 cháu bé02:38
Tiết lộ về nữ doanh nhân ở Hải Dương nhảy xuống hồ cứu 3 cháu bé02:38 CSGT hú còi mở đường cho xe chở người bị điện giật nguy kịch đi cấp cứu01:10
CSGT hú còi mở đường cho xe chở người bị điện giật nguy kịch đi cấp cứu01:10 Thông tin về ô tô 'tự di chuyển' ở sân bay Tân Sơn Nhất09:00
Thông tin về ô tô 'tự di chuyển' ở sân bay Tân Sơn Nhất09:00 Lọ Lem diện áo nhỏ xíu, nhún nhảy hút triệu view, còn được bố ruột làm điều này!03:16
Lọ Lem diện áo nhỏ xíu, nhún nhảy hút triệu view, còn được bố ruột làm điều này!03:16 Mới sinh con 3 tháng, người mẹ trẻ không có đối thủ trên sới vật02:34
Mới sinh con 3 tháng, người mẹ trẻ không có đối thủ trên sới vật02:34 Đi ngược chiều trên cao tốc, nữ tài xế bị phạt 19 triệu đồng01:30
Đi ngược chiều trên cao tốc, nữ tài xế bị phạt 19 triệu đồng01:30 Drama Bộ Tứ Báo Thủ nghi thuê 2 tỷ dàn dựng, người tiết lộ xuất hiện công khai?03:15
Drama Bộ Tứ Báo Thủ nghi thuê 2 tỷ dàn dựng, người tiết lộ xuất hiện công khai?03:15Tiêu điểm
Tin đang nóng
Tin mới nhất

Nữ sinh viên "mất tích" dịp Tết và giây phút gặp lại người thân ở sân bay Tân Sơn Nhất

Xác minh clip cảnh sát giao thông gắt gỏng, chửi thề với cô gái ở TPHCM

Chở trẻ em trên 6 tuổi ngồi trước xe máy sẽ bị xử phạt đến 10 triệu đồng

Xe máy 'kẹp 3' đâm vào gốc cây làm 3 thanh niên tử vong tại chỗ

Một vận động viên tử vong và 2 người bị thương tại giải đua thuyền ở tỉnh Quảng Nam

Dừng xe máy mặc áo mưa có thể bị phạt tới 14 triệu đồng

Nữ sinh mất liên lạc ở TPHCM chính thức lên tiếng

Lái xe "lố" 4 giờ nhưng không thể dừng vì ùn tắc, thiếu trạm nghỉ

Vụ trâu chết la liệt trong rừng: Phát hiện thêm 9 xác trâu

Lật xe khách tại Phú Yên khiến 3 người chết, nhiều người bị thương

Bốn trận động đất liên tiếp trong sáng nay ở Kon Tum

Vụ khe co giãn cao tốc bị bung, nhiều xe nổ lốp: Cục Đường bộ chỉ đạo nóng
Có thể bạn quan tâm

Khối tài sản 5.300 tỷ đồng của Mr Pips được xử lý như thế nào?
Pháp luật
17:55:40 09/02/2025
Argentina nỗ lực chống cháy rừng trong Vườn quốc gia dọc dãy Andes
Thế giới
17:41:08 09/02/2025
Em gái Từ Hy Viên chia sẻ hình ảnh kỷ vật của chị gái, vô tình để lộ chi tiết về lễ tang?
Sao châu á
17:36:02 09/02/2025
Phản ứng ngỡ ngàng của Hương Giang và dàn sao khi nghe "Đen xin xuống đi ngủ, Linh kêu rồi!"
Sao việt
17:32:42 09/02/2025
Bằng chứng sốc: Sao Hỏa từng dễ sống hơn Trái Đất ngày nay?
Lạ vui
17:11:35 09/02/2025
Hot girl người Úc được Thiều Bảo Trâm và dàn dâu nhà giàu theo dõi: Sách mẫu cho mọi cô gái cần tóc đẹp
Làm đẹp
16:28:40 09/02/2025
Xe tang đâm trực diện vào chiếc xe tải, ai nấy đều hãi hùng khi nhìn vào đằng sau
Netizen
16:27:01 09/02/2025
Erik "mất nhiệt" và cú lội ngược dòng ngoạn mục của "hoàng tử ballad"
Nhạc việt
15:59:55 09/02/2025
Các thành viên BLACKPINK bận rộn với các dự án cá nhân trước khi tái hợp
Nhạc quốc tế
15:51:08 09/02/2025
Tử vi tổng quan tuổi Thân năm Ất Tỵ 2025: Sự nghiệp thuận lợi, tài lộc rực rỡ, tình cảm có tin vui
Trắc nghiệm
15:45:05 09/02/2025
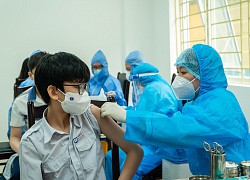 Sở Y tế Hà Nội hướng dẫn về việc tiêm vắc xin COVID-19 mũi 3
Sở Y tế Hà Nội hướng dẫn về việc tiêm vắc xin COVID-19 mũi 3 Đẩy nhanh tự chủ thuốc trị COVID-19
Đẩy nhanh tự chủ thuốc trị COVID-19
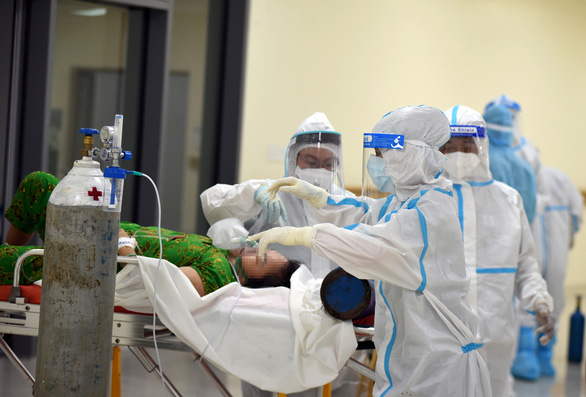



 Bộ Y tế kiểm tra công tác phòng, chống dịch COVID-19 tại An Giang
Bộ Y tế kiểm tra công tác phòng, chống dịch COVID-19 tại An Giang 31 triệu liều vắc xin Pfizer sắp về Việt Nam, đề nghị thông quan nhanh nhất
31 triệu liều vắc xin Pfizer sắp về Việt Nam, đề nghị thông quan nhanh nhất Hơn 500.000 liều vaccine AstraZeneca về tới Việt Nam
Hơn 500.000 liều vaccine AstraZeneca về tới Việt Nam An toàn tiêm chủng là ưu tiên hàng đầu
An toàn tiêm chủng là ưu tiên hàng đầu Bộ Y tế tiếp nhận hỗ trợ 190.000 kit xét nghiệm COVID-19 của 4 bang thuộc Cộng hoà Liên bang Đức
Bộ Y tế tiếp nhận hỗ trợ 190.000 kit xét nghiệm COVID-19 của 4 bang thuộc Cộng hoà Liên bang Đức VCCI góp ý sửa đổi những nội dung gì cho Nghị định về nhãn hàng hóa?
VCCI góp ý sửa đổi những nội dung gì cho Nghị định về nhãn hàng hóa? Nữ sinh mất tích bí ẩn ở TPHCM được tìm thấy tại Trung Quốc
Nữ sinh mất tích bí ẩn ở TPHCM được tìm thấy tại Trung Quốc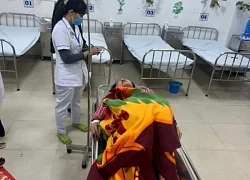 Danh tính các nạn nhân tử vong trong xe khách bị lật ở Phú Yên
Danh tính các nạn nhân tử vong trong xe khách bị lật ở Phú Yên Hành khách trong vụ tai nạn ở Phú Yên: Đi Đà Lạt chụp ảnh cưới thì bị nạn
Hành khách trong vụ tai nạn ở Phú Yên: Đi Đà Lạt chụp ảnh cưới thì bị nạn Danh tính nạn nhân tử vong trong xe khách 54 chỗ bị lật ở Phú Yên
Danh tính nạn nhân tử vong trong xe khách 54 chỗ bị lật ở Phú Yên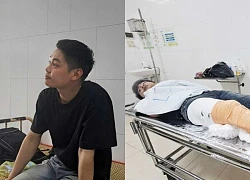 Kinh hoàng vụ lật xe khách tại Phú Yên và lời kể của nạn nhân
Kinh hoàng vụ lật xe khách tại Phú Yên và lời kể của nạn nhân Tài xế xe ôm bị thương nặng sau tai nạn giao thông liên hoàn tại Cầu Giấy, Hà Nội
Tài xế xe ôm bị thương nặng sau tai nạn giao thông liên hoàn tại Cầu Giấy, Hà Nội Người phụ nữ tìm được gia đình sau 32 năm bị lừa bán sang Trung Quốc
Người phụ nữ tìm được gia đình sau 32 năm bị lừa bán sang Trung Quốc Nữ sinh Sơn La 17 tuổi mất tích: Gia đình nhận tin con gái ở Cần Thơ
Nữ sinh Sơn La 17 tuổi mất tích: Gia đình nhận tin con gái ở Cần Thơ Chồng Từ Hy Viên lâm nguy: Giam mình, không mở miệng nói chuyện vì lý do này sau cú sốc mất vợ
Chồng Từ Hy Viên lâm nguy: Giam mình, không mở miệng nói chuyện vì lý do này sau cú sốc mất vợ Khách tố quán bánh mì ở Hà Nội bán 'thịt mốc đen', chủ quán phản bác ra sao?
Khách tố quán bánh mì ở Hà Nội bán 'thịt mốc đen', chủ quán phản bác ra sao? Chồng cũ Từ Hy Viên nổi điên, mẹ chồng cũ "mặt dày" la lối sau khi dính đòn trừng phạt nặng
Chồng cũ Từ Hy Viên nổi điên, mẹ chồng cũ "mặt dày" la lối sau khi dính đòn trừng phạt nặng
 Từ Hy Viên vừa qua đời 7 ngày, hình ảnh gia đình tụ tập bên bánh kem gây dậy sóng MXH
Từ Hy Viên vừa qua đời 7 ngày, hình ảnh gia đình tụ tập bên bánh kem gây dậy sóng MXH
 HOT: Quỳnh Lương tổ chức đám cưới với thiếu gia Trà Vinh
HOT: Quỳnh Lương tổ chức đám cưới với thiếu gia Trà Vinh 3 năm với chồng mới là thời gian hạnh phúc nhất cuộc đời Từ Hy Viên
3 năm với chồng mới là thời gian hạnh phúc nhất cuộc đời Từ Hy Viên Bức ảnh làm lộ chuyện 2 con Từ Hy Viên bị bỏ bê nghiêm trọng sau khi đột ngột mất mẹ
Bức ảnh làm lộ chuyện 2 con Từ Hy Viên bị bỏ bê nghiêm trọng sau khi đột ngột mất mẹ Ca sĩ Lynda Trang Đài sau khi bị bắt vì ăn trộm: Có động thái lạ trên MXH, dàn sao hé lộ tình trạng bất ổn
Ca sĩ Lynda Trang Đài sau khi bị bắt vì ăn trộm: Có động thái lạ trên MXH, dàn sao hé lộ tình trạng bất ổn Nóng: Tro cốt Từ Hy Viên bị phản đối đặt tại nhà, gia đình phải đưa ra quyết định an táng gây xót xa
Nóng: Tro cốt Từ Hy Viên bị phản đối đặt tại nhà, gia đình phải đưa ra quyết định an táng gây xót xa Đòn trừng phạt chồng cũ Từ Hy Viên và mẹ chồng cũ sau trò lố lợi dụng cái chết của minh tinh
Đòn trừng phạt chồng cũ Từ Hy Viên và mẹ chồng cũ sau trò lố lợi dụng cái chết của minh tinh Đoạn văn 85 chữ miêu tả ông nội của học sinh tiểu học khiến cả cõi mạng cười bò, "nạn nhân" đọc xong ho nguyên 1 bản giao hưởng
Đoạn văn 85 chữ miêu tả ông nội của học sinh tiểu học khiến cả cõi mạng cười bò, "nạn nhân" đọc xong ho nguyên 1 bản giao hưởng
 Thiều Bảo Trâm đăng đàn ẩn ý, 1 chi tiết dự sắp bùng drama giữa lúc tình cũ nghi hẹn hò Hoa hậu?
Thiều Bảo Trâm đăng đàn ẩn ý, 1 chi tiết dự sắp bùng drama giữa lúc tình cũ nghi hẹn hò Hoa hậu? Đạo diễn 'vượt mặt' cả Trấn Thành và Thu Trang là ai?
Đạo diễn 'vượt mặt' cả Trấn Thành và Thu Trang là ai? Bị truy đuổi, tên trộm bơi qua sông nhưng không thoát nên dùng dao tự sát
Bị truy đuổi, tên trộm bơi qua sông nhưng không thoát nên dùng dao tự sát