Bộ Y tế khẳng định EVUSHELD là thuốc, không phải là ’siêu vaccine’, không được phép sử dụng để dự phòng COVID-19
Chiều ngày 18/3, Cục Quản lý Dược -Bộ Y tế phát đi thông tin khẳng định EVUSHELD là thuốc, không phải là “siêu vaccine”, không được phép sử dụng EVUSHELD để dự phòng COVID-19 cho các đối tượng có thể tiêm vaccine.
Chiều ngày 18/3, thông tin từ Cục quản lý Dược- Bộ Y tế cho biết, để đa dạng nguồn cung thuốc phòng và điều trị COVID-19, ngày 2/3, Bộ Y tế đã căn cứ các quy định hiện hành để cấp Giấy phép nhập khẩu thuốc EVUSHELD đáp ứng nhu cầu điều trị đặc biệt của cơ sở khám chữa bệnh.
Cho đến nay, EVUSHELD đã được cấp phép lưu hành trong tình trạng khẩn cấp tại một số quốc gia như: Mỹ, Pháp, Các tiểu vương quốc Ả Rập thống nhất, Bahrain…
EVUSHELD là thuốc, không phải là “siêu vaccine”, không được phép sử dụng để dự phòng COVID-19.
EVUSHELD là thuốc, không phải vaccine. EVUSHELD không chỉ định dùng thay thế cho vaccine COVID-19 đối với những trường hợp có thể tiêm được vaccine.
Video đang HOT
Bản chất, EVUSHELD gồm 01 liều kháng thể đơn dòng tixagevimab và 01 liều kháng thể đơn dòng cilgavimab. Việc sử dụng thuốc cần phải được bác sĩ đánh giá thỏa đáng và sàng lọc chặt chẽ trước khi được xác định là đối tượng sử dụng phù hợp.
Một liều thuốc được chỉ định để dự phòng mắc bệnh COVID-19 trong thời gian ít nhất 6 tháng (với các dữ liệu hiện có) cho người lớn và trẻ em từ 12 tuổi có cân nặng từ 40kg trở lên với điều kiện các đối tượng này không đang nhiễm SARS-CoV-2 và không có tiếp xúc với người nhiễm SARS-CoV-2 được xác định và phải thuộc một trong các trường hợp sau:
- Có suy giảm miễn dịch mức độ vừa đến nặng do một tình trạng bệnh lý hoặc sử dụng các thuốc hoặc phác đồ điều trị ức chế miễn dịch và có khả năng không tạo được đáp ứng miễn dịch thỏa đáng đối với vaccine COVID-19.
- Không thể tiêm bất kỳ loại vaccine COVID-19 nào hiện có vì có tiền sử xảy ra tác dụng ngoại ý nghiêm trọng (ví dụ như dị ứng nặng) với bất kỳ thành phần nào của vaccine COVID-19.
Theo khuyến cáo của nhà sản xuất, các tình trạng y khoa hoặc phương pháp điều trị có thể dẫn tới suy giảm miễn dịch mức độ vừa đến nặng và đáp ứng miễn dịch không thỏa đáng đối với vaccine COVID-19 bao gồm nhưng không giới hạn:
Đang điều trị đối với các khối u đặc và bệnh lý huyết học ác tính . Cấy ghép nội tạng và đang điều trị với liệu pháp ức chế miễn dịchTiếp nhận tế bào lympho T chứa thụ thể kháng nguyên dạng khảm (CAR)-T hoặc cấy ghép tế bào gốc tạo máu (trong vòng 2 năm sau khi cấy ghép hoặc đang điều trị ức chế miễn dịch).Suy giảm miễn dịch nguyên phát mức độ vừa đến nặng (ví dụ, hội chứng DiGeorge, hội chứng Wiskott-Aldrich).Nhiễm HIV giai đoạn tiến triển hoặc chưa được điều trị (những người nhiễm HIV với số lượng tế bào CD4 Điều trị tích cực bằng corticosteroid liều cao (nghĩa là 20 mg prednisone hoặc tương đương mỗi ngày khi dùng trong 2 tuần), tác nhân alkyl hóa, chất chống chuyển hóa, thuốc ức chế miễn dịch liên quan đến cấy ghép, tác nhân hóa trị ung thư được phân loại là ức chế miễn dịch mức độ nặng, thuốc ức chế yếu tố hoại tử khối u (TNF), và các tác nhân sinh học khác có tác dụng ức chế miễn dịch hoặc điều hòa miễn dịch (ví dụ, tác nhân ức chế tế bào B).
Hiện nay, EVUSHELD chưa được cấp phép sử dụng ở đối tượng đang điều trị COVID-19, hoặc dự phòng sau phơi nhiễm COVID-19 ở những người đã tiếp xúc với người nhiễm SARS-CoV-2.
Tại Việt Nam, EVUSHELD được cấp giấy phép nhập khẩu để sử dụng trong cơ sở khám chữa bệnh. Người bệnh phải được cơ sở khám chữa bệnh thông tin về tình trạng hồ sơ cấp phép của thuốc và cơ sở chỉ được sử dụng thuốc khi có sự đồng ý của bệnh nhân hoặc người nhà của bệnh nhân.
Như vậy, EVUSHELD là thuốc, không phải là “siêu vaccine”, không được phép sử dụng EVUSHELD để dự phòng COVID-19 cho các đối tượng có thể tiêm vaccine.
Mỹ mua bổ sung 500.000 liều Evusheld
Nhà sản xuất dược phẩm AstraZeneca (Anh-Thụy Điển) ngày 12/1 cho biết Chính phủ Mỹ đã nhất trí mua thêm 500.000 liều hỗn hợp kháng thể Evusheld để điều trị cho các bệnh nhân COVID-19.
Chính phủ Mỹ đã nhất trí mua thêm 500.000 liều hỗn hợp kháng thể Evusheld để điều trị cho các bệnh nhân COVID-19. Ảnh minh họa: Reuters
Theo thông báo của AstraZeneca, việc vận chuyển lô thuốc bổ sung trên dự kiến được thực hiện trong quý I/2022 và chi tiết về hợp đồng này sẽ được công bố trong những tuần tới.
AstraZeneca cũng nhấn mạnh thêm rằng đây là liệu pháp kháng thể duy nhất cho đến nay được cấp phép tại Mỹ để điều trị COVID-19.
Trước đó, Chính phủ Mỹ đã mua 700.000 liều Evusheld. Theo các kết quả thử nghiệm giai đoạn cuối được công bố vào tháng 8 năm ngoái, Evusheld giúp giảm 77% nguy cơ triệu chứng bệnh trở nặng ở người mắc COVID-19. Vào tháng 12, loại hỗn hợp kháng thể được tạo thành từ hai loại kháng thể đơn dòng tixagevimab và cilgavimab này đã chứng tỏ được khả năng phòng ngừa biến thể Omicron trong một nghiên cứu ở phòng thí nghiệm. Ngày 8/12, Cơ quan Quản lý Thực phẩm và Dược phẩm (FDA) Mỹ đã cấp phép sử dụng Evusheld để ngăn ngừa COVID-19 ở những người có hệ thống miễn dịch kém hoặc có tiền sử bị tác dụng phụ với các vaccine phòng bệnh này.
*Trong một diễn biến khác ngày 12/1, Thủ tướng Canada Justin Trudeau tuyên bố tỷ lệ trẻ nhỏ tại nước này được tiêm vaccine ngừa COVID-19 còn hạn chế ở thời điểm hiện tại khi biến thể Omicron đe dọa gây quá tải đối với hệ thống y tế trên cả nước.
Phát biểu họp báo thường kỳ, Thủ tướng Trudeau nêu rõ hiện mới chỉ có gần 50% trẻ em trên toàn Canada được tiêm vaccine ngừa COVID-19. Do đó, ông nhấn mạnh cần đẩy nhanh nỗ lực tiêm phòng cho nhóm này.
Tuyên bố trên được đưa ra tại thời điểm nhiều trường học ở Canada dự kiến sẽ nối lại chương trình học tập trực tiếp vào những ngày tới, chẳng hạn như các trường ở hai tỉnh Ontario và Quebec sẽ mở cửa lại vào ngày 17/1 này.
Theo thống kê chính thức, tính đến ngày 1/1/2022, có 87,6% trẻ trên 12 tuổi tại Canada đã được tiêm hai mũi vaccine. Tuy nhiên, tỷ lệ này ở nhóm từ 5-12 tuổi giảm xuống chỉ còn 2% và trong nhóm tuổi này, mới chỉ có 45,6% trẻ được tiêm một mũi vaccine.
Pháp phê duyệt liệu pháp kháng thể cho các trường hợp có nguy cơ cao mắc COVID-19  Theo phóng viên TTXVN tại Paris, các cơ quan y tế Pháp đã phê duyệt việc sử dụng một phương pháp điều trị kháng thể do AstraZeneca sản xuất cho những người có nguy cơ cao, có biểu hiện kháng vaccine phòng COVID-19. Điều trị cho bệnh nhân mắc COVID-19 tại bệnh viện ở Martinique thuộc Pháp ngày 1/12/2021. Ảnh minh họa: AFP/TTXVN...
Theo phóng viên TTXVN tại Paris, các cơ quan y tế Pháp đã phê duyệt việc sử dụng một phương pháp điều trị kháng thể do AstraZeneca sản xuất cho những người có nguy cơ cao, có biểu hiện kháng vaccine phòng COVID-19. Điều trị cho bệnh nhân mắc COVID-19 tại bệnh viện ở Martinique thuộc Pháp ngày 1/12/2021. Ảnh minh họa: AFP/TTXVN...
 Sự cố chấn động điền kinh: VĐV bị đối thủ vụt gậy vào đầu, nghi vỡ hộp sọ02:05
Sự cố chấn động điền kinh: VĐV bị đối thủ vụt gậy vào đầu, nghi vỡ hộp sọ02:05 TP.HCM: Xôn xao clip nhóm người ngang nhiên chặn xe kiểm tra giấy tờ06:11
TP.HCM: Xôn xao clip nhóm người ngang nhiên chặn xe kiểm tra giấy tờ06:11 Kế hoạch bắt cóc người đàn ông Trung Quốc, tống tiền 10 tỷ đồng ở TPHCM13:48
Kế hoạch bắt cóc người đàn ông Trung Quốc, tống tiền 10 tỷ đồng ở TPHCM13:48 Ông Trump gợi ý ông Zelensky có thể ra đi vì từ chối thỏa thuận08:44
Ông Trump gợi ý ông Zelensky có thể ra đi vì từ chối thỏa thuận08:44 Ông Trump muốn đàm phán lại biên giới Mỹ - Canada07:42
Ông Trump muốn đàm phán lại biên giới Mỹ - Canada07:42 Trung Quốc gửi thông điệp cứng rắn đến Đài Loan08:38
Trung Quốc gửi thông điệp cứng rắn đến Đài Loan08:38 Ông Trump phát biểu tại quốc hội, một nghị sĩ bị mời ra ngoài09:32
Ông Trump phát biểu tại quốc hội, một nghị sĩ bị mời ra ngoài09:32 Hàn Quốc: Hàng chục ngàn người xuống đường sau khi ông Yoon Suk Yeol được thả01:03
Hàn Quốc: Hàng chục ngàn người xuống đường sau khi ông Yoon Suk Yeol được thả01:03 TSMC đầu tư 100 tỉ USD vào Mỹ, Đài Loan nói Mỹ sẽ không bỏ Indo-Pacific08:14
TSMC đầu tư 100 tỉ USD vào Mỹ, Đài Loan nói Mỹ sẽ không bỏ Indo-Pacific08:14 Dồn dập diễn biến chiến tranh thuế quan08:30
Dồn dập diễn biến chiến tranh thuế quan08:30 Kế hoạch xoay chiều cục diện ở Gaza09:14
Kế hoạch xoay chiều cục diện ở Gaza09:14Tiêu điểm
Tin đang nóng
Tin mới nhất

Thực phẩm an toàn cho người cao huyết áp

Dịch sởi diễn biến phức tạp tại một số địa phương
5 bài thuốc giảm mỡ máu hiệu quả

Nhiều người bị chẩn đoán nhầm u não, ung thư... do mắc bệnh giun sán
Dấu hiệu nhận biết trẻ mắc bệnh tay chân miệng
Bệnh sởi ở trẻ nhỏ: Cẩn trọng trước những biến chứng nguy hiểm
Một loại vaccine phụ nữ mang thai không nên bỏ qua

Những thực phẩm người lớn tuổi nên ăn thường xuyên

Mua thuốc giảm đau đầu cho chồng, vợ bất ngờ khi nghe lý do dược sĩ từ chối bán

Cứu sống bệnh nhân người Lào bị sốc nhiễm khuẩn, suy đa tạng
Những cách phòng tránh bệnh lý xương khớp dễ gặp vào mùa xuân

Thời điểm cần nhập viện khi bị sốt do cúm A
Có thể bạn quan tâm

Hệ quả từ những thay đổi chính sách của Tổng thống Trump
Thế giới
12:47:09 12/03/2025
Sự cố "hớ hênh" của Jennie bị biến thành trò đùa tình dục, netizen kịch liệt lên án
Nhạc quốc tế
11:58:28 12/03/2025
Kim Sae Ron từng công khai thể hiện tình yêu với Kim Soo Hyun ở phim trường và đây là cách tài tử phản ứng
Sao châu á
11:54:06 12/03/2025
Vụ ngụy trang đất hiếm 'tuồn' ra nước ngoài: Bộ Công an truy nã Lưu Đức Hoa
Pháp luật
11:26:18 12/03/2025
Để con 2 tuổi tự chơi với chó Golden, cảnh tượng sau đó khiến người mẹ chết điếng người
Netizen
11:16:35 12/03/2025
Chu Thanh Huyền - vợ Quang Hải đáp trả khi bị so sánh chỉ bằng một nửa nàng dâu hào môn Phương Nhi
Sao thể thao
11:06:16 12/03/2025
Điều đặc biệt ở sa mạc Sahara trông như một viễn cảnh ngoài hành tinh
Lạ vui
11:02:21 12/03/2025
Người phụ nữ 31 tuổi sống một mình trong căn hộ tối giản, đẹp mê: Đi đâu cũng không bằng về nhà
Sáng tạo
10:57:13 12/03/2025
Đánh hội đồng nữ sinh lớp 7 rồi tung clip lên mạng xã hội
Tin nổi bật
10:45:55 12/03/2025
7 sai lầm trong việc skincare có thể hủy hoại làn da của bạn
Làm đẹp
10:33:46 12/03/2025
 Tự điều trị Covid-19 tại nhà cho con bạn, khi nào cần gọi bác sĩ?
Tự điều trị Covid-19 tại nhà cho con bạn, khi nào cần gọi bác sĩ? Phẫu thuật thành công cho nam thanh niên bị cụt chi do máy cắt cỏ
Phẫu thuật thành công cho nam thanh niên bị cụt chi do máy cắt cỏ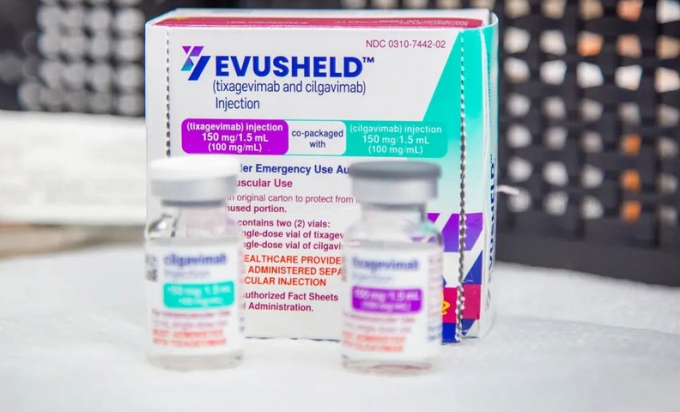
 FDA Mỹ cấp phép sử dụng hỗn hợp kháng thể Evusheld của AstraZeneca
FDA Mỹ cấp phép sử dụng hỗn hợp kháng thể Evusheld của AstraZeneca AstraZeneca tuyên bố thuốc kháng thể chống COVID-19 có hiệu quả bảo vệ trong 6 tháng
AstraZeneca tuyên bố thuốc kháng thể chống COVID-19 có hiệu quả bảo vệ trong 6 tháng Chảy máu vùng miệng không ngừng, cô gái trẻ được chẩn đoán suy thận giai đoạn cuối
Chảy máu vùng miệng không ngừng, cô gái trẻ được chẩn đoán suy thận giai đoạn cuối Phát hiện phương pháp điều trị đầy hứa hẹn cho ung thư gan ác tính
Phát hiện phương pháp điều trị đầy hứa hẹn cho ung thư gan ác tính Viêm tuyến giáp Hashimoto có biểu hiện như thế nào?
Viêm tuyến giáp Hashimoto có biểu hiện như thế nào? U40 gặp dấu hiệu này chứng tỏ xương đang lão hóa nhanh, dễ mắc bệnh
U40 gặp dấu hiệu này chứng tỏ xương đang lão hóa nhanh, dễ mắc bệnh Điều gì xảy ra khi luôn uống một cốc cà phê mỗi sáng?
Điều gì xảy ra khi luôn uống một cốc cà phê mỗi sáng? Những thuốc nào cần uống sau khi bị đột quỵ?
Những thuốc nào cần uống sau khi bị đột quỵ? Bánh mì kết hợp cùng loại gia vị quen thuộc này, càng ăn càng sống thọ
Bánh mì kết hợp cùng loại gia vị quen thuộc này, càng ăn càng sống thọ Cứu sống người phụ nữ ngộ độc nguy kịch do ăn cá nóc
Cứu sống người phụ nữ ngộ độc nguy kịch do ăn cá nóc Công nhân vệ sinh tìm thấy 7 kg vàng trị giá hơn 17 tỷ đồng trong thùng rác sân bay
Công nhân vệ sinh tìm thấy 7 kg vàng trị giá hơn 17 tỷ đồng trong thùng rác sân bay
 Ngày tàn của Kim Soo Hyun đã đến: 15 thương hiệu cao cấp xếp hàng chờ bồi thường, có nguy cơ nhận án tù?
Ngày tàn của Kim Soo Hyun đã đến: 15 thương hiệu cao cấp xếp hàng chờ bồi thường, có nguy cơ nhận án tù? Hoang mang tột độ: Kim Sae Ron bị công ty Kim Soo Hyun ép đi tiếp khách, uống rượu trước khi gây tai nạn?
Hoang mang tột độ: Kim Sae Ron bị công ty Kim Soo Hyun ép đi tiếp khách, uống rượu trước khi gây tai nạn? Công an TP HCM thông tin về clip CSGT có lời nói chưa chuẩn mực
Công an TP HCM thông tin về clip CSGT có lời nói chưa chuẩn mực Rầm rộ tin Won Bin trả nợ 12 tỷ cho Kim Sae Ron, Kim Soo Hyun bị chê chỉ đáng xách dép
Rầm rộ tin Won Bin trả nợ 12 tỷ cho Kim Sae Ron, Kim Soo Hyun bị chê chỉ đáng xách dép Đi làm về khuya, mọi người đều đi ngủ, chỉ duy nhất bố chồng còn thức đợi, câu đầu tiên ông nói khiến tôi bật khóc nức nở
Đi làm về khuya, mọi người đều đi ngủ, chỉ duy nhất bố chồng còn thức đợi, câu đầu tiên ông nói khiến tôi bật khóc nức nở Nam thần VTV một thời nghỉ việc ở nhà hát, giờ phụ vợ bán bún riêu, dắt xe cho khách vẫn vui vẻ
Nam thần VTV một thời nghỉ việc ở nhà hát, giờ phụ vợ bán bún riêu, dắt xe cho khách vẫn vui vẻ Sau Lê Phương, thêm 1 sao nữ lên livestream ẩn ý về người diễn giả trân trong tang lễ của Quý Bình
Sau Lê Phương, thêm 1 sao nữ lên livestream ẩn ý về người diễn giả trân trong tang lễ của Quý Bình Lê Phương chia sẻ ẩn ý sau tang lễ Quý Bình, netizen nghi ngờ liên quan đến vợ của cố nghệ sĩ
Lê Phương chia sẻ ẩn ý sau tang lễ Quý Bình, netizen nghi ngờ liên quan đến vợ của cố nghệ sĩ Drama dồn dập: "Ông hoàng" Châu Kiệt Luân đánh bài thua hơn 3.500 tỷ, phải thế chấp 3 biệt thự và 1 máy bay riêng?
Drama dồn dập: "Ông hoàng" Châu Kiệt Luân đánh bài thua hơn 3.500 tỷ, phải thế chấp 3 biệt thự và 1 máy bay riêng?
 Lê Phương gây hoang mang khi đăng status sau tang lễ Quý Bình, nhiều nghệ sĩ vào bình luận ẩn ý
Lê Phương gây hoang mang khi đăng status sau tang lễ Quý Bình, nhiều nghệ sĩ vào bình luận ẩn ý Bị chỉ trích "khóc không có giọt nước mắt" trong đám tang Quý Bình, một nữ nghệ sĩ lên tiếng
Bị chỉ trích "khóc không có giọt nước mắt" trong đám tang Quý Bình, một nữ nghệ sĩ lên tiếng

 Kim Soo Hyun chính thức "phản đòn" livestream bóc phốt: Nghe mà hoang mang tột độ!
Kim Soo Hyun chính thức "phản đòn" livestream bóc phốt: Nghe mà hoang mang tột độ!